技术分享:揭示神经-上皮-免疫轴调节皮肤免疫监视机制
屏障组织时刻发挥着宿主防御和免疫监视功能,这一过程是由静态的结构成分和运动的免疫细胞相互作用协调完成。上皮细胞建立起物理屏障并向下方组织传递信号,免疫细胞则负责持续监视着这些界面。此外,神经密集分布于屏障组织内,传递着感觉和自主神经信号,扮演着上皮完整性和免疫监视的关键调节者[1]。神经通过与上皮和免疫细胞的双向通讯,帮助维持组织内稳态,并响应生理变化或病原体侵袭来调动适应性反应[2]。然而,上皮、免疫和神经这三类细胞在生理稳态维持和疾病发生过程中的协同作用机制仍不清楚。
皮肤驻留记忆CD8⁺ T(TRM)细胞是驻留在上皮区域内的关键免疫哨兵[3]。它们起源于淋巴器官中的效应T细胞 (TEFF),部分TEFF在组织归巢趋化因子和粘附分子的引导下迁移到皮肤[4],接收到局部信号转化定居下来,以响应共生微生物群、病原体或恶性细胞的抗原激活。CD8⁺ TRM细胞驻留在毛囊间表皮及上部毛囊内[5],当再次遇到局部抗原或炎症刺激时,它们能迅速分泌效应细胞因子,如肿瘤坏死因子-α (TNF-α) 和干扰素-γ (IFN-γ)。通过这种“感知与警报”机制,TRM细胞不仅发挥着即刻保护作用,还能招募和激活其他免疫细胞进一步增强局部免疫反应[6]。TRM细胞的保护能力与其丰度密切相关,充足的TRM池能赋予机体强大的局部免疫力,不足则可能使病原体得以扩散或肿瘤得以进展。然而,影响皮肤CD8⁺ TRM细胞丰度及其战略定位的上皮与神经信号机制,至今仍未明确。外周神经系统被视为在屏障部位(如肠道、肺和皮肤)调控免疫反应的关键协调者[7]。神经元输出能快速响应环境和生理变化,但这些信号如何影响屏障组织中TRM细胞动态及局部免疫监视,目前也尚不明确。
2026年1月,Cell期刊报道了一项研究,揭示由皮肤上皮介导了神经系统与免疫系统之间的协同作用机制,发现皮肤交感神经与表皮角质形成细胞密切互作,间接调控组织常驻记忆CD8⁺ T(TRM)细胞的局部丰度,进而影响区域内的肿瘤免疫监视强度。具体而言,这些交感神经并不直接与CD8⁺ TRM细胞接触,而是在表皮基底层附近形成类似突触样结构,并通过去甲肾上腺素-ADRB2信号通路动态调控皮肤CD8⁺ TRM细胞形成所必需的上皮来源CXCL16趋化因子,后者协调CD8⁺ TRM细胞的招募与定位。该研究阐明了一种全身神经输入信号调节组织免疫监视强度的“神经-上皮-免疫”轴,这一机制对于理解区域化免疫监视及组织中肿瘤发展的早期步骤至关重要[8]。
首先,研究者探究了小鼠皮肤CD8⁺ TRM细胞是否受外周神经信号调控,检测其相对于上皮细胞和交感神经(皮肤中主要的外周神经类型)的分布情况。免疫荧光染色证实,CD8⁺ TRM细胞主要位于毛囊间表皮和毛囊上部,且未与交感神经直接接触(图一A)。流式分析进一步确认这些CD8⁺ T细胞胞大多表达皮肤TRM标志物如CD69和CD103、以及TNF-α和IFN-γ(图一B)。整体免疫荧光染色清晰显示,交感神经在皮肤上皮层形成密集网络,且CD8⁺ TRM细胞散布其中(图一C)。为探究皮肤交感信号是否影响CD8⁺ TRM细胞,使用选择性神经毒素6-羟基多巴胺(6-OHDA)特异性消融皮肤交感神经[9]。交感神经消融后,皮肤中CD8⁺ TRM细胞数量显著增加(图一D),其中表皮区的增幅最为显著,真皮区亦有轻微上升(图一E)。在交感神经消融后至少6周内,TRM细胞数量持续保持高位(图一E),直至14周后随着交感神经纤维开始重新支配皮肤才逐渐回落。利用DBHCre; ROSAiDTR小鼠进行基因介导的交感神经消融,同样观察到CD8⁺ TRM细胞的增加。以上数据表明,皮肤交感神经虽不直接接触CD8⁺ TRM细胞,但对其丰度的调控有着重要作用。
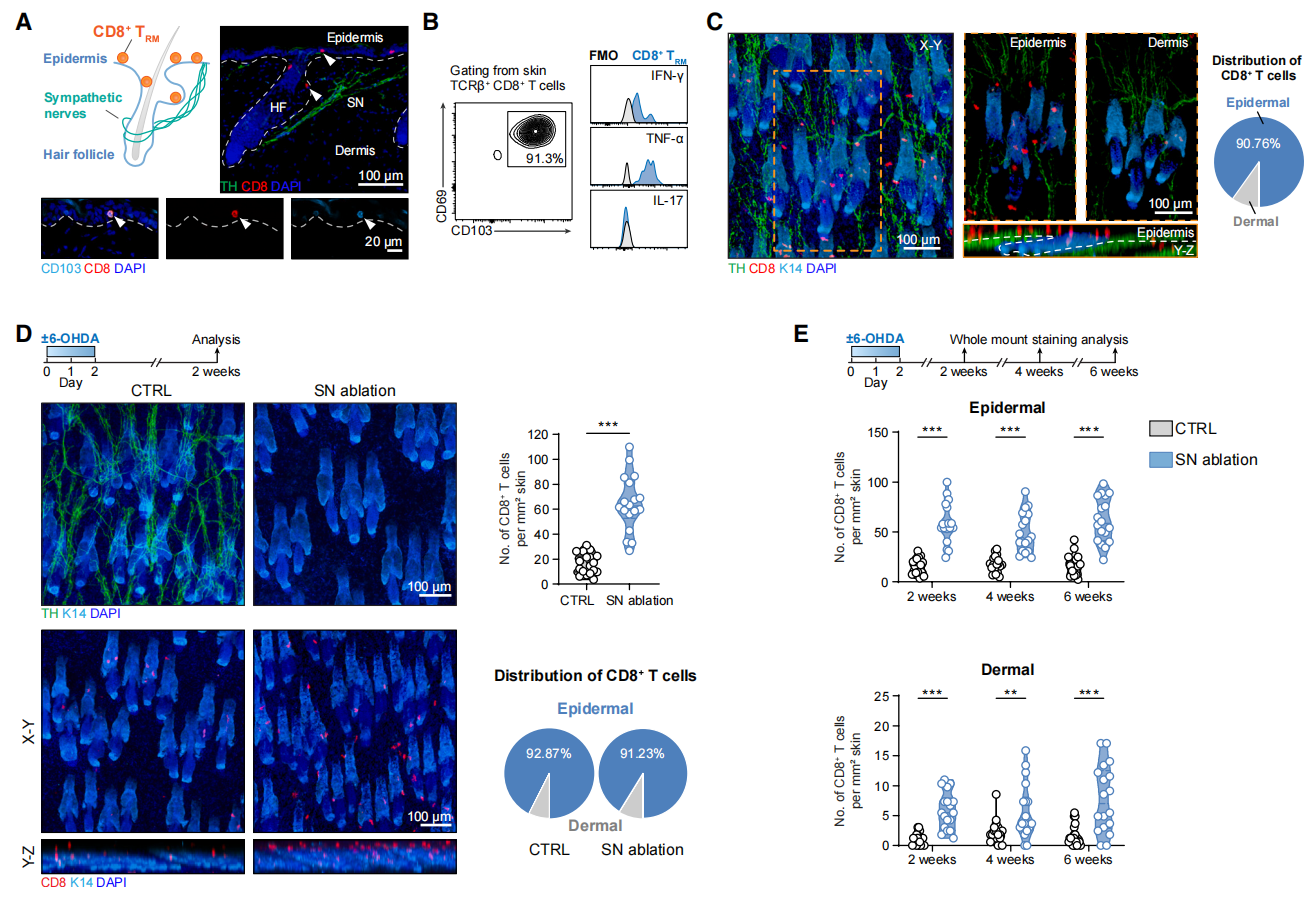
图一 交感神经消融可增加皮肤中的CD8⁺ TRM细胞[8]
接着,研究者采用DREADD化学遗传学系统[10]探究交感神经的神经元信号是否影响皮肤CD8⁺ TRM细胞。构建DBHCre; R26-LSL-Gi-DREADD小鼠(Gi-DREADD),其交感神经元中表达工程化Gαi/o蛋白偶联受体,给予氯氮平N-氧化物(CNO)后可抑制神经元活性(图二A)。通过腹腔注射CNO进行全身性交感抑制,快速引起皮肤CD8⁺ T细胞增加(图二B)。该效应具有瞬时性,首次CNO给药后2天内,表皮和真皮中的CD8+ T细胞均显著上升,可维持约1周的高位水平,2周后恢复至基线水平(图二C)。流式分析确认,增加的细胞群主要由CD69+ CD103+ CD8+ TRM细胞构成(图二D)。从对照组和Gi-DREADD小鼠背部皮肤中分离出T细胞,转录组分析证实在两组小鼠中,CD8+ TRM 细胞均占所有T细胞的主导地位,且高表达经典驻留标志物和转录因子如Cd69、Itgae(CD103)和Znf683(Hobit),低表达Ccr7、Klrg1和Sell(CD62L)(图二E),表明抑制交感神经可导致皮肤CD8⁺ TRM出现可逆性激增,且不会显著改变其身份或功能状态。为探究CD8⁺ TRM细胞的增加是否依赖于皮肤中的局部交感信号,研究者将CNO皮内注射到Gi-DREADD小鼠背部的一小块区域,同时在另一侧的镜像区域注射生理盐水作为对照 (图二F)。局部CNO递送也导致CNO注射部位的CD8⁺ TRM细胞密度显著高于对照部位 (图二F),表明在皮肤中局部抑制交感信号足以增加CD8⁺ TRM群体 (图二 G)。
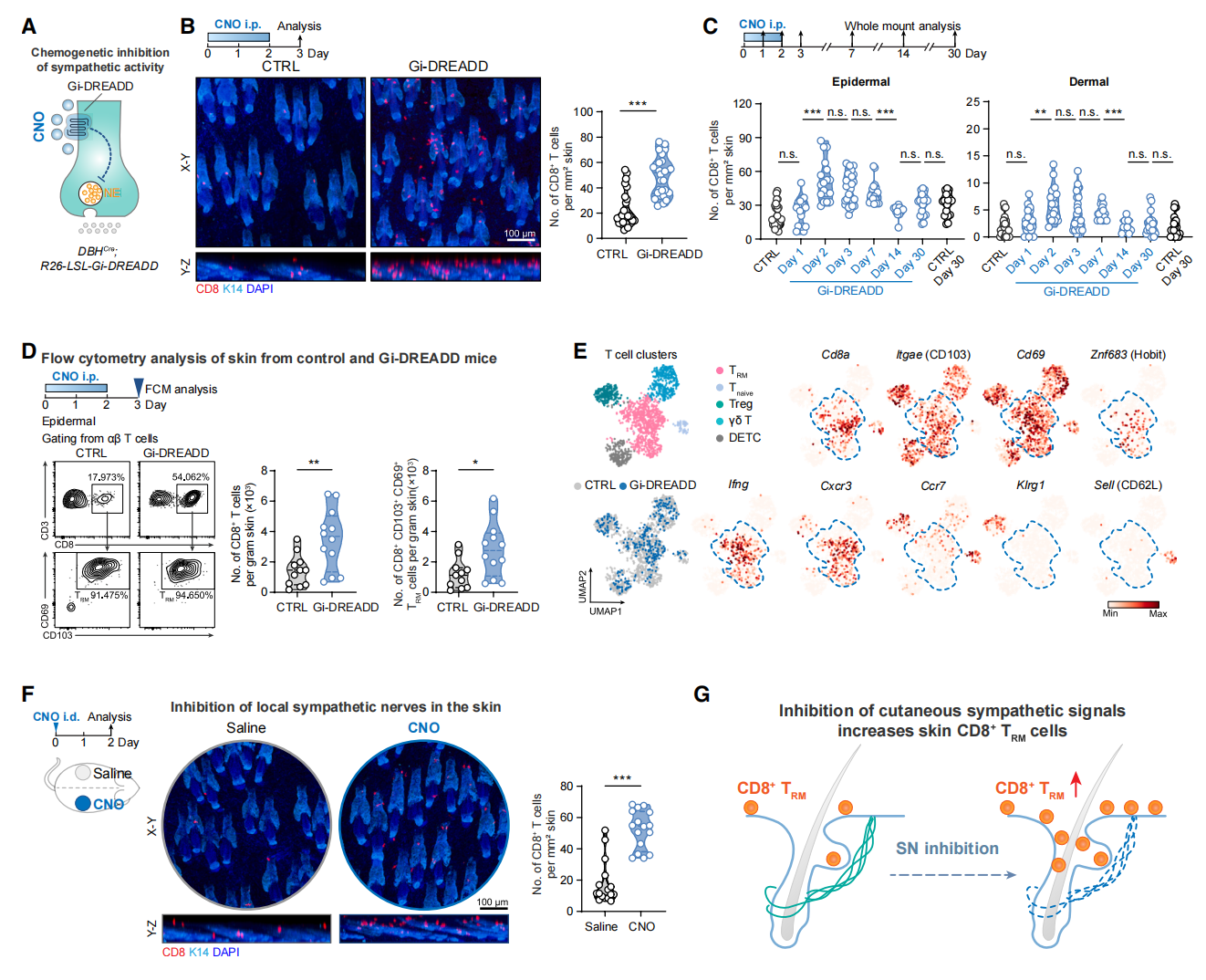
图二 抑制交感神经信号可增加皮肤CD8⁺ TRM细胞池[8]
作为自主神经系统的重要组成部分,交感神经系统通过持续活动维持心率和血流等生命活动[11]。交感神经释放去甲肾上腺素 (NE),NE与靶细胞上的肾上腺素能受体结合并激活下游信号通路,从而调节各种细胞过程 (图三A)。为了测试在皮肤中局部抑制NE-肾上腺素能受体信号传导是否能模拟交感抑制对CD8⁺ TRM细胞的影响,研究者在小鼠背部皮肤的一侧皮内注射一种β-肾上腺素能受体阻滞剂纳多洛尔。与对侧注射生理盐水的部位相比,纳多洛尔处理显著增加了注射部位的CD8⁺ TRM细胞数量 (图三B)。为确定NE在皮肤中负责调控CD8⁺ TRM细胞的直接细胞靶点。研究者利用scRNA-seq分析小鼠主要皮肤细胞类型中的肾上腺素能受体表达情况。结果显示,β2-肾上腺素能受体Adrb2的表达最为显著(图三C)。随后,研究者敲除了不同皮肤免疫细胞群体中的Adrb2基因,检测其是否能模拟交感抑制的表型(图三D)。发现在T细胞、调节性T细胞、树突状细胞和其他髓系细胞群体中条件性敲除Adrb2,均未改变皮肤CD8⁺ TRM细胞的数量(图三E和F),表明交感信号并非通过直接靶向T细胞或间接通过髓系细胞来调控CD8⁺ TRM细胞的丰度。Adrb2在表皮角质形成细胞中的表达水平和细胞比率最高(图三C),提示皮肤上皮可能是关键的中间媒介。皮肤交感神经主要分布于毛囊间表皮和毛囊之间,其中一部分交感神经轴突末端终止于表皮基底层附近(图三G)。这些轴突与支配立毛肌的神经纤维相互独立,呈现出类似储存神经递质的轴突膨体结构,并与突触前标志物囊泡单胺转运蛋白2(VMAT2)和突触素存在共定位现象(图三H)。透射电子显微镜进一步揭示了这些交感神经末梢内存在典型的突触小泡结构(图三I)。为探究交感神经与表皮角质形成细胞之间的NE-ADRB2信号传导是否调控皮肤CD8⁺ TRM细胞丰度,研究者构建K14rtTA; TetOCre; Adrb2fl/fl小鼠模型,通过强力霉素诱导角质形成细胞特异性Adrb2基因敲除。表皮角质形成细胞中Adrb2的缺失显著增加了皮肤CD8⁺ TRM细胞数量,完美重现了交感抑制的表型(图三J)。进一步皮内注射局部补充NE并不能逆转小鼠中升高的TRM细胞数量(图三K),确证了该表型特异性源于角质形成细胞中ADRB2的缺失。以上数据表明,皮肤交感神经通过ADRB2向表皮角质形成细胞传递信号,间接调控局部CD8⁺ TRM细胞丰度(图三L)。
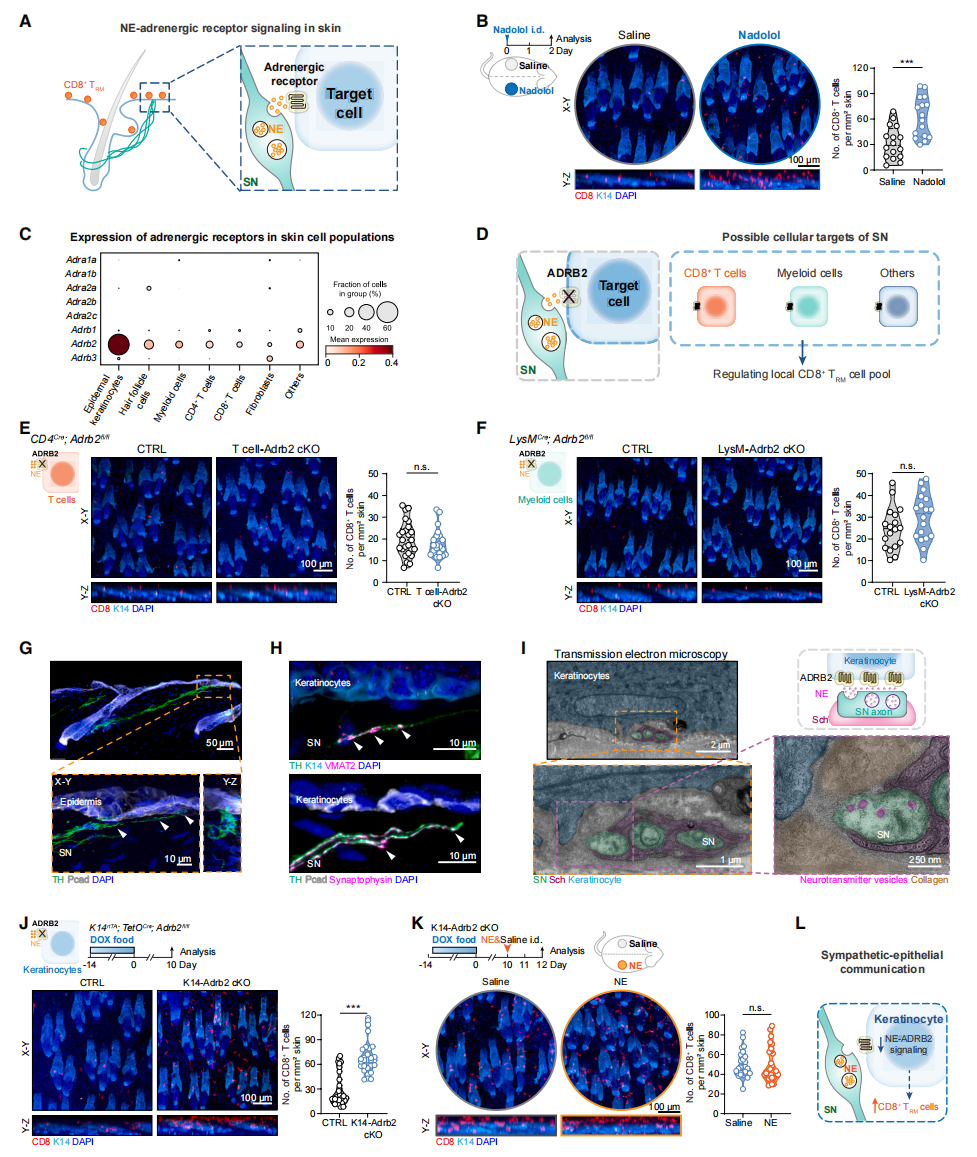
图三 交感神经-上皮通讯调控局部CD8⁺ TRM细胞丰度[8]
接下来,研究者探究皮肤上皮中NE-ADRB2信号如何影响TRM细胞。推测二种可能性,其一,当交感神经张力降低时,诱发已存在的TRM细胞进行原位增殖[12];其二,交感抑制增强了T细胞从循环中招募到皮肤(图四A)。为验证第一种假设,研究者在CNO注射后每6小时腹腔注射5-乙炔基-2'-脱氧尿苷(EdU),标记对照组和Gi-DREADD小鼠的CD8⁺ TRM细胞增殖48小时。然而,EdU⁺ CD8⁺ TRM细胞比例并未发生变化(图四B)。为验证第二种假设,研究者用羧基荧光素琥珀酰亚胺酯(CFSE)标记来自OT-1供体小鼠的活化CD8⁺ T细胞(经卵清蛋白(OVA)加完全弗氏佐剂(CFA)处理),并移植到对照组和Gi-DREADD小鼠。CNO诱导的交感神经抑制显著增加了归巢到皮肤的CFSE⁺ CD8⁺ T细胞数量(图四C)。将OT-1 CD8⁺ T细胞静脉注射至对照组和Gi-DREADD小鼠后,OVA/CFA经皮免疫两组小鼠,随后进行CNO交感抑制。接种后7周,流式分析显示Gi-DREADD小鼠皮肤中的OT-1 CD8⁺ TRM细胞显著增加(图四D),表明在活跃的免疫应答期间短暂阻断皮肤交感信号,能够驱动建立更大且长期的抗原特异性CD8⁺ TRM细胞池。此外,研究者检测交感抑制是否影响中央记忆T细胞(TCM)和效应记忆T细胞(TEM)的招募。将纯化的OT-1 TCM和TEM细胞分别用不同染料标记,并按1:1的比例共同移植到受体小鼠体内。发现交感抑制选择性地增加了TEM细胞向表皮和真皮的招募,而TCM细胞的招募极少且没有变化(图四E)。与进入真皮的细胞相比,进入表皮的招募细胞表现出更高的TRM标志物CD69和CD103的表达(图四F和G)。以上数据表明,抑制交感信号增强了循环TEFF和TEM细胞向皮肤的募集,并促进其在表皮内定位,接收局部信号转化为TRM细胞。
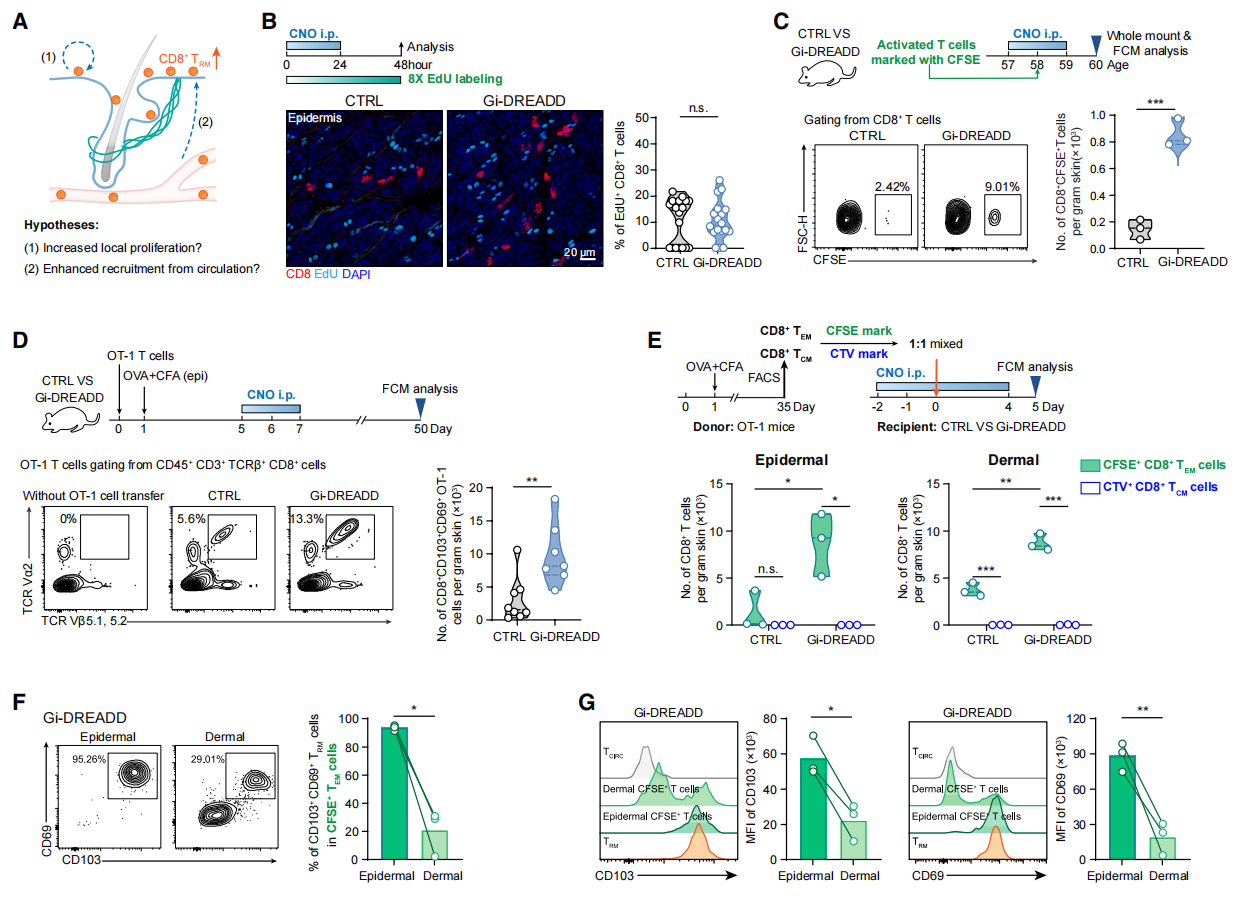
图四 交感神经抑制增强循环T细胞向皮肤的募集[8]
TEFF或TEM细胞通过迁移/归巢受体响应组织特异性趋化因子的招募而进入屏障组织,随后在组织特异性分子信号驱动下成熟。研究者推测,角质形成细胞中ADRB2信号的缺失可能上调了招募循环T细胞的趋化因子。scRNA-seq数据分析显示,皮肤CD8⁺ TRM细胞高表达趋化因子受体CXCR6等多种分子[13](图五A),其配体CXCL16可由上皮细胞产生,并以可溶性和膜结合两种形式存在。一致地,CNO处理后Gi-DREADD小鼠皮肤的角质形成细胞中Cxcl16转录本增加约2倍,而其他趋化因子则下降或保持不变(图五B)。免疫荧光染色证实CXCL16蛋白水平升高(图五C)。细胞间通讯CellChat分析显示,在交感抑制的皮肤中,从表皮角质形成细胞到CD8⁺ TRM细胞的CXCL16-CXCR6信号传导增强(图五D)。CNO处理皮肤中招募的CD8⁺ T细胞常位于CXCL16高表达的角质形成细胞附近(图五E)。此外,被优先招募的TEFF和TEM细胞表达高水平的CXCR6,而未显示招募增加的TCM细胞则缺乏CXCR6(图五F)。为验证CXCL16是否为TRM增加所必需,研究者在经CNO处理的Gi-DREADD小鼠背部皮肤的指定区域皮内注射抗CXCL16阻断抗体或免疫球蛋白G(IgG)同型对照。在IgG处理部位,CNO诱导的交感抑制增加了CD8⁺ TRM细胞;而在CXCL16阻断抗体处理部位,这种增加被抑制(图五G)。随后,研究者构建K14rtTA; TetOCre; Cxcl16fl/fl小鼠特异性敲除了角质形成细胞的Cxcl16,发现交感抑制未能增加皮肤TRM细胞(图五H)。类似地,Cxcr6-/-小鼠在6-OHDA交感神经切除后也未表现出TRM增加(图五I)。研究者还进行了一项竞争性归巢实验,将体外活化的野生型(tdTomato⁺)和CXCR6缺陷型(GFP⁺)CD8⁺ T细胞的混合物共同移植到对照组和Gi-DREADD小鼠中。交感抑制后,tdTomato⁺对照细胞表现出强劲的皮肤归巢能力,而GFP⁺ CXCR6缺陷型T细胞则未能归巢(图五J)。这些数据表明,角质形成细胞来源的CXCL16靶向CXCR6⁺ CD8⁺ T细胞,是交感信号被抑制时增强CD8⁺ TRM细胞招募的主要驱动因素(图五K)。此外,角质形成细胞转录组分析显示,交感抑制显著上调了皮肤上皮TRM发育相关的多个因子,包括TGF-β、E-钙粘蛋白、细胞间粘附分子1(ICAM-1)、IL-7以及几个编码整合素和胶原蛋白的基因(图五L)。研究者检查了鼻粘膜和肺气道,探究交感抑制是否同样影响其他上皮屏障处的CD8⁺ TRM细胞。在鼻腔和气道上皮附近观察到交感神经支配,交感抑制后,上皮CXCL16表达增加,同时CD8⁺ TRM细胞数量相应上升(图五M),表明神经-上皮-免疫轴在多个屏障组织中发挥作用。
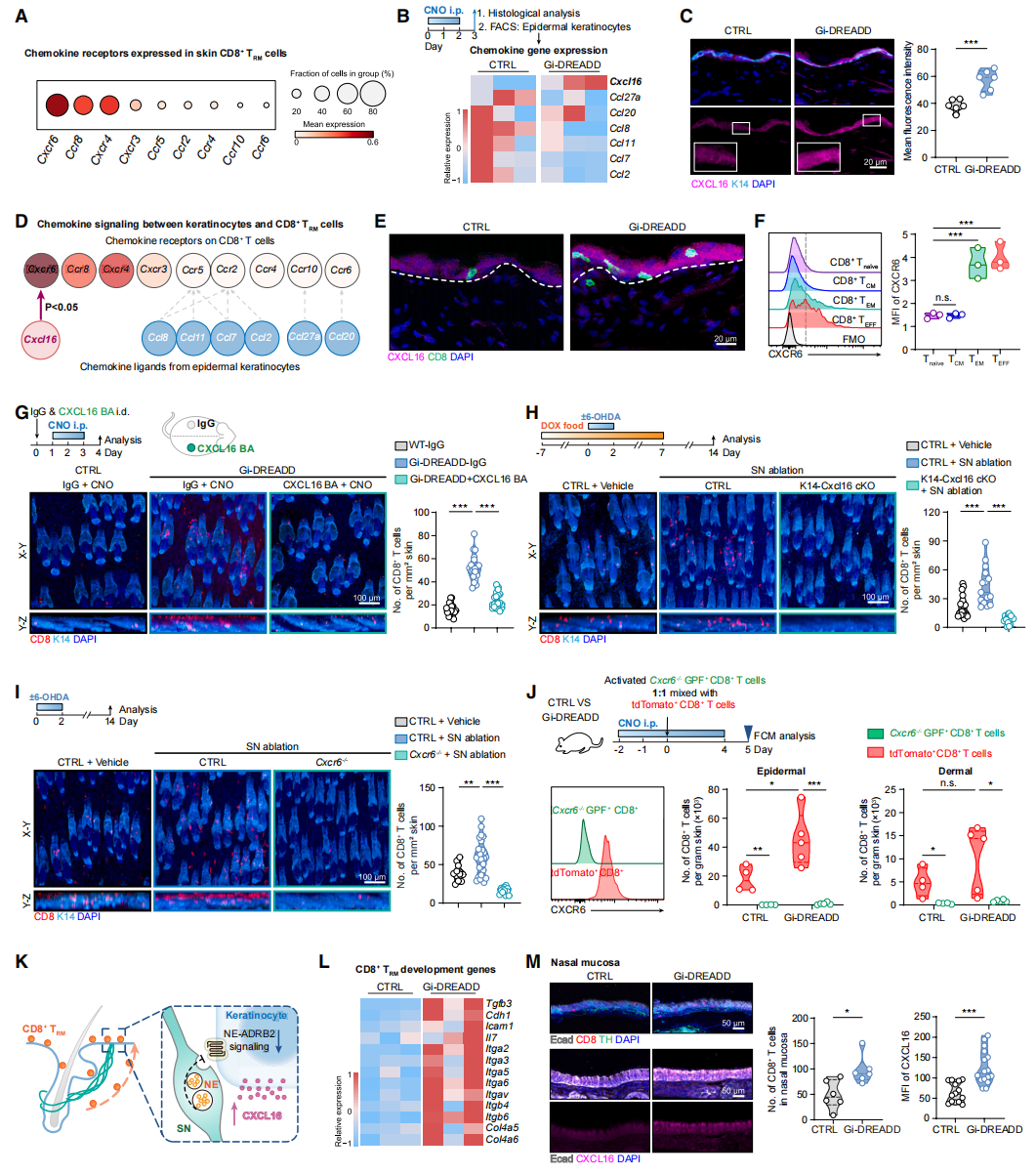
图五 上皮来源CXCL16-CXCR6信号调控CD8+ TRM的形成[8]
基于CD8⁺ TRM细胞在抗肿瘤免疫,尤其是皮肤抗肿瘤免疫中发挥重要作用,研究者推测交感抑制扩大TRM池可能增强上皮对新发癌症的免疫监视。于是,将低剂量的B16黑色素瘤细胞接种到皮肤上皮,局部诱导靶向黑色素瘤细胞的CD69⁺ CD103⁺ CD8⁺ TRM池,后者有助于在皮肤上皮中建立持久的肿瘤-免疫平衡以限制癌症进展,使得一部分小鼠在接种后很长时间内仍无肉眼可见的皮肤病变,即无瘤小鼠(图六A)。接种后6周,相比对照组,交感抑制组的无瘤小鼠百分比增加了一倍(图六B)。这些无瘤小鼠的皮肤中含有丰富的CD8⁺ TRM细胞,与黑色素瘤细胞混杂分布,提示存在持续的免疫监视或细胞毒性活动(图六C)。此外,更高的TRM细胞丰度与上皮中更少的黑色素瘤细胞相关(图六D)。流式证实皮肤中CD69⁺ CD103⁺ CD8⁺ TRM细胞的增加(图六E)。在出现肉眼可见肿瘤的小鼠中,交感抑制组的平均肿瘤体积显著缩小(图六F),生存率从约30%提高到70%(图六G)。使用CXCL16阻断抗体或IgG同型对照重复经皮黑色素瘤接种实验(图六H)。在IgG处理的小鼠中,交感抑制持续增加了无瘤小鼠的比例,减缓了肿瘤生长,并提高了生存率。然而,阻断CXCL16消除了这些效应,导致肿瘤生长更快、肿瘤体积更大(图六H–J),表明交感抑制增强的肿瘤保护作用依赖于CXCL16介导的TRM细胞招募。以上数据表明,升高的CXCL16及其产生的局部CD8⁺ TRM细胞增加对于交感抑制后改善针对皮肤黑色素瘤的免疫监视至关重要。
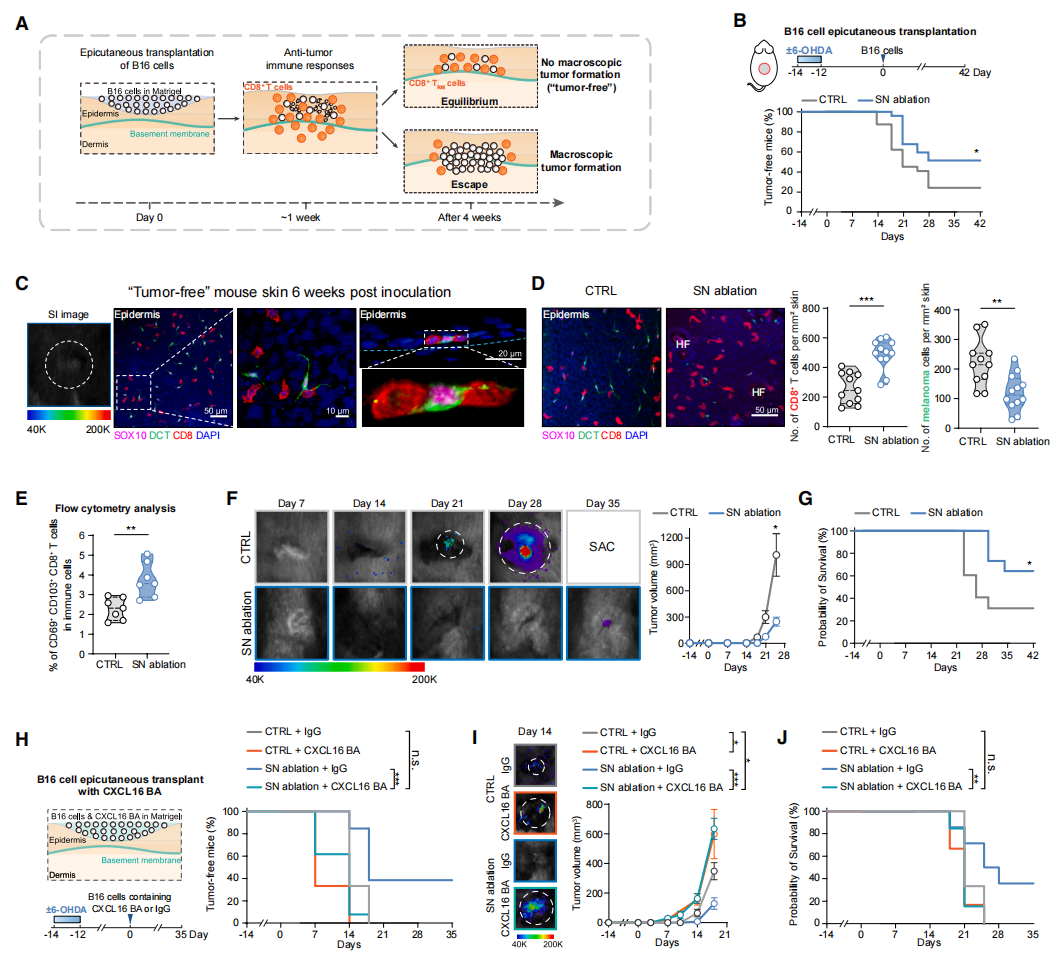
图六 交感神经抑制增强皮肤局部癌症免疫监视[8]
综上所述,该研究揭示了一种“神经-上皮-免疫”轴,上皮组织作为信号中转站。交感神经在表皮基底层附近形成类似突触样结构,通过去甲肾上腺素-ADRB2信号通路动态调控上皮角质形成细胞分泌CXCL16趋化因子,进而选择性招募CXCR6⁺ 效应T细胞进入皮肤,转化为CD8⁺ TRM细胞表型并驻留下来。通过这种间接机制,抑制交感神经可增加皮肤中TRM细胞丰度,进而增强局部免疫监视强度,改善肿瘤控制能力。该研究强调了神经-上皮-免疫轴对维持屏障组织完整与稳态的重要性,揭示了精神压力调控组织局部免疫力的分子机制,以及为TRM细胞相关炎症与自免性疾病提供了潜在干预靶点。

GTP研发中心负责实施基因组标签计划(Genome tagging project, GTP),基于自主知识产权的类精子干细胞介导半克隆技术,为全基因组的功能基因一一贴上标签,致力于构建标签细胞和标签小鼠资源库。类精子干细胞是从精子来源单倍体囊胚中建系获得的一种孤雄单倍体胚胎干细胞,将其注入卵母细胞,能够像精子一样支持整个胚胎发育过程,产生健康的半克隆小鼠。GTP研发中心在类精子干细胞的蛋白质编码基因上原位敲入标签序列,建立了液氮保存的标签细胞资源库。研究需要时,利用半克隆技术将标签细胞注射到小鼠卵母细胞中,一步法获得标签小鼠。

已有标签产品可直接订购,详情查阅以下官网链接。如有需要欢迎联系,我们将竭诚为您服务。
标签细胞网址:
标签小鼠网址:
http://www.sibcb.ac.cn/gtp/msearch.jsp
地址:上海市岳阳路320号
责任编辑:甜点
新媒体运营:suway
参考文献
1. Chu C, Artis D, Chiu IM: Neuro-immune Interactions in the Tissues. Immunity 2020, 52(3):464-474.
2. Wallrapp A, Chiu IM: Neuroimmune Interactions in the Intestine. Annu Rev Immunol 2024, 42(1):489-519.
3. Szabo PA, Miron M, Farber DL: Location, location, location: Tissue resident memory T cells in mice and humans. Sci Immunol 2019, 4(34):eaas9673.
4. Mackay LK, Rahimpour A, Ma JZ, Collins N, Stock AT, Hafon ML, Vega-Ramos J, Lauzurica P, Mueller SN, Stefanovic T et al: The developmental pathway for CD103(+)CD8+ tissue-resident memory T cells of skin. Nat Immunol 2013, 14(12):1294-1301.
5. Adachi T, Kobayashi T, Sugihara E, Yamada T, Ikuta K, Pittaluga S, Saya H, Amagai M, Nagao K: Hair follicle-derived IL-7 and IL-15 mediate skin-resident memory T cell homeostasis and lymphoma. Nat Med 2015, 21(11):1272-1279.
6. Schenkel JM, Fraser KA, Vezys V, Masopust D: Sensing and alarm function of resident memory CD8⁺ T cells. Nat Immunol 2013, 14(5):509-513.
7. Zhu Y, Meerschaert KA, Galvan-Pena S, Bin NR, Yang D, Basu H, Kawamoto R, Shalaby A, Liberles SD, Mathis D et al: A chemogenetic screen reveals that Trpv1-expressing neurons control regulatory T cells in the gut. Science 2024, 385(6708):eadk1679.
8. Zhang P, Miao J, Yu H, Yu H, Liu C, Zhao L, Yang P, Zhou T, Zhang B: Sympathetic-epithelial crosstalk governs tissue-resident memory T cell immunosurveillance in the skin. Cell 2026, 189(5):1323-1340.e25.
9. Zhang B, Ma S, Rachmin I, He M, Baral P, Choi S, Gonçalves WA, Shwartz Y, Fast EM, Su Y et al: Hyperactivation of sympathetic nerves drives depletion of melanocyte stem cells. Nature 2020, 577(7792):676-681.
10. Zhu H, Aryal DK, Olsen RH, Urban DJ, Swearingen A, Forbes S, Roth BL, Hochgeschwender U: Cre-dependent DREADD (Designer Receptors Exclusively Activated by Designer Drugs) mice. Genesis 2016, 54(8):439-446.
11. Karemaker JM: An introduction into autonomic nervous function. Physiol Meas 2017, 38(5):R89-r118.
12. Park SL, Zaid A, Hor JL, Christo SN, Prier JE, Davies B, Alexandre YO, Gregory JL, Russell TA, Gebhardt T et al: Local proliferation maintains a stable pool of tissue-resident memory T cells after antiviral recall responses. Nat Immunol 2018, 19(2):183-191.
13. Heim TA, Ibrahim O, Lin Z, Schultz AC, Steele MM, Mudianto T, Lund AW: CXCR6 promotes dermal CD8(+) T cell survival and transition to long-term tissue residence. J Immunol 2026.215(1):vkaf219.
转载请注明来源于【GTP研发中心】
声明:本文仅用于分享,不代表GTP研发中心立场,若有侵权,请及时联系我们第一时间更正!



