技术分享:绘制小鼠器官及全身3D细胞图谱,助力开启三维细胞组学时代
细胞是构成所有生命体的基本单位。解析完整器官及全身的三维细胞架构,能够加深人们对发育、生理和疾病的理解。近期三维病理学研究表明,传统的二维组织学仅能捕捉到部分结构异质性,常会遗漏罕见的疾病相关细胞[1]。随着各种组学技术的发展,拓宽了人们对细胞异质性的认识,但每种方法因其检测方法都存在一定的局限性。单细胞测序技术基于高灵敏度能揭示细胞多样性,但分析对象为解离的单细胞,故缺乏细胞的空间背景信息。空间转录组学的发展弥补了这一不足,但多数方法仍基于二维层面,且在分辨率与分子覆盖度方面难以两全。相比之下,基于成像的三维组织学技术则为全面收集空间信息提供了另一条途径[2]。细胞组学技术通过综合分析多细胞系统中的全部细胞群体,利用空间背景信息来展现细胞组织的全面视图[3]。该方法能够在成像所有细胞的同时保留其空间关系,从而基于固有的空间信息进行聚类分析。
组织透明化技术结合光片荧光显微镜(LSFM),推动了全器官乃至全身的三维组织学与细胞组学研究[4]。目前已有数十种现代组织透明化方案问世,其中部分因卓越的透明化效率脱颖而出,特别适用于结合LSFM进行器官/全身三维成像,包括BABB、3DISCO、CUBIC、MACS、CLARITY,以及SHIELD。与透明化技术并进的是,针对透明化样本的LSFM成像系统也取得了同步发展,如tiling LSFM,ASLM和ExA-SPIM。为开展全细胞组分析,建立一套用于比较、聚类及生物学解读的标准化计算流程至关重要。一个典型的例子是全脑c-Fos映射,流程涉及将检测到的细胞坐标和强度映射到脑图谱上,从而实现对特定脑区的定量分析。然而,广泛使用的体积图谱如艾伦脑图谱[5],缺乏单细胞分辨率且依赖于预定义的解剖边界。因此,亟需能以单细胞分辨率分析全器官乃至全身的高度灵敏技术,来建立针对器官及全身的单细胞分辨率图谱。
2026年3月,Cell 期刊报道了一项研究,通过优化了组织透明化方案,并开发exMOVIE成像系统,构建了一套针对成年小鼠十一种器官和新生鼠全身的单细胞分辨率三维参考图谱(CUBIC器官/全身图谱)。该图谱提供了各器官内所有细胞的三维空间坐标,助力于单细胞分辨率水平上的多个样本的定量细胞组学对比分析,可应用于器官发育研究、疾病状态分析以及通过三维免疫染色进行全身免疫细胞图谱绘制等。该研究建立了一套通用的细胞组学工作流程,增进了生理、发育和病理过程中对生物体的系统层面理解[6]。
研究者此前开发了基于坐标的小鼠大脑单细胞图谱——CUBIC脑图谱,采用的是ScaleCUBIC-1去脂、CUBIC-X透明化,其中安替比林的引入实现了脑组织膨胀与高折射率的双重效果[7]。然而,许多器官所需的折射率约为1.50-1.55,CUBIC-X的最终折射率为1.467,不足以实现全器官的充分透明。为解决此问题,后续开发了去脂效率更高的CUBIC-L,以及能在保持CUBIC-X膨胀特性的同时实现目标折射率1.52的CUBIC-R+[8]。为了构建器官/全身图谱,研究者采用了基于CUBIC-L/R+的透明化方案,并针对每个器官及全身样本优化了透明化工作流程(图一A和C)。由此,成功实现成年小鼠甲状腺、唾液腺、心脏、肺、肝脏、胰腺、肾脏、膀胱、附睾、睾丸和子宫,以及新生小鼠全身的充分透明化(图一B和D)。
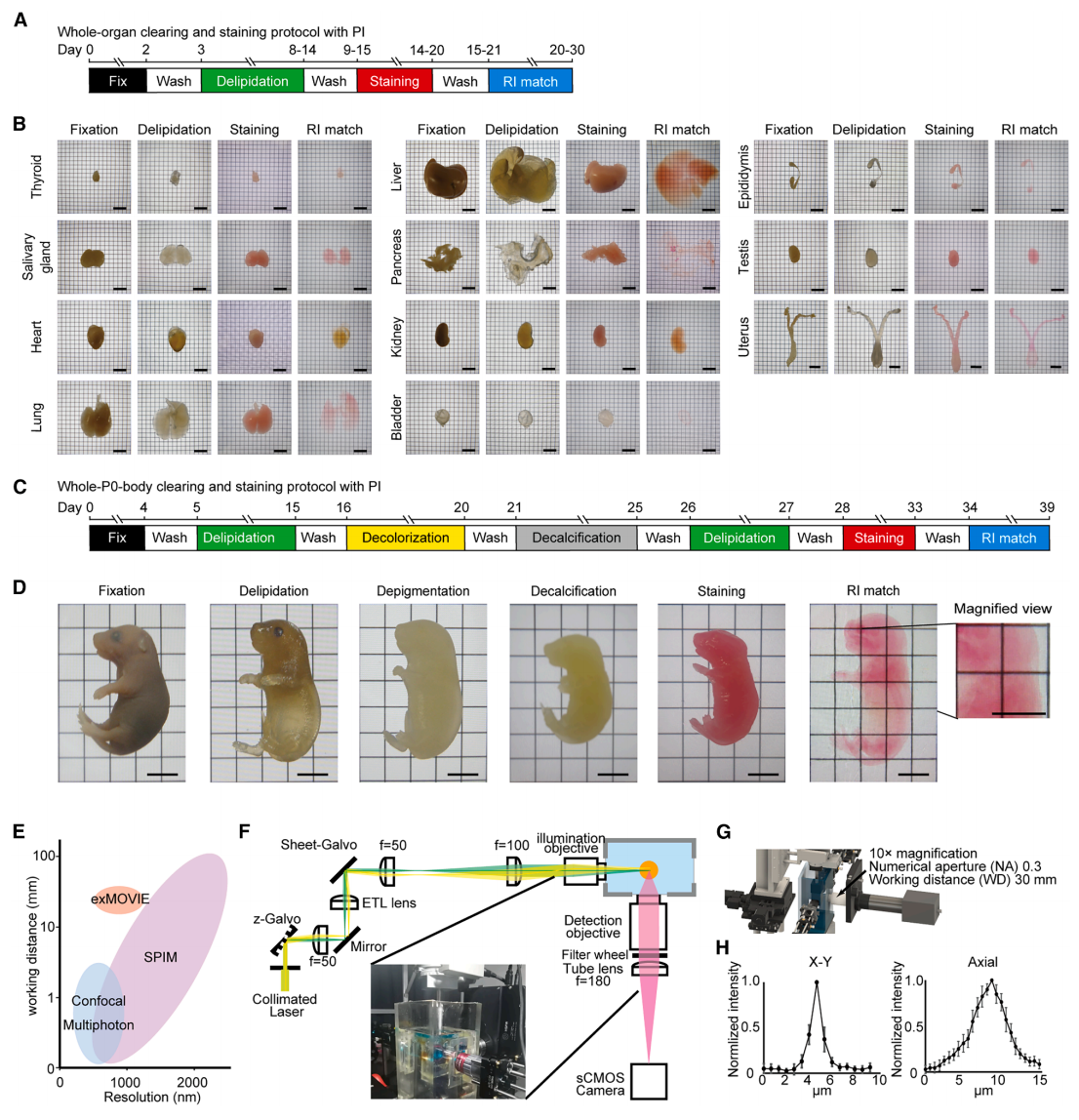
图一 11个器官及新生鼠全身组织透明化流程优化和exMOVIE系统研发[6]
具体而言,所有器官均采用CUBIC-L进行脱脂处理,使用碘化丙啶(PI)进行细胞核染色,并用CUBIC-R+进行折射率匹配(图一A和B)。CUBIC-L由10 wt% N-丁基二乙醇胺和10 wt% Triton X-100溶于蒸馏水配制而成。CUBIC-R+则由45 wt%安替比林、30 wt%烟酰胺和0.1%(体积比)N-丁基二乙醇胺溶于蒸馏水配制而成。使用数字折射仪将CUBIC-R+的折射率调整为1.522。CUBIC-L和CUBIC-R+均可从CUBICStars公司购买。在每个步骤之间,器官用PBS洗涤三次。每一步均在37°C下进行,并对各器官的处理时间进行优化。脱脂时,第一天使用蒸馏水稀释至50%的CUBIC-L进行处理。除肝脏使用20 mL外,其余器官的CUBIC-L用量均为10 mL。用于细胞核染色的PI终浓度为30 μg/ml。折射率匹配时,除肝脏外,所有器官第一天均使用50%稀释的CUBIC-R+进行处理。肝脏的折射率匹配则按以下流程进行:20% CUBIC-R+处理2天,40% CUBIC-R+处理2天,60% CUBIC-R+处理2天,80% CUBIC-R+处理2天,100% CUBIC-R+处理3天。除肝脏使用20 mL外,其余器官的CUBIC-R+用量均为10 mL。
新生小鼠的处理流程包括:使用CUBIC-L进行脱脂、过氧化氢进行脱色素、CUBIC-B进行脱钙[8]、PI进行细胞核染色或免疫染色,以及CUBIC-R+进行折射率匹配(图一C和D)。脱脂步骤在37°C下进行10天,每样本使用10 mL CUBIC-L,其中前两天使用水稀释至50%的CUBIC-L。脱色素步骤在25°C下进行4天,每样本使用10 mL 3%过氧化氢溶液。脱钙步骤在37°C下进行4天,每样本使用10 mL CUBIC-B。细胞核染色在37°C下进行5天,每样本使用700 μg PI,终浓度为175 μg/mL。对于计划进行免疫染色的样本,细胞核染色使用BOBO™-1 Iodide,每样本8 μL。免疫染色遵循CUBIC-HV方案[9]进行。折射率匹配在37°C下进行5天,每样本使用10 mL 用水稀释至50%的CUBIC-R+。
全器官及全身成像面临的一大挑战,是缺乏能够对厚度超过20 mm的样本进行快速细胞分辨率成像的显微镜。此类成像所需的物镜需具备以下特性:足以观察肝脏等厚器官的长工作距离、能清晰分辨细胞核的足够轴向分辨率,以及能够处理TB级数据量的高速采集能力(图一E)。为攻克这些难题,研究者研发了一款名为exMOVIE的光片荧光显微镜。该系统集长工作距离、高分辨率与快速成像于一身,专为大型器官和全身样本的单细胞水平成像而设计(图一F)。exMOVIE采用10倍放大倍数、数值孔径0.3、工作距离30 mm的物镜(图一G)。其高速成像能力得益于每秒50帧的sCMOS相机与MOVIE自动对焦系统的结合。此外,通过整合ASLM的技术元素,系统轴向分辨率得到提升。这一集成使得在实时自动对焦下,三维成像速度最高可达33帧每秒,同时在整个视野内保持约1 μm(x-y轴)和5 μm(轴向)的半高宽分辨率(图一H)。exMOVIE系统实现了体素分辨率为0.65×0.65×2.5 μm的完整器官及全身成像,使得在可行的时间范围内对完整器官进行全面的单细胞分辨率成像成为现实。
通过图形处理器(GPU)从细胞核染色图像中提取细胞坐标,各器官均实现了高检测精度。由于高倍率光片荧光显微镜的视野有限,每个器官均需从两侧采集重叠的x-y方向拼图块。为处理这些庞大数据集并校正几何畸变如载物台偏移、俯仰、偏转,研究者开发了一套针对大体积三维数据优化的拼接与配准流程,成功实现每个器官完整三维点云的精确重建(图二A-K)。最终构建的CUBIC器官图谱提供了每个器官内所有细胞的三维空间坐标参考。各器官细胞数量从甲状腺的1.02×10⁶ ± 1.42×10⁴ 个到肝脏的2.94×10⁸ ± 1.64×10⁶ 个不等(图二L)。
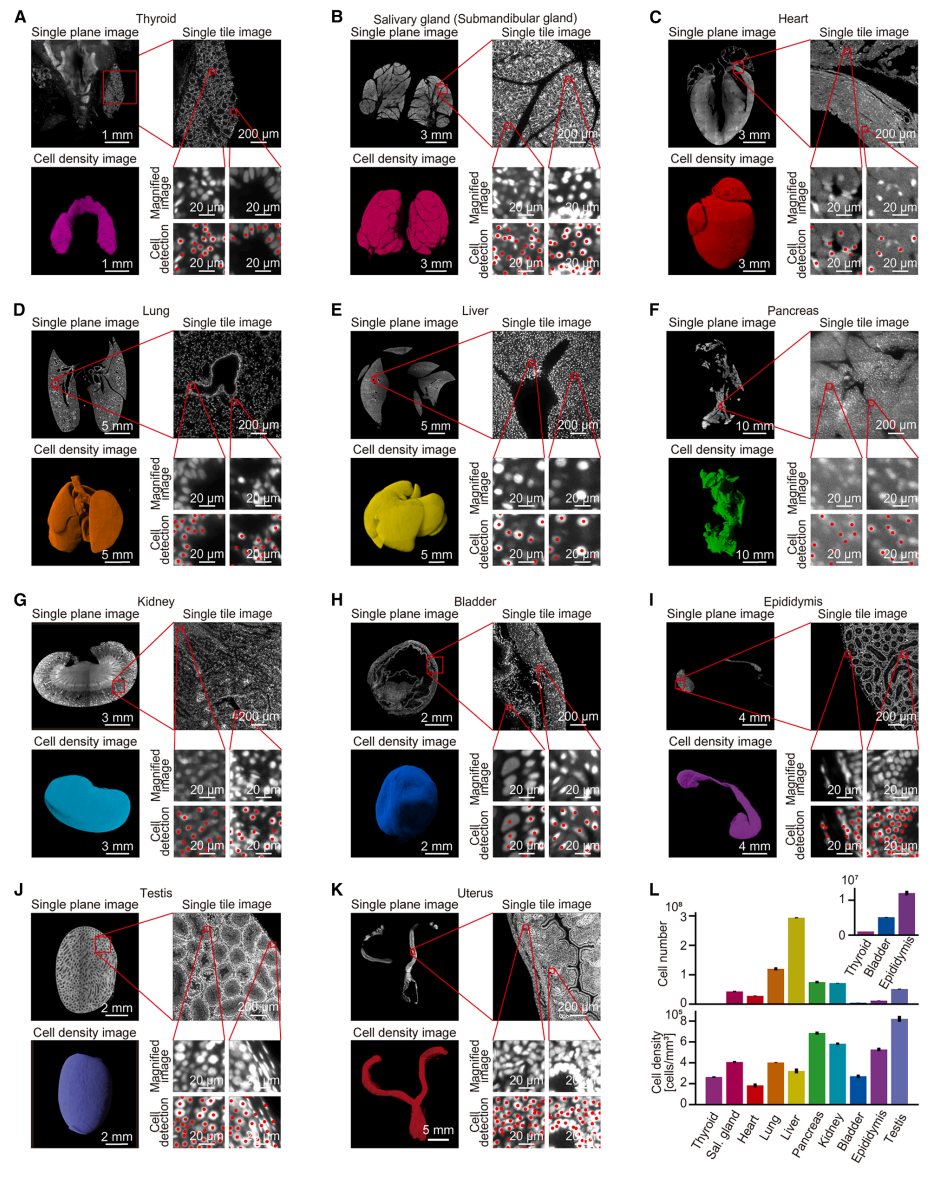
图二 小鼠全器官单细胞成像与细胞检测[6]
研究者在CUBIC器官图谱中对心脏、肺、肝脏和肾脏进行解剖结构分区(图三A)。与基于艾伦脑图谱三维分割数据构建CUBIC脑图谱的情况不同[7],这些器官并无现成的三维分区数据可用,不得不从头创建这些数据集。首先根据三维细胞密度分布定义各区域边界,然后将这些边界重建为分割的体积数据。随后,图谱中检测到的每个细胞核都会根据其所在位置被标记上对应的区域信息,从而支持全器官范围内的空间分析。运用此方法,将心脏划分为四个心腔,肺划分为五个肺叶,肝脏划分为六个肝叶,肾脏划分为三个主要区域。遵循同样的工作流程,还为雌性器官构建了相应的分区图谱(图三B和C)。利用已进行区域注释的CUBIC器官图谱,展示了多样本比较分析的应用(图三D)。每个器官都创建了基于雄性(n=3)和雌性(n=3)样本的模板。值得注意的是,肝脏在形态上表现出显著的性别差异,因此需要分别为雄性和雌性创建单独的模板。所有模板均已公开共享https://whole.cfosdb.systems-based-medicine.org/whole_body/ ,以支持更广泛的配准工作流程应用。随后,对各解剖区域的细胞数量进行定量分析(图三E)。这些分析清晰地揭示了每个器官内部的多细胞组织结构及其结构与功能的关系。在肺部,利用3D Slicer软件对支气管和动脉进行分割,并量化了各区域的细胞数量(图三F和G)。
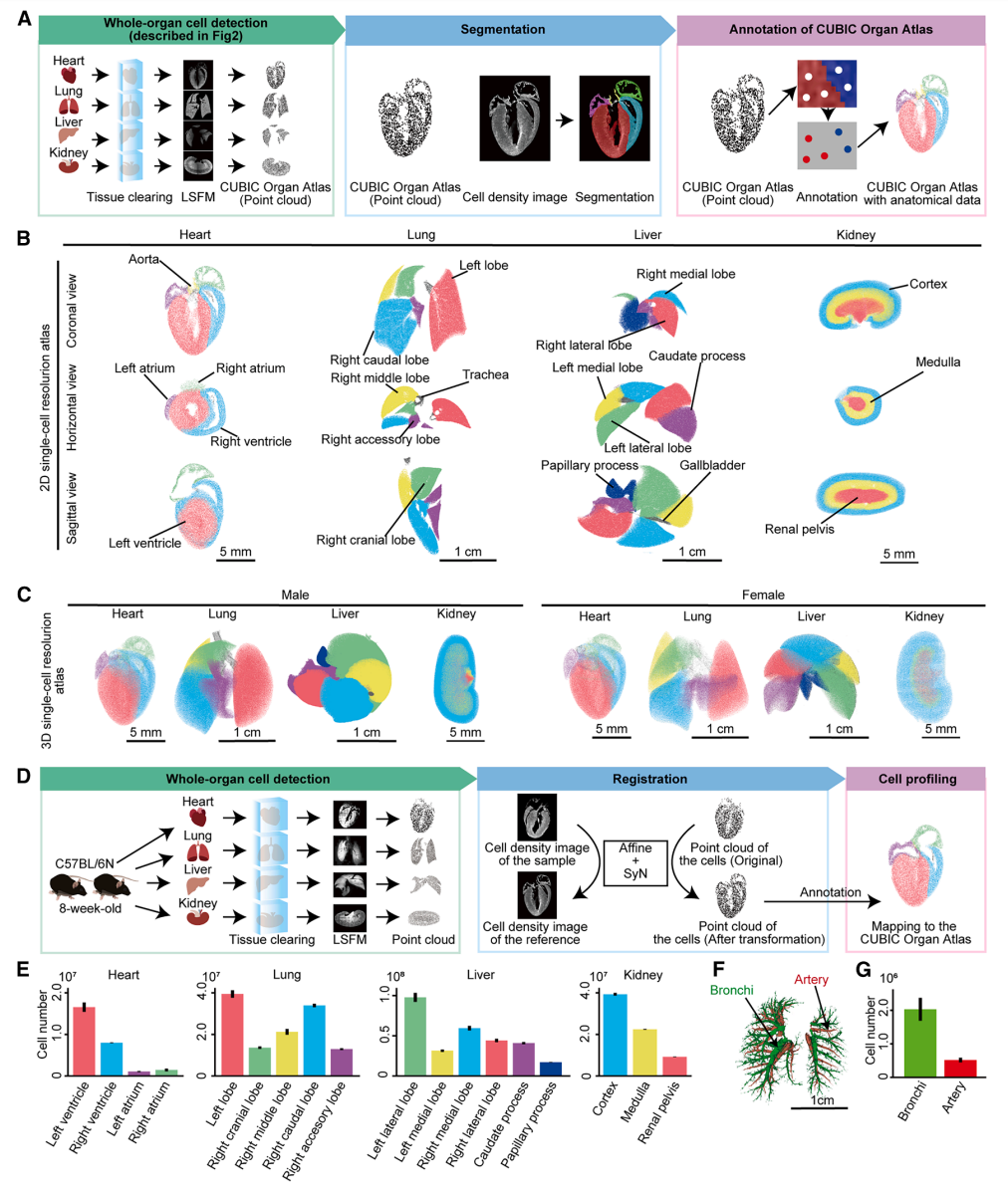
图三 构建用于比对分析的注释CUBIC器官图谱[6]
此外,研究者展示了CUBIC器官图谱在发育生物学中的应用,进行小鼠肾脏不同发育阶段的全器官单细胞分析,揭示了发育过程中细胞数量的动态变化。还展示CUBIC器官图谱在病理学研究中的应用价值,对药物诱导的肾损伤和肺损伤进行全器官单细胞分析,揭示了局部细胞密度变化的病理区域。CUBIC器官图谱也适用于常规实验场景,如将样本信号映射至CUBIC器官图谱并进行融合以确认是否成功建立肺转移模型等,表明能够广泛应用于各类用户驱动研究。
为构建CUBIC全身图谱,研究者对经过透明化处理和细胞核染色的C57BL/6N新生鼠进行成像(图一C和D)。得益于exMOVIE系统的高速成像能力,在72小时内采集了20 TB的全身数据,获得了足以进行全身细胞计数的图像(图四A和B)。对骨骼、皮肤、眼睛、胸腺、肺、心脏、肝脏、脾脏、大脑、脊髓、肠道、肾脏和膀胱等结构进行分割,并将检测到的每一个细胞核都归属到对应的区域(图四C和D)。完成区域标注后,即可从图谱中数字化提取出各个单独的器官(图四E)。
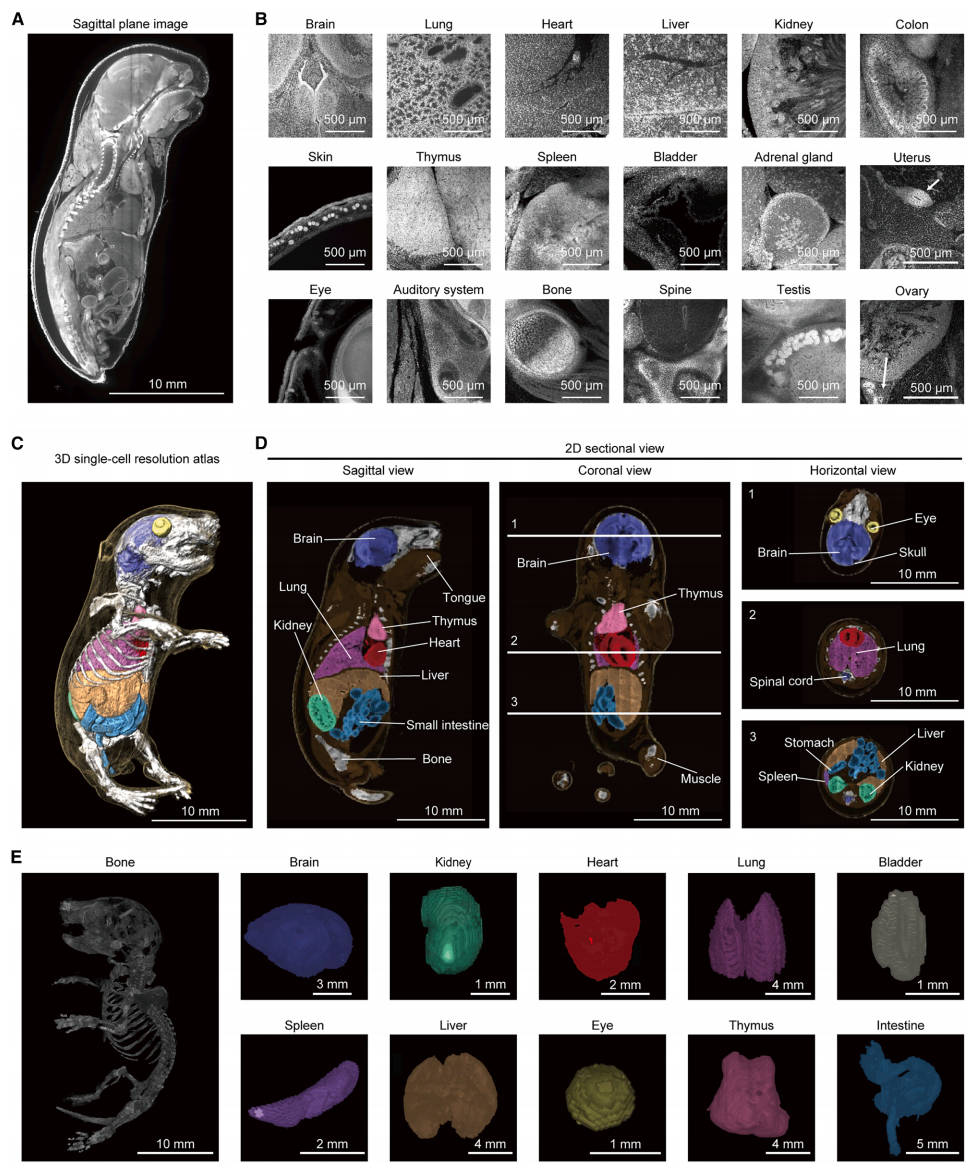
图四 新生小鼠全身单细胞分辨率图谱的构建[6]
最后,研究者在全身范围内开展细胞组学分析(图五A)。作为初步应用,量化每个注释解剖区域的总细胞数和细胞密度(图五B和C)。随后,利用全身免疫染色技术对特定细胞类型进行分析。重点研究巨噬细胞,这类细胞在早期免疫应答、组织修复和稳态维持中至关重要[10],但其全身总数和整体分布情况尚不明确。使用标记巨噬细胞、树突状细胞和单核细胞的抗IBA1抗体进行全身免疫染色,检测IBA1阳性细胞并提取其坐标信息(图五D)。同时采集的细胞核染色图像被配准到CUBIC全身参考图谱,并将所得的变换矩阵应用于IBA1阳性细胞的坐标,从而实现其分布的全身绘图(图五E和F)。量化各个注释器官中IBA1阳性细胞的数量和密度,细胞数量范围从膀胱的1.30×10³ ± 5.62×10² 个到骨骼的1.99×10⁵ ± 2.81×10⁴ 个不等(图五G)。然后,计算每个器官内IBA1阳性细胞的最近距离,并将分布情况以直方图形式可视化(图五H和I)。在大脑中,IBA1阳性细胞表现出狭窄的距离分布和较小的细胞间距,这与小胶质细胞均匀且密集分布的已知特征一致[11]。相比之下,肺部的距离分布则更宽,这也与肺内同时存在高密度和低密度巨噬细胞群体的报道相符[12]。这些结果表明,IBA1阳性细胞的分布模式与器官结构之间存在密切关系,揭示了不同器官免疫细胞空间组织模式差异。此外,还对酪氨酸羟化酶阳性细胞和α-SMA阳性细胞的全身三维分布进行分析,进一步证明了CUBIC全身图谱在神经元和血管图谱绘制方面的适用性(图五J和K)。
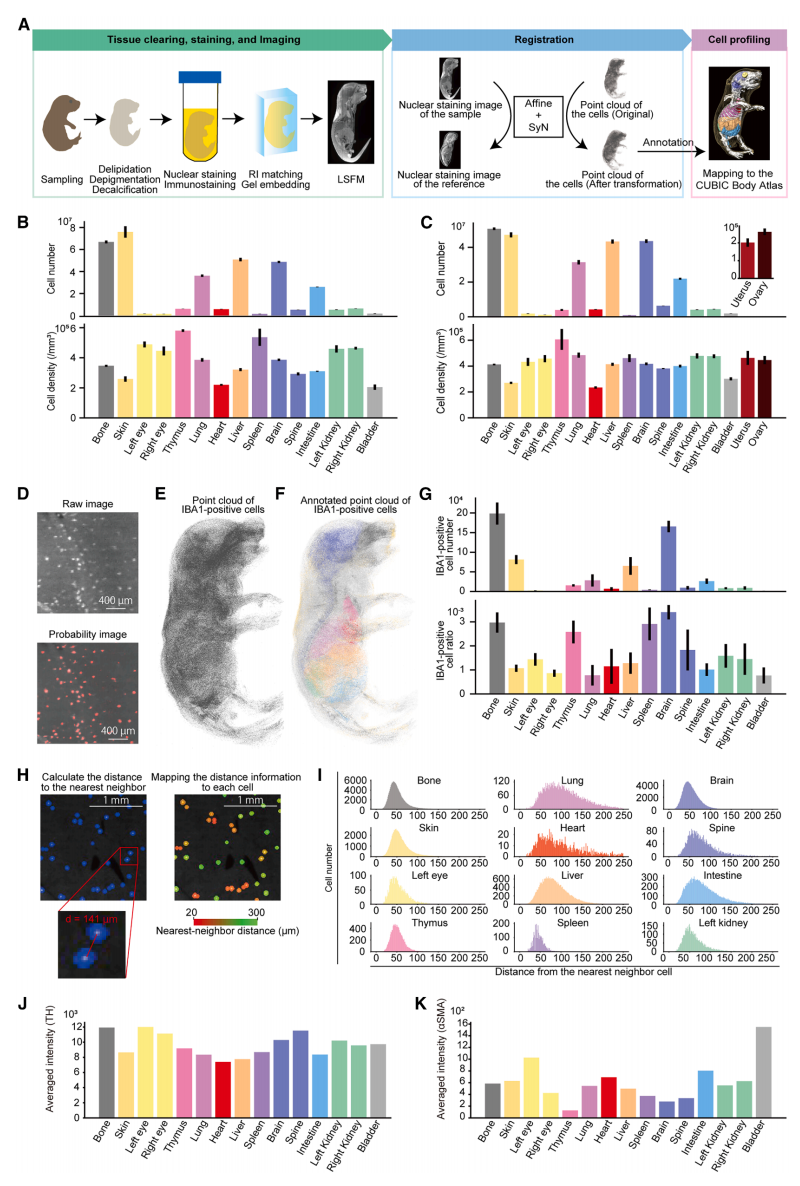
图五 CUBIC全身图谱实现全身细胞分析[6]
综上所述,该研究利用优化的组织透明化方案和具备足够工作距离与轴向分辨率的exMOVIE成像系统,实现了小鼠器官/全身范围的三维细胞成像,并使用针对大体积三维数据优化的拼接与配准流程,成功构建小鼠的器官/全身范围单细胞分辨率的三维细胞参考图谱(CUBIC器官/全身图谱)。作为面向科学界的共享资源,与其他组学平台一样,这一细胞组学资源可支持用户根据自身需求开展研究。CUBIC器官/全身图谱主要以三维点云形式呈现,包含细胞的空间坐标及基础的解剖区域信息。随着更多三维空间转录组数据的出现,该图谱有望成为整合转录组信息、解剖结构和细胞类型信息的基础结构框架,助力细胞组学和空间转录组学的融合发展,助力开启三维细胞组学时代。

GTP研发中心负责实施基因组标签计划(Genome tagging project, GTP),基于自主知识产权的类精子干细胞介导半克隆技术,为全基因组的功能基因一一贴上标签,致力于构建标签细胞和标签小鼠资源库。类精子干细胞是从精子来源单倍体囊胚中建系获得的一种孤雄单倍体胚胎干细胞,将其注入卵母细胞,能够像精子一样支持整个胚胎发育过程,产生健康的半克隆小鼠。GTP研发中心在类精子干细胞的蛋白质编码基因上原位敲入标签序列,建立了液氮保存的标签细胞资源库。研究需要时,利用半克隆技术将标签细胞注射到小鼠卵母细胞中,一步法获得标签小鼠。

已有标签产品可直接订购,详情查阅以下官网链接。如有需要欢迎联系,我们将竭诚为您服务。
标签细胞网址:
标签小鼠网址:
http://www.sibcb.ac.cn/gtp/msearch.jsp
地址:上海市岳阳路320号
责任编辑:多一百
新媒体运营:suway
参考文献
1. Nojima S, Susaki EA, Yoshida K, Takemoto H, Tsujimura N, Iijima S, Takachi K, Nakahara Y, Tahara S, Ohshima K et al: CUBIC pathology: three-dimensional imaging for pathological diagnosis. Sci Rep 2017, 7(1):9269.
2. Ertürk A: Deep 3D histology powered by tissue clearing, omics and AI. Nature methods 2024, 21(7):1153-1165.
3. Mitani TT, Susaki EA, Matsumoto K, Ueda HR: Realization of cellomics to dive into the whole-body or whole-organ cell cloud. Nature methods 2024, 21(7):1138-1142.
4. Yang B, Treweek JB, Kulkarni RP, Deverman BE, Chen CK, Lubeck E, Shah S, Cai L, Gradinaru V: Single-cell phenotyping within transparent intact tissue through whole-body clearing. Cell 2014, 158(4):945-958.
5. Wang Q, Ding SL, Li Y, Royall J, Feng D, Lesnar P, Graddis N, Naeemi M, Facer B, Ho A et al: The Allen Mouse Brain Common Coordinate Framework: A 3D Reference Atlas. Cell 2020, 181(4):936-953.e920.
6. Yoshida SY, Matsumoto K, Takagi S, Kinoshita FL, Yamashita K, Shigeta D, Yoshioka Y, Ushiku T, Morii E, Susaki EA et al: Whole-organ and whole-body 3D atlases enable cellome-wide profiling. Cell 2026.189(6):1836-1853.e19.
7. Murakami TC, Mano T, Saikawa S, Horiguchi SA, Shigeta D, Baba K, Sekiya H, Shimizu Y, Tanaka KF, Kiyonari H et al: A three-dimensional single-cell-resolution whole-brain atlas using CUBIC-X expansion microscopy and tissue clearing. Nature neuroscience 2018, 21(4):625-637.
8. Tainaka K, Murakami TC, Susaki EA, Shimizu C, Saito R, Takahashi K, Hayashi-Takagi A, Sekiya H, Arima Y, Nojima S et al: Chemical Landscape for Tissue Clearing Based on Hydrophilic Reagents. Cell Rep 2018, 24(8):2196-2210.e2199.
9. Susaki EA, Shimizu C, Kuno A, Tainaka K, Li X, Nishi K, Morishima K, Ono H, Ode KL, Saeki Y et al: Versatile whole-organ/body staining and imaging based on electrolyte-gel properties of biological tissues. Nature communications 2020, 11(1):1982.
10. Mass E, Nimmerjahn F, Kierdorf K, Schlitzer A: Tissue-specific macrophages: how they develop and choreograph tissue biology. Nature reviews Immunology 2023, 23(9):563-579.
11. Dos Santos SE, Medeiros M, Porfirio J, Tavares W, Pessôa L, Grinberg L, Leite REP, Ferretti-Rebustini REL, Suemoto CK, Filho WJ et al: Similar Microglial Cell Densities across Brain Structures and Mammalian Species: Implications for Brain Tissue Function. J Neurosci 2020, 40(24):4622-4643.
12. Balestrieri B, Granata F, Loffredo S, Petraroli A, Scalia G, Morabito P, Cardamone C, Varricchi G, Triggiani M: Phenotypic and Functional Heterogeneity of Low-Density and High-Density Human Lung Macrophages. Biomedicines 2021, 9(5):505.
转载请注明来源于【GTP研发中心】
声明:本文仅用于分享,不代表GTP研发中心立场,若有侵权,请及时联系我们第一时间更正!



