技术分享:跨膜蛋白SIGLEC12介导坏死性凋亡MLKL下游的质膜破裂
坏死性凋亡是一种裂解性细胞死亡形式,常在感染和炎症性疾病中被过度激活[1]。坏死性凋亡由一系列信号级联反应所介导,致使假激酶MLKL发生寡聚化,在细胞膜上形成孔状结构使水分内流,最后引发质膜破裂(PMR)。质膜破裂是所有裂解性细胞死亡形式的终末共同特征。研究发现跨膜蛋白NINJ1是在细胞焦亡、毒素诱导性坏死、凋亡和铁死亡过程中,介导质膜破裂的关键效应蛋白[2, 3],但NINJ1在MLKL下游坏死性凋亡的质膜破裂过程中并非必需。然而,尚不清楚何种介质介导了坏死性凋亡中的质膜破裂,以及对MLKL下游分子事件机制的理解也不完整。
2026年1月,Nature期刊报道了一项研究,通过CRISPR-Cas9全基因组敲除筛选,发现人源SIGLEC12是MLKL下游介导坏死性凋亡发生质膜破裂(PMR)的核心因子。敲降或敲除SIGLEC12的细胞在坏死性凋亡诱导的质膜破裂过程中存在缺陷,呈现出“泡状膨胀”形态。SIGLEC12被TMPRSS4切割是诱导坏死性凋亡质膜破裂的必要且充分条件,且癌症相关SIGLEC12变异体Ser458Phe减弱了TMPRSS4的切割作用。小鼠细胞敲除Siglec12并不影响质膜破裂,提示该机制具有物种特异性。该研究填补了坏死性凋亡执行步骤的关键一环,并为治疗这种促炎性细胞死亡相关人类疾病提供了新的途径[4]。
为探究MLKL下游执行坏死性凋亡的分子机制,研究者在HEK293细胞中利用强力霉素诱导表达系统(FlpIn-Trex)来诱导表达组成型活化形式的MLKL(MLKLQ356A)[5],在此基础上进行全基因组CRISPR-Cas9敲除文库筛选(图一a)。结果发现敲除SIGLEC12基因后,能够保护细胞免受MLKLQ356A表达引起的细胞死亡(图一b和c)。SIGLEC12是一种一次跨膜蛋白,是SIGLEC家族免疫球蛋白样凝集素成员之一。该家族蛋白主要在免疫细胞表达,通过识别含唾液酸的聚糖在免疫应答调控中发挥关键作用[6]。SIGLEC12的胞外区包含两个V型唾液酸结合免疫球蛋白结构域和两个C2型免疫球蛋白结构域,胞内区则具有一个基于免疫受体酪氨酸的抑制基序(ITIM)和一个基于免疫受体酪氨酸的转换基序(ITSM,图一d)。SIGLEC12与NINJ1之间存在显著的氨基酸相似性,例如共有的NISI基序(图一d红色区域),提示二者可能存在功能同源性。与其他SIGLEC家族成员不同,人类SIGLEC12因其V型免疫球蛋白结构域发生多处突变而丧失了唾液酸结合能力。SIGLEC12在胃肠道、上皮细胞、巨噬细胞以及某些癌症中均有表达,并可能参与肿瘤进展过程。基于该人源蛋白体内无法结合唾液酸的特性,提示其可能在人类特有的生理稳态维持中发挥物种特异性作用。
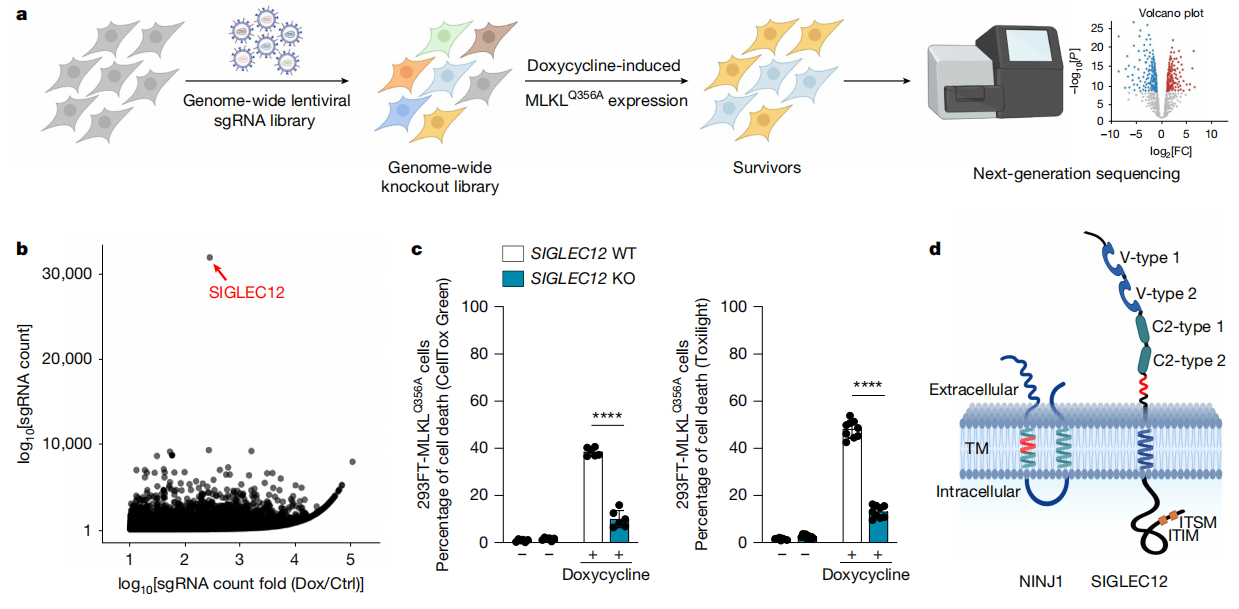
图一 SIGLEC12是坏死性凋亡的介导因子[4]
与筛选结果一致,敲除或敲降SIGLEC12能够保护细胞免受以下三种方式诱导的坏死性凋亡:1)组成型激活的MLKLQ356A表达;2)坏死性凋亡诱导组合TSE(TNF、SM-164、emricasan);3)坏死性凋亡诱导组合TRAIL+SE(TRAIL、SM-164、emricasan)(图二a-d)。值得注意的是,SIGLEC12缺失可保护细胞免于CellToxGreen染色阳性,后者是一种仅在质膜破裂时染色的DNA结合荧光染料(图二a,c,d和e左),并减少乳酸脱氢酶(LDH)释放(图二b),但通过CellTiter-Glo检测ATP水平下降显示其不能阻止细胞死亡(图二a和d),表明SIGLEC12的作用可能主要涉及介导质膜破裂。根据自磷酸化标志物及MLKL寡聚化判断,SIGLEC12缺失并未改变坏死性凋亡关键介质RIPK1、RIPK3和MLKL的激活状态(图二d)。SIGLEC12缺陷细胞在坏死性凋亡过程中无法破裂质膜,导致在光学与电子显微镜下观察到“泡状膨胀”表型(图二e右和f),破裂质膜缺陷导致胞质蛋白和HMGB1的释放减少(图二g),以及促炎细胞因子IL-1β、IL-8、CXCL1和TNF的产生减少。此外,将SIGLEC12 NISI基序中的ISLS残基突变为AAAA,即可完全阻断破裂质膜,提示该基序为核心结构。以上数据表明,SIGLEC12处于坏死性凋亡MLKL的下游。
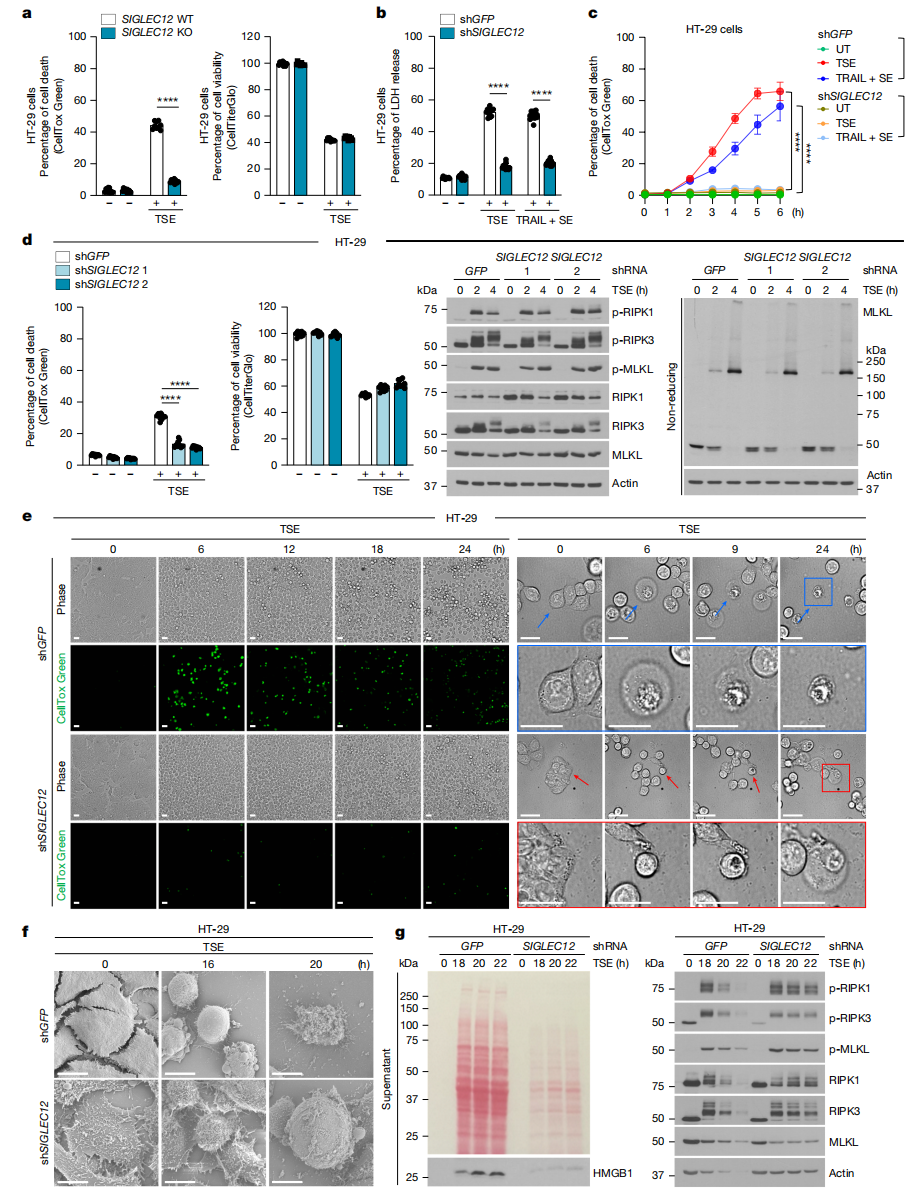
图二 SIGLEC12处于坏死性凋亡MLKL的下游[4]
鉴于NINJ1在多种细胞死亡场景中介导质膜破裂的重要性,但在坏死性凋亡过程中却非必需,研究者测试SIGLEC12是否在坏死性凋亡以外的细胞死亡场景中也能发挥作用。在多种测试条件下,SIGLEC12在外源性凋亡(TNF+SM-164)、内源性凋亡(依托泊苷)、细胞焦亡(α-酮戊二酸、LPS+黑藻素)以及铁死亡(erastin)过程中的质膜破裂均非必需(图三a-b)。与NINJ1在细胞焦亡过程中的表现相似,SIGLEC12在坏死性凋亡期间形成点状结构并转位至质膜(图三c)。值得注意的是,SIGLEC12在人类结肠癌活检组织中也形成点状结构,但在正常结肠组织中未见此现象(图三d)。电子显微镜观察显示,SIGLEC12在坏死性凋亡过程中形成纤维束结构(图三e),这种组装特征近期被证实是NINJ1诱导质膜破裂的关键机制[7]。与其在MLKL下游介导坏死性凋亡的作用相符,SIGLEC12在坏死性凋亡期间与MLKL发生相互作用,且这种相互作用可被MLKL抑制剂坏死磺胺(NSA)阻断,该抑制剂能阻止MLKL与质膜的结合[8];而与RIPK1或RIPK3无直接结合(图三f-h)。基于质谱的磷酸化位点图谱分析显示,在坏死性凋亡过程中,SIGLEC12的Thr519、Ser532、Ser539和Thr555位点发生去磷酸化(图三i),但该事件尚不足以激活SIGLEC12诱导质膜破裂的功能。以上数据表明,SIGLEC12在坏死性凋亡过程中受到调控。需要特别指出的是,在Siglec12敲除的小鼠细胞系中,坏死性凋亡过程中的质膜破裂并未受到抑制,表明SIGLEC12在MLKL下游促进质膜破裂的活性可能具有物种特异性,甚至可能仅限于人类。
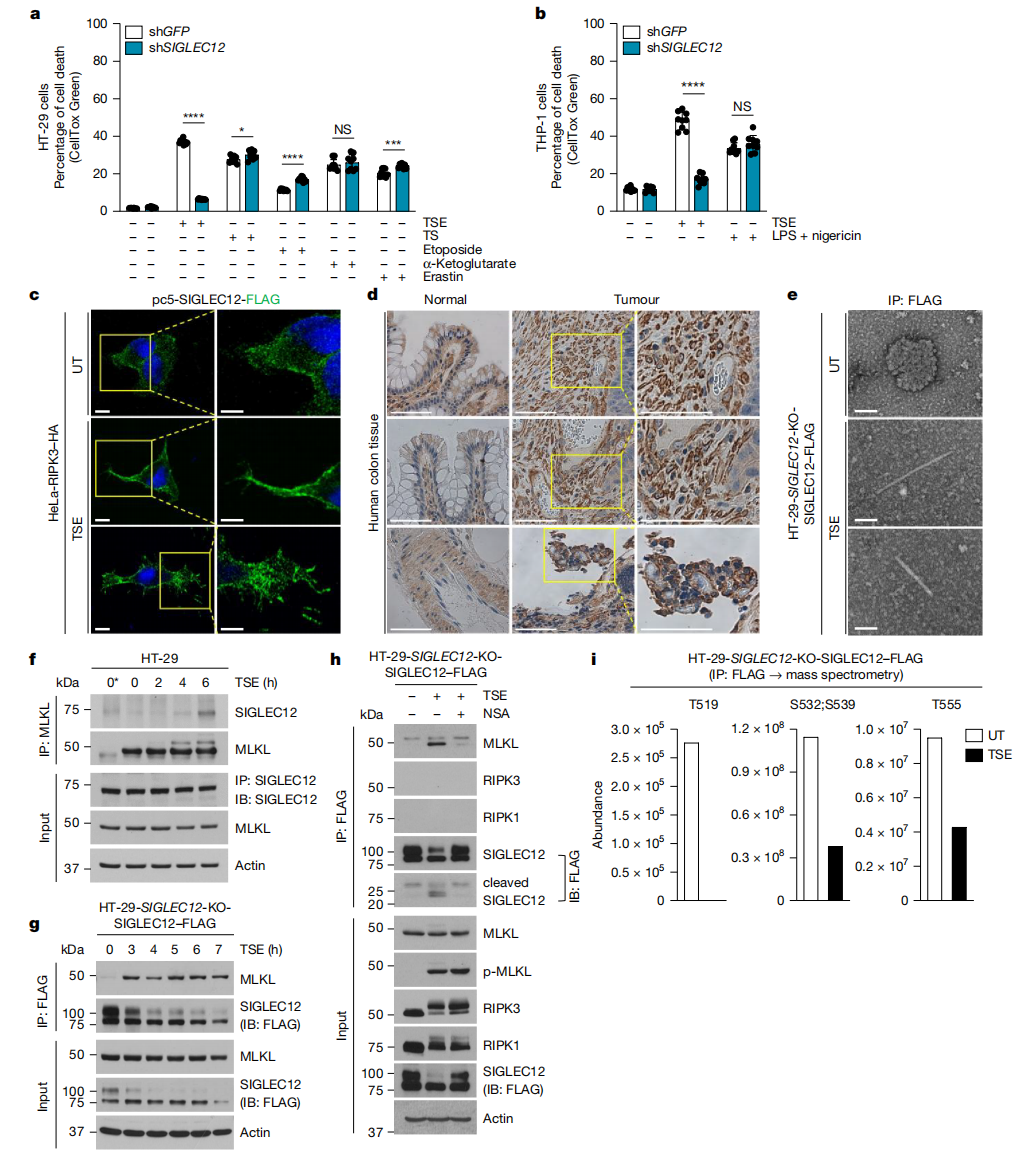
图三 坏死性凋亡过程中SIGLEC12受到调控[4]
为了验证SIGLEC12是否直接诱导质膜破裂,研究者在293T细胞中过表达了全长SIGLEC12,但未检测到显著的细胞死亡现象(图四a)。推测SIGLEC12在坏死性凋亡过程中的激活可能是诱导释放其质膜破裂能力所必需的。实验证实,在坏死性凋亡期间出现了一个约20 kDa的小型切割片段,全长和切割片段都可被C末端FLAG标签的抗体检测到(图四b和c),表明SIGLEC12的胞外区域在坏死性凋亡期间被切割。对该区域胰蛋白酶样蛋白酶切割位点的氨基酸分析显示,保守的Arg410符合此类切割特征,预测在该残基处切割可产生观测到的20 kDa片段。于是,研究者删除信号肽与Arg410之间的氨基酸序列,构建了截短突变体SIGLEC12-ΔN,发现过表达SIGLEC12-ΔN,而非全长SIGLEC12,能显著诱导质膜破裂(图四a)。这种质膜破裂现象不受NSA抑制剂阻断,表明SIGLEC12-ΔN诱导的质膜破裂不依赖于MLKL。SIGLEC12-ΔN的表达足以形成胞质和膜相关的斑点并产生纤维(图四d),表明蛋白质切割事件是驱动SIGLEC12激活并促进纤维组装的关键。
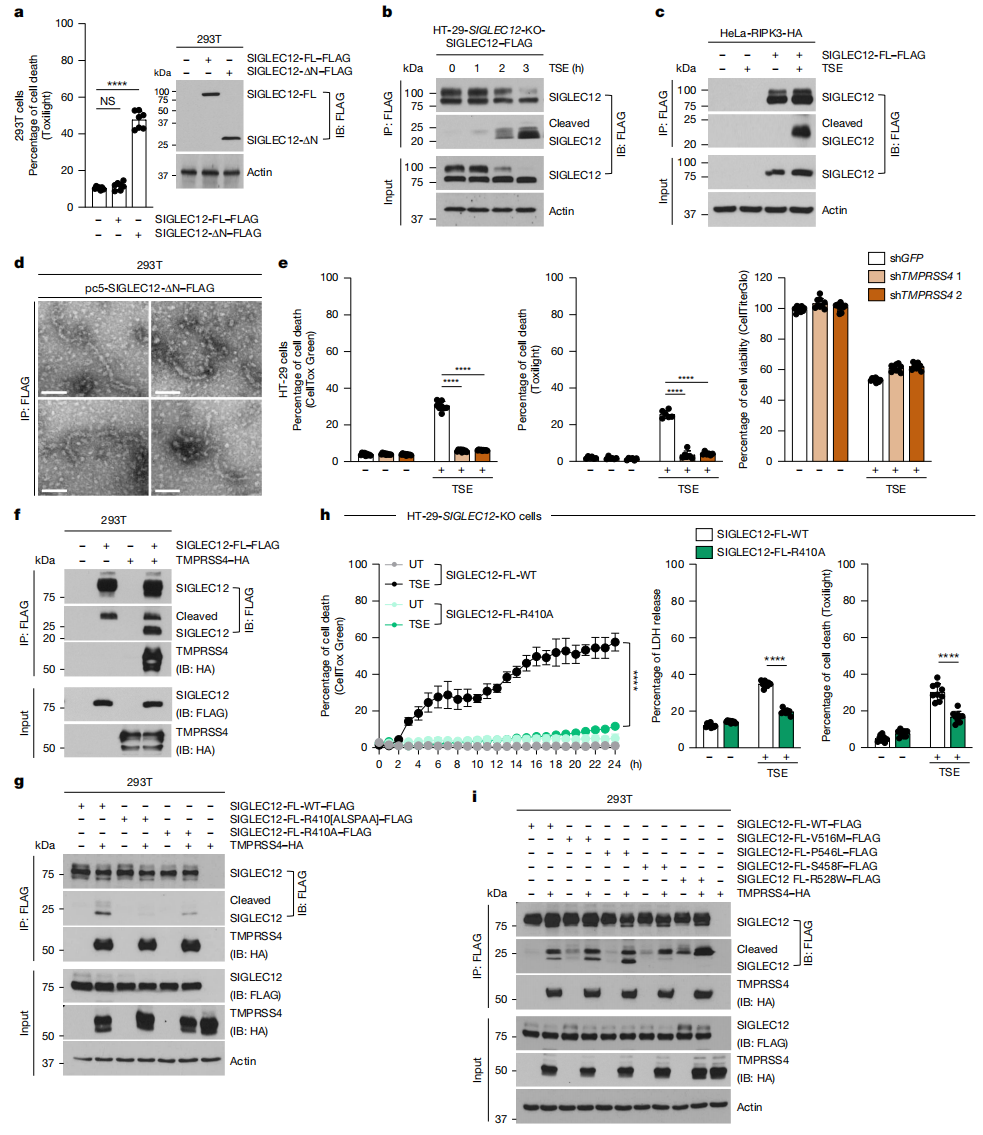
图四 在坏死性凋亡过程中,TMPRSS4切割SIGLEC12诱导质膜破裂[4]
随后,研究者探究坏死性凋亡过程中SIGLEC12的切割机制。先前一项酵母双杂交筛选发现SIGLEC12与一种跨膜蛋白酶TMPRSS4存在相互作用[9]。实验证实,敲降TMPRSS4能抑制坏死性凋亡中的质膜破裂,而不影响上游信号传导(图四e)。此外,TMPRSS4与SIGLEC12存在物理相互作用(图四f和g),共表达野生型TMPRSS4与SIGLEC12-FLAG可诱导SIGLEC12的切割(图四f),这种TMPRSS4诱导的SIGLEC12切割与质膜破裂可被R410位点突变所抑制(图四g和h),表明TMPRSS4在坏死性凋亡过程中对SIGLEC12的胞外切割与激活至关重要,它能将SIGLEC12从前体形式转化为活性形式,进而引发后续的质膜破裂。
癌细胞常丧失坏死性凋亡的能力。分析67,030名癌症患者的癌症基因组图谱(TCGA)数据,发现在SIGLEC12外显子区域存在444个错义突变和63个截短突变。经验证,最高频的SIGLEC12错义突变Ser458Phe会抑制TMPRSS4对SIGLEC12的切割能力(图四i)。值得注意的是,该突变位于NISI基序中,提示该基序可能在SIGLEC12的切割与激活过程中发挥作用,以及SIGLEC12促质膜破裂功能的失活可能是癌症抵抗坏死性凋亡的原因之一。据报道功能性MLKL突变存在于全球2-3%的人口中[10]。通过检索NCBI dbSNP数据库,在正常人群中发现了SIGLEC12的三种主要胞质区变异体:Val516Met、Arg528Trp和Pro546Leu。经验证,Arg528Trp突变也能阻断TMPRSS4对SIGLEC12的切割(图四i)。这些SIGLEC12序列变异对人类生理功能的影响仍有待阐明。
综上所述,该研究确认了人源SIGLEC12是坏死性凋亡过程中质膜破裂的关键蛋白,其具有与NINJ1相似的结构特征和序列特性(如NISI基序)。SIGLEC12缺失并不阻断RIPK1/RIPK3/MLKL激活,却显著抑制质膜破裂和炎症因子释放,细胞呈“泡状膨胀”形态。在坏死性凋亡期间,SIGLEC12被TMPRSS4切割,产生携带NISI基序的C端20 kDa小片段,后者聚集成纤维并执行质膜破裂。SIGLEC12介导的质膜破裂具有物种特异性,可能为人类特有,揭示了程序性坏死执行机制的复杂性,为靶向SIGLEC12/TMPRSS4轴干预促炎性细胞死亡相关疾病提供了潜在治疗靶点。

GTP研发中心负责实施基因组标签计划(Genome tagging project, GTP),基于自主知识产权的类精子干细胞介导半克隆技术,为全基因组的功能基因一一贴上标签,致力于构建标签细胞和标签小鼠资源库。类精子干细胞是从精子来源单倍体囊胚中建系获得的一种孤雄单倍体胚胎干细胞,将其注入卵母细胞,能够像精子一样支持整个胚胎发育过程,产生健康的半克隆小鼠。GTP研发中心在类精子干细胞的蛋白质编码基因上原位敲入标签序列,建立了液氮保存的标签细胞资源库。研究需要时,利用半克隆技术将标签细胞注射到小鼠卵母细胞中,一步法获得标签小鼠。

已有标签产品可直接订购,详情查阅以下官网链接。如有需要欢迎联系,我们将竭诚为您服务。
标签细胞网址:
标签小鼠网址:
http://www.sibcb.ac.cn/gtp/msearch.jsp
地址:上海市岳阳路320号
责任编辑:甜点
新媒体运营:suway
参考文献
1. Khoury MK, Gupta K, Franco SR, Liu B: Necroptosis in the Pathophysiology of Disease. The American journal of pathology 2020, 190(2):272-285.
2. Kayagaki N, Kornfeld OS, Lee BL, Stowe IB, O'Rourke K, Li Q, Sandoval W, Yan D, Kang J, Xu M et al: NINJ1 mediates plasma membrane rupture during lytic cell death. Nature 2021, 591(7848):131-136.
3. Ramos S, Hartenian E, Santos JC, Walch P, Broz P: NINJ1 induces plasma membrane rupture and release of damage-associated molecular pattern molecules during ferroptosis. Embo j 2024, 43(7):1164-1186.
4. Noh H, Hashem Z, Boms E, Najafov A: SIGLEC12 mediates plasma membrane rupture during necroptotic cell death. Nature 2026, 649(8096):460-466.
5. Aagaard L, Amarzguioui M, Sun G, Santos LC, Ehsani A, Prydz H, Rossi JJ: A facile lentiviral vector system for expression of doxycycline-inducible shRNAs: knockdown of the pre-miRNA processing enzyme Drosha. Molecular therapy : the journal of the American Society of Gene Therapy 2007, 15(5):938-945.
6. Crocker PR, Paulson JC, Varki A: Siglecs and their roles in the immune system. Nat Rev Immunol 2007, 7(4):255-266.
7. Degen M, Santos JC, Pluhackova K, Cebrero G, Ramos S, Jankevicius G, Hartenian E, Guillerm U, Mari SA, Kohl B et al: Structural basis of NINJ1-mediated plasma membrane rupture in cell death. Nature 2023, 618(7967):1065-1071.
8. Wang H, Sun L, Su L, Rizo J, Liu L, Wang LF, Wang FS, Wang X: Mixed lineage kinase domain-like protein MLKL causes necrotic membrane disruption upon phosphorylation by RIP3. Mol Cell 2014, 54(1):133-146.
9. Luck K, Kim DK, Lambourne L, Spirohn K, Begg BE, Bian W, Brignall R, Cafarelli T, Campos-Laborie FJ, Charloteaux B et al: A reference map of the human binary protein interactome. Nature 2020, 580(7803):402-408.
10. Garnish SE, Martin KR, Kauppi M, Jackson VE, Ambrose R, Eng VV, Chiou S, Meng Y, Frank D, Tovey Crutchfield EC et al: A common human MLKL polymorphism confers resistance to negative regulation by phosphorylation. Nature communications 2023, 14(1):6046.
转载请注明来源于【GTP研发中心】
声明:本文仅用于分享,不代表GTP研发中心立场,若有侵权,请及时联系我们第一时间更正!



