技术分享:人类染色体的高保真转移与內源性消除
合成基因组学是对生物基因组DNA进行编辑、合成以及组合的一个新兴交叉学科,是合成生物学的关键底层技术。人类基因组合成技术有助于理解天然基因组序列及其架构背后的因果关系与规律,可用于重建灭绝古人类的基因型,加速生物生产进程,提升细胞疗法疗效等。然而,人类染色体体积过于庞大,无法在常规的微生物宿主中进行组装,尽管后者已成功应用于支原体和大肠杆菌基因组合成、以及酿酒酵母染色体合成[1, 2]。此外,人类DNA包含高度重复序列,使得在酿酒酵母等易发生同源重组的宿主中也难以实现大规模的稳定维持与操作。在二倍体基因组的人类细胞中,对单个染色体拷贝进行靶向操作同样面临挑战。因此,亟需开发新技术以应对人类基因组合成面临的诸多难题。
2025年12月,Science期刊报道了一种分步实现精准高保真构建合成人类染色体的新策略(图一)。该策略分为三步:首先,将人类染色体从人类细胞简便转移至小鼠胚胎干细胞(组装细胞),使其呈现单倍体状态、非必需性、且可进行遗传操作;其次,将这些人类染色体从单染色体杂合体系重新导入人类细胞,以构建特定合成的非整倍体;最后,在非整倍体中消除相应的内源人类染色体,使细胞恢复二倍体状态且携带转移染色体。以上所有步骤均在非转化细胞中进行,未引发染色体碎裂现象,且仅产生极少量结构变异、插入、缺失或单核苷酸变异[3]。
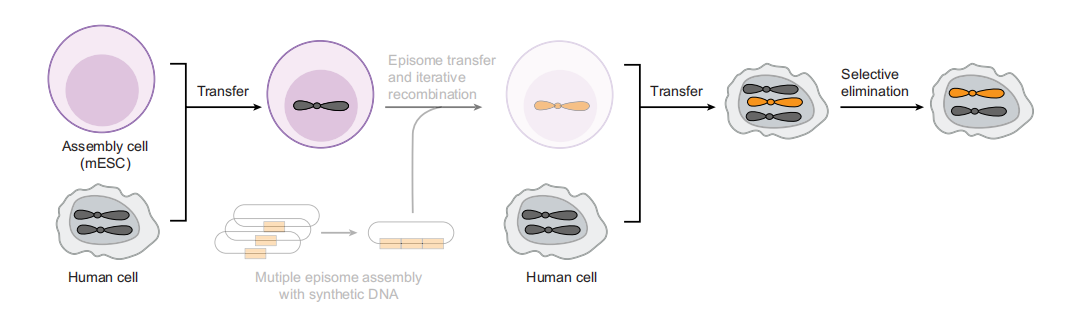
图一 携带合成人类染色体的人类细胞构建策略[3]
首先是供体细胞和组装细胞的选择与准备。研究者选择非转化且永生化的人类视网膜色素上皮(RPE1)细胞系作为染色体转移实验的供体,因其具有稳定且接近二倍体的核型[4]。为便于后续识别和分离人类染色体,研究者对RPE1供体的所有染色体进行标记,使用PiggyBac转座子系统标记上超级折叠绿色荧光蛋白(sfGFP)和G418抗性的新霉素抗性基因(sfGFP-NEO)[5]。这些标记位点均匀分布于基因组中,并且每条染色体的标记数量与其长度呈正相关。研究者选择小鼠胚胎干细胞(mESC)作为组装细胞,异源性可提高编辑单条人类染色体的效率,同时降低发生重组的风险,以及鼠源脱靶效应不会传递至终产物人类细胞中。
其次是分离人类染色体与导入组装细胞。将表达sfGFP-NEO的RPE1供体细胞用秋水仙胺处理6-9小时,使其停滞于M期,并用肌动蛋白聚合抑制剂latrunculin B处理1小时[6]。随后将凝缩的染色体从细胞中释放至保护性多胺缓冲液,获得的染色体悬液通过聚乙烯亚胺(PEI)转染至mESC,转染效率仅约为10-6(图二A)[7]。经过13次独立的染色体转染实验,获得了49个G418抗性mESC克隆。总体而言,这些克隆覆盖了13条不同的人类染色体(4, 5, 6, 8, 9, 10, 12, 13, 14, 19, 20, 21和22),包含有完整的人类染色体、片段化染色体或存在内部拷贝数变异染色体。研究者对三个mESC克隆Hchr4(CL3)、Hchr21(CT2-1)和Hchr20(CB20F)进行深入表征。G带分析及流式核型分析结果显示,这些克隆存在单条完整的人类染色体(图二B和C),覆盖了人类染色体的三种类型:亚中着丝粒染色体(4号染色体;193.5 Mb)、中央着丝粒染色体(20号染色体;66.2 Mb)和近端着丝粒染色体(21号染色体;45.1 Mb)。对这三个克隆分别进行高覆盖度(20-30×)Illumina全基因组测序、牛津纳米孔长读长和PacBio测序、以及Bionano光学基因组图谱分析(图二D-G),发现这三个组装细胞中各含有一份相应人类染色体的单拷贝(图二D和E),且mESC中完整人类染色体出现的拷贝数变异、结构变异、插入缺失以及单核苷酸变异频率较低,与RPE1供体细胞的变异频率偏差极小(图二H和I)。利用光学基因组图谱技术测量末端标记至单个DNA分子末端的距离,来估算染色体末端的端粒长度[8]。发现在RPE1细胞中,Hchr4和 Hchr21的端粒分子长度在5到10 kb 之间,这与预期相符[9]。有趣的是,在mESC单染色体杂交体中,映射至人类4号和21号染色体端粒区域的分子长度显著增加,mESC Hchr4的端粒中位长度分别达到99 kb(4p)和108 kb(4q),mESC Hchr21的21q臂端粒中位长度为57 kb,多数长度介于30-120 kb之间(图二J)。mESC中人类染色体臂的端粒分子长度,与同一克隆中内源小鼠染色体的端粒长度相当(约100 kb,图二J),也与文献报道的小鼠端粒长度相近。表明将人类染色体转移至mESC后,其端粒被主动延长以匹配小鼠端粒长度的设定值,并能维持在该长度。
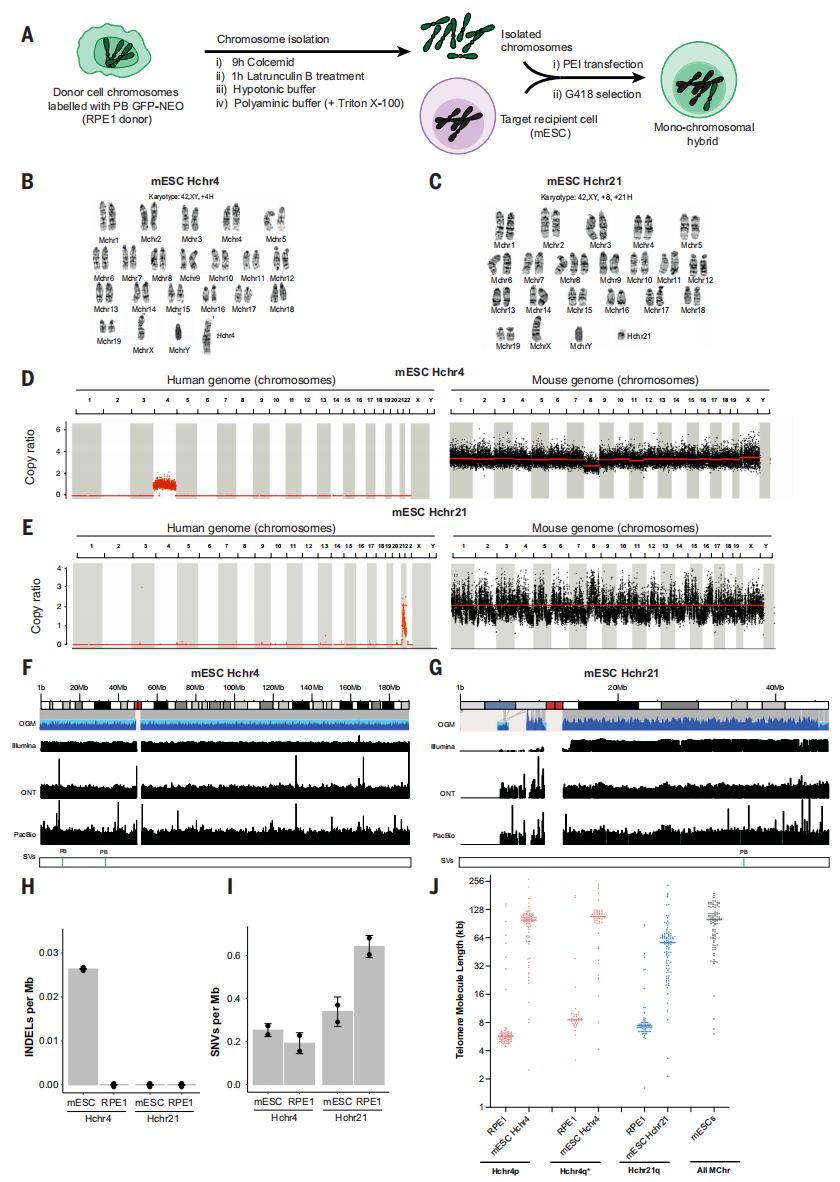
图二 人类染色体可被转染至mESC中并能稳定维持[3]
为验证人类染色体在mESC中的可编辑性,研究者尝试将Hchr20染色体35.69-35.70 Mb区域替换成合成DNA,实现ROMO1和NFS1基因座内的23个野生型密码子置换为同义密码子。先在Hchr20染色体中预先整合“着陆垫”,后者含有蓝色荧光蛋白 (BFP) 和潮霉素抗性 (HygR)。随后电转导入一个35 kb的BAC载体,其携带10 kb的合成DNA及mCherry/PuroR筛选盒。同时利用CRISPR Cas9切割人类染色体,诱导同源重组介导的着陆垫与BAC的同源合成DNA置换。经基因分型、流式细胞术和纳米孔测序多重验证,确认了合成DNA在Hchr20中的成功整合以及序列正确,表明在mESC组装细胞中对人类染色体进行遗传操作的可行性。
再次,将人类染色体从单染色体杂合mESC转移至人类细胞,获得染色体特异性的非整倍体。为此,研究者开发了一种快速微细胞介导染色体转移技术(R-MMCT)。传统的MMCT技术需要长达2-4天的秋水仙胺处理以诱导有丝分裂阻滞,这不仅导致微核形成和染色体断裂,克隆存活率大幅降低,且仅能应用于少数可耐受超倍体化的细胞类型如A9和CHO[10]。而R-MMCT技术通过显著缩短秋水仙胺处理时间,使用经短暂处理的有丝分裂细胞制备微细胞,按大小筛选后,利用失活的仙台病毒(HVJ-E)使微细胞与RPE1受体细胞进行融合[6],再通过G418筛选出携带转移染色体的RPE1细胞,效率仅约为10-6(图三A)。以携带Hchr21、Hchr4、Hchr20人类染色体的mESC为供体,独立进行R-MMCT实验,分别获得了107、51和42个表型正确的RPE1克隆。对其中两种三体细胞系Hchr4(2A8)和Hchr21(7M5-1-2)克隆进行深入表征。低覆盖度全基因组测序、sfGFP稳定性及流式核型分析结果,均表明这些细胞系中存在完整且稳定的非整倍体。G带核型分析显示,所有选定克隆均因成功转移染色体而呈现出预期的染色体拷贝数增加(图三B和C)。测序和基因组图谱的综合数据(图三D-I)表明,通过R-MMCT技术可将完整人类染色体从单染色体杂合mESC转移至人类细胞,不残留小鼠DNA,且该过程引发的DNA损伤与突变极低(图三H)。扩增RPE1克隆并经连续传代培养至少六代后,通过光学基因组图谱数据估算端粒的长度。结果显示,对于Hchr4、Hchr20和Hchr21染色体,多数映射至端粒区域的分子长度与野生型RPE1细胞相似。然而,在Hchr21(7M5-1-2)的Hchr21q端粒、Hchr4(2A8)的Hchr4p与Hchr4q端粒中,部分端粒(15-150 kb)显著长于对照RPE1细胞(5-10 kb,图三I),表明人类染色体转移后的端粒长度通常短于其在mESC的状态,且随着传代次数的增加,可能逐步缩短至人类端粒的典型长度,即恢复到内源性染色体的状态。
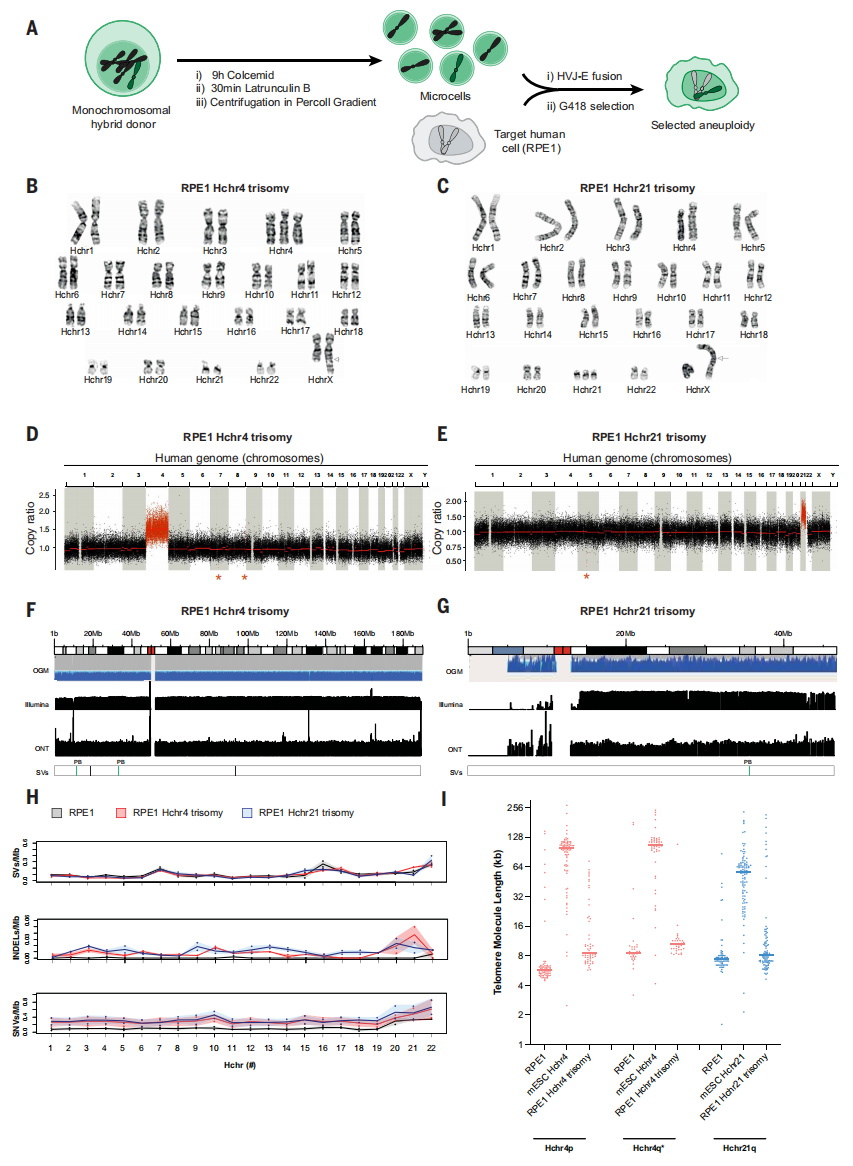
图三 通过R-MMCT技术将人类染色体从单染色体杂合mESC转移至RPE1细胞[3]
最后,研究者尝试从非整倍体克隆中消除内源性人类染色体,采用PIGA负向筛选标记方式,在前面构建的三体RPE1细胞中消除内源性4号或21号染色体。PIGA基因位于X染色体,编码GPI锚定生物合成途径的关键组分。可利用原气单胞菌素筛选GPI缺陷细胞,这种由嗜水气单胞菌产生的原毒素经蛋白酶切割激活后,通过与GPI锚结合形成跨膜孔道导致细胞裂解死亡[11]。研究者先在前面构建的三体RPE1细胞中敲除PIGA,同时将包含负筛选标记PIGA和BFP报告基因(PIGA-BFP)引入目标内源性4号或21号人类染色体(图四A)。随后用CRISPR切割目标染色体的着丝粒周边区域,短暂抑制有丝分裂检查点。通过流式细胞术分选sfGFP阳性、BFP阴性的细胞以富集那些保留转移染色体但丢失筛选标记的细胞,再利用原气单胞菌素筛选出成功消除目标内源性染色体的克隆(图四A-C),如消除内源Hchr4的 elCL18和 elCL35,以及消除内源Hchr21的elCL1和elCL2(图四D和E)。多重分析结果显示,这些克隆均为二倍体且转移染色体的结构保持完整(图四D-I),DNA损伤和变异基本与其直接来源的非整倍体细胞系相当(图四J)。消除内源性染色体后,保留的转移染色体Hchr4p、Hchr4q和Hchr21q的端粒分子中位长度与野生型RPE1中的长度无显著差异(图四K),表明内源性染色体消除及传代培养后,转移染色体的端粒长度可恢复至野生型RPE1细胞的水平。
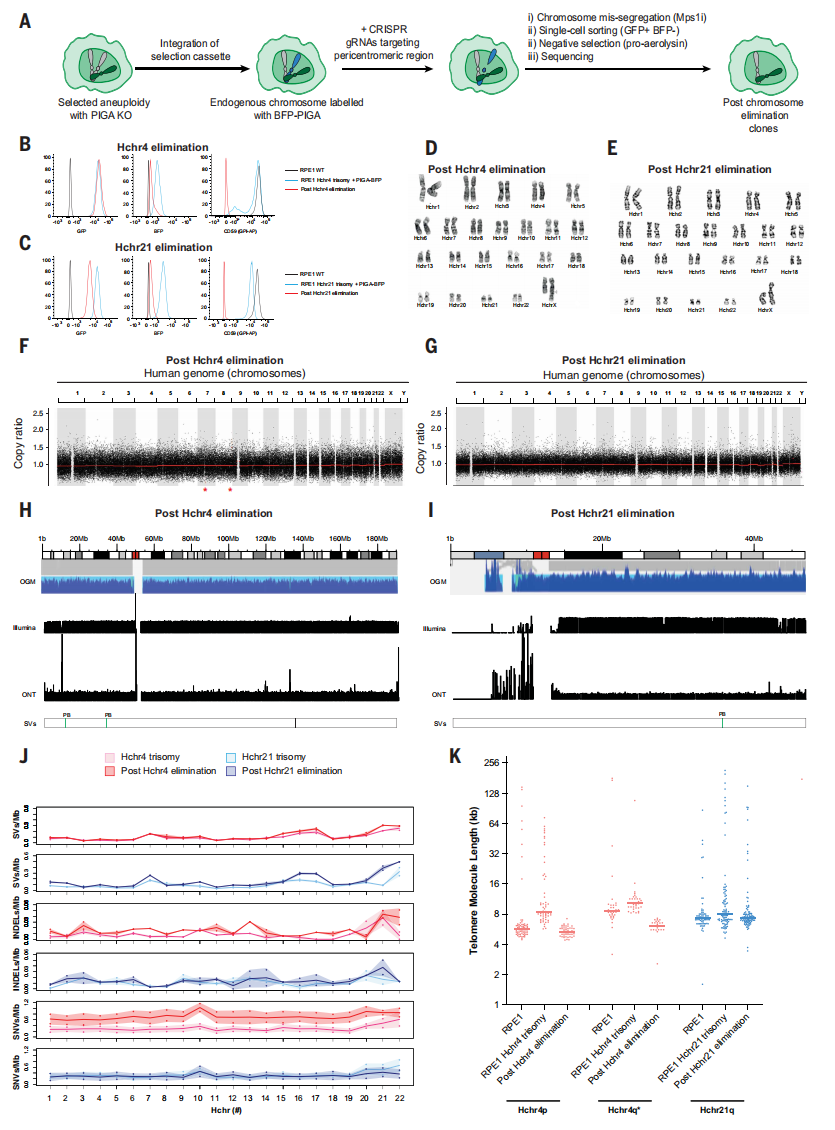
图四 靶向消除三体RPE1细胞中的非整倍体内源染色体[3]
综上所述,该研究建立了一套高保真构建合成人类染色体的工作流程。利用小鼠胚胎干细胞(mESC)作为组装细胞,导入分离的人类染色体,同时在mESC中对其进行遗传操作,最终将人工改造染色体重新导入人类细胞,并恢复正常的核型结构。该流程涉及的染色体转染和R-MMCT技术,在已测试的染色体转移操作中均展现出相当高的保真度和效率。过程中产生的中间型非整倍体,为研究特定染色体拷贝数变化的影响提供了资源。人类染色体在mESC组装细胞中呈非必需状态,为进一步的遗传操作例如删除必需基因或单倍剂量不足基因创造了条件。未来,结合大片段合成DNA的构建与递送技术、mESC中大范围染色体区域替换技术的发展,有望加速人类基因组合成。

GTP研发中心负责实施基因组标签计划(Genome tagging project, GTP),基于自主知识产权的类精子干细胞介导半克隆技术,为全基因组的功能基因一一贴上标签,致力于构建标签细胞和标签小鼠资源库。类精子干细胞是从精子来源单倍体囊胚中建系获得的一种孤雄单倍体胚胎干细胞,将其注入卵母细胞,能够像精子一样支持整个胚胎发育过程,产生健康的半克隆小鼠。GTP研发中心在类精子干细胞的蛋白质编码基因上原位敲入标签序列,建立了液氮保存的标签细胞资源库。研究需要时,利用半克隆技术将标签细胞注射到小鼠卵母细胞中,一步法获得标签小鼠。

已有标签产品可直接订购,详情查阅以下官网链接。如有需要欢迎联系,我们将竭诚为您服务。
标签细胞网址:
标签小鼠网址:
http://www.sibcb.ac.cn/gtp/msearch.jsp
地址:上海市岳阳路320号
责任编辑:甜点
新媒体运营:suway
参考文献
1. Fredens J, Wang K, de la Torre D, Funke LFH, Robertson WE, Christova Y, Chia T, Schmied WH, Dunkelmann DL, Beránek V et al: Total synthesis of Escherichia coli with a recoded genome. Nature 2019, 569(7757):514-518.
2. Schindler D, Walker RSK, Jiang S, Brooks AN, Wang Y, Müller CA, Cockram C, Luo Y, García A, Schraivogel D et al: Design, construction, and functional characterization of a tRNA neochromosome in yeast. Cell 2023, 186(24):5237-5253.e5222.
3. Petris G, Grazioli S, van Bijsterveldt L, Murat P, Liu KC, Birnbaum J, Sale JE, Chin JW: High-fidelity human chromosome transfer and elimination. Science 2025, 390(6777):1038-1043.
4. Bodnar AG, Ouellette M, Frolkis M, Holt SE, Chiu CP, Morin GB, Harley CB, Shay JW, Lichtsteiner S, Wright WE: Extension of life-span by introduction of telomerase into normal human cells. Science 1998, 279(5349):349-352.
5. Elsässer SJ, Ernst RJ, Walker OS, Chin JW: Genetic code expansion in stable cell lines enables encoded chromatin modification. Nat Methods 2016, 13(2):158-164.
6. Liskovykh M, Lee NC, Larionov V, Kouprina N: Moving toward a higher efficiency of microcell-mediated chromosome transfer. Mol Ther Methods Clin Dev 2016, 3:16043.
7. Ng BL, Carter NP: Factors affecting flow karyotype resolution. Cytometry A 2006, 69(9):1028-1036.
8. Young E, Pastor S, Rajagopalan R, McCaffrey J, Sibert J, Mak ACY, Kwok PY, Riethman H, Xiao M: High-throughput single-molecule mapping links subtelomeric variants and long-range haplotypes with specific telomeres. Nucleic acids research 2017, 45(9):e73.
9. Blasco MA: Telomeres and human disease: ageing, cancer and beyond. Nat Rev Genet 2005, 6(8):611-622.
10. Uno N, Takata S, Komoto S, Miyamoto H, Nakayama Y, Osaki M, Mayuzumi R, Miyazaki N, Hando C, Abe S et al: Panel of human cell lines with human/mouse artificial chromosomes. Sci Rep 2022, 12(1):3009.
11. Buckley JT, Howard SP: Aerolysin from Aeromonas hydrophila. Methods in enzymology 1988, 165:193-199.
转载请注明来源于【GTP研发中心】
声明:本文仅用于分享,不代表GTP研发中心立场,若有侵权,请及时联系我们第一时间更正!



