技术分享:揭示线粒体靶向序列的应激信号传导新功能
线粒体是细胞代谢与信号传递的核心细胞器,包含了1000余种蛋白质,其中大部分是在细胞质核糖体上合成,随后通过翻译后易位进入线粒体[1]。这些线粒体前体蛋白大多含有一个15-55个残基组成的N端线粒体靶向序列(MTS)[1-3]。MTS通过线粒体外膜(TOM)和内膜转位酶复合体(TIM)介导了蛋白质转运,并在进入基质后被切除[1]。前体蛋白的完全导入需要一个由TIM亚基、线粒体Hsp70及其辅助伴侣蛋白组成的ATP依赖性Hsp70马达系统[1, 4]。
低效的前体蛋白导入不仅消耗了线粒体必需因子,还使其在细胞的其他部位积累,损害了线粒体和细胞的稳态[1, 5, 6]。线粒体蛋白质输入缺陷已被证明与多种疾病相关,包括神经退行性疾病和生物能量紊乱[1, 5, 7]。细胞可以通过限制细胞质翻译和增强蛋白质质量控制的转录程序、或线粒体特异性通路如未折叠蛋白反应(UPRmt)来应对线粒体蛋白质输入应激[8, 9]。尽管UPRmt的激活机制已较为明确,但其他线粒体应激信号如何传递至细胞核仍不清楚。最近研究表明,线粒体蛋白质输入受损可导致前体蛋白停滞于TOM[10, 11]。这种缺陷可由ATP酶Cdc48(哺乳动物为Vcp)和Msp1(Atad1)修复,它们能提取停滞的多肽并清理转位酶[11, 12]。在芽殖酵母中,Msp1高效募集至堵塞的转位酶需要接头蛋白CIS1,后者是线粒体蛋白输入受损反应(mitoCPR)的靶标之一。mitoCPR又受转录因子Pdr3的调控[12]。然而,线粒体应激信号是如何传递并激活Pdr3仍然未知。
2026年1月,Nature期刊发表了一项研究,揭示了酵母线粒体Hsp70辅助伴侣蛋白Mge1可作为应激信使发挥作用。在线粒体应激期间,未导入线粒体的Mge1前体蛋白进入了细胞核,进而触发线粒体蛋白输入受损反应(mitoCPR)靶基因的转录。这一应激信号传导功能依赖于Mge1的线粒体靶向序列(MTS)与转录因子Pdr3的相互作用。该研究揭示了MTS的新功能,除负责传统的蛋白靶向输入功能外,还可作为线粒体应激信号的传递介质,指示着线粒体的健康状态[13]。
研究者前期研究证实,线粒体蛋白输入缺陷通过激活转录因子Pdr3来触发mitoCPR,Psd1过表达会损害线粒体蛋白输入并激活mitoCPR[12]。定位结果显示,GFP标记的Pdr3在基础条件下定位于细胞核(图一a),且过表达Psd1也不影响Pdr3的核定位(图一a)。染色质免疫沉淀(ChIP)实验显示,无论在对照细胞还是PSD1过表达细胞(PSD1OE)中,Pdr3均与mitoCPR靶基因CIS1的启动子相结合(图一b),表明Pdr3并非直接感知线粒体缺陷,而是对蛋白输入受损时传递到细胞核的信号作出了响应。为了揭示Pdr3的响应机理,研究者构建了一个报告系统,将LEU2基因置于CIS1的启动子下游[12],使发生mitoCPR的细胞能够在缺乏亮氨酸的条件下生长。随后进行全基因组范围的过表达筛选,发现筛选出的前20个候选基因中,8个为线粒体蛋白(图一c)。
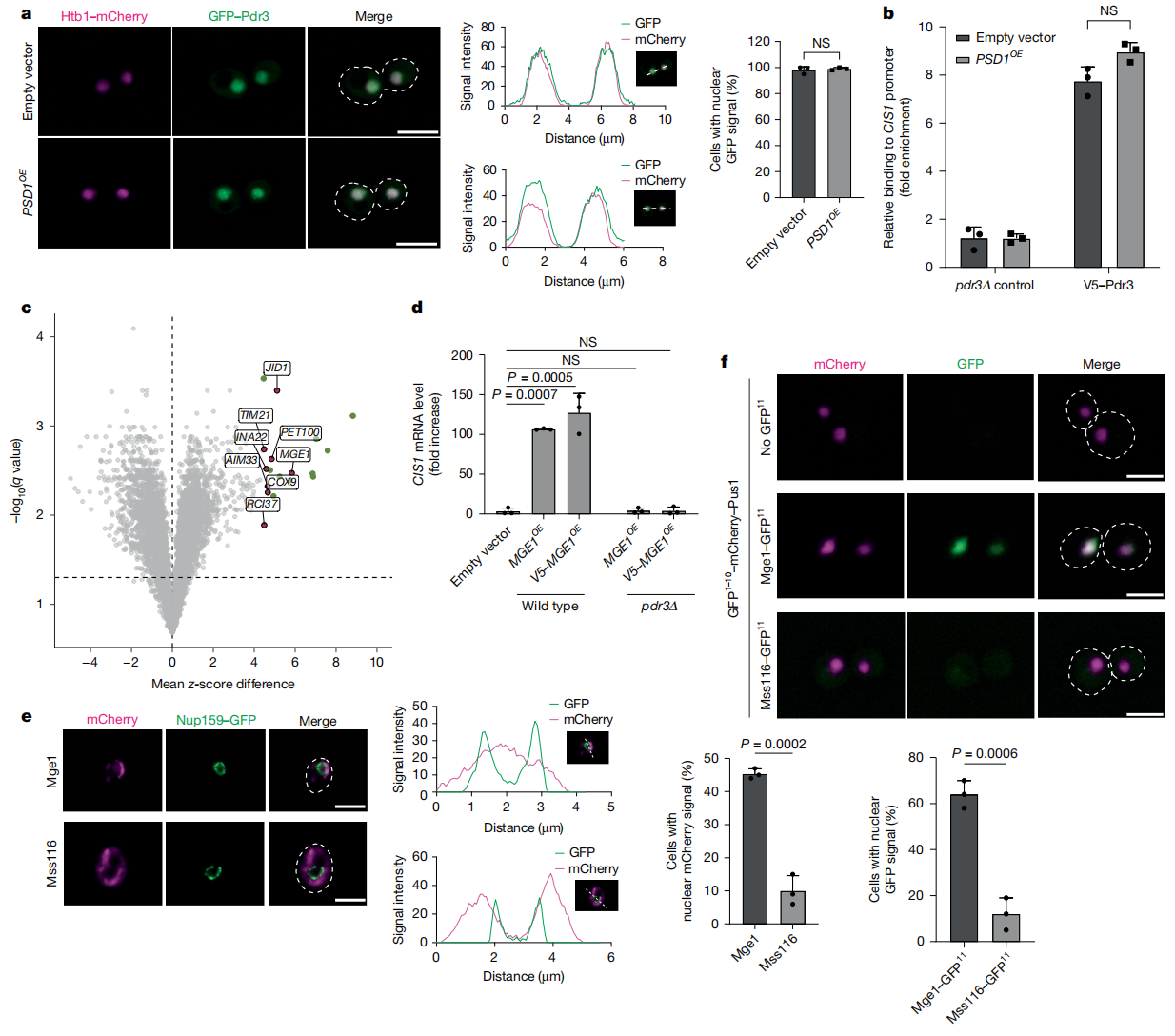
图一 遗传筛选发现Pdr3的潜在激活因子Mge1[13]
当蛋白输入受损时,线粒体前体蛋白可能积聚在包括细胞核在内的多种细胞区室中[6, 14, 15],线粒体蛋白过表达也可能因超出容量而产生类似效应,导致部分过表达的前体在线粒体外积累。为排除其他间接激活因素,研究者在候选蛋白的MTS上游插入V5标签,以掩盖MTS阻断易位,防止其在线粒体内积累造成间接损伤。结果显示,过表达N端标记V5的候选蛋白后,大多数均未能触发CIS1上调;而过表达V5-Mge1能强烈诱导CIS1,与野生型Mge1相当,且具有Pdr3依赖性(图一d),提示Mge1在Pdr3激活中发挥直接作用。Mge1是一种与细菌GrpE同源的基质辅助伴侣蛋白[16],通过介导线粒体Hsp70的核苷酸释放,帮助蛋白质转入基质以及蛋白质折叠[16]。与对照线粒体蛋白Mss116不同,过表达Mge1-mCherry不仅与线粒体共定位,还能与细胞核共定位(图一e)。研究者进一步使用分裂型GFP系统,将GFP1-10与核蛋白融合,GFP11分别与Mge1或Mss116融合,出现GFP荧光信号表明进入了细胞核。结果显示,单独表达核定位GFP1–10或与Mss116-GFP11共表达时均未检测到GFP信号,而与Mge1-GFP11共表达时,约65%的细胞中出现了荧光信号(图一f),提示并非所有Mge1前体都被输入线粒体,部分Mge1可能转位至细胞核,进而诱导mitoCPR。
于是,研究者利用PSD1OE模拟蛋白输入受损,进一步监测Mge1前体的定位。在Mge1内源基因位点的C端融合Flag标签,该标签融合位置不影响蛋白输入。在对照组细胞中,仅检测到单一形式的Mge1-Flag,对应于成熟切割后的蛋白大小;而在PSD1OE细胞中存在两种形式的Mge1-Flag,表明其前体蛋白出现积累(图二a)。进一步分离细胞组分,发现在线粒体富集组分中仅能检测到Mge1成熟形式,未能检测到其前体。从PSD1OE细胞分离的细胞核中,检测到了Mge1-Flag的前体形式而非成熟形式(图二b),表明在线粒体输入受损的情况下,Mge1前体可以转位进入细胞核。使用预测工具未能在Mge1中鉴定出典型的核定位信号[17]。因此,研究者测试了Mge1的MTS是否是其核定位所必需的。结果显示,与全长Mge1不同,缺失MTS的ΔMTS-Mge1-Flag在PSD1OE细胞核中完全消失,仅在非核组分中被检测到(图二c),表明Mge1的MTS可能参与促进其核转位。研究者系统敲除多个非必需的核转运蛋白-β基因,发现在缺失KAP114、KAP122、KAP104或NMD5的细胞中,PSD1OE仍能诱导CIS1上调,但在kap123∆细胞中未观察到上调现象(图二d),且Mge1前体在其细胞核中几乎检测不到(图二e),表明Kap123是Mge1前体核定位所必需的。
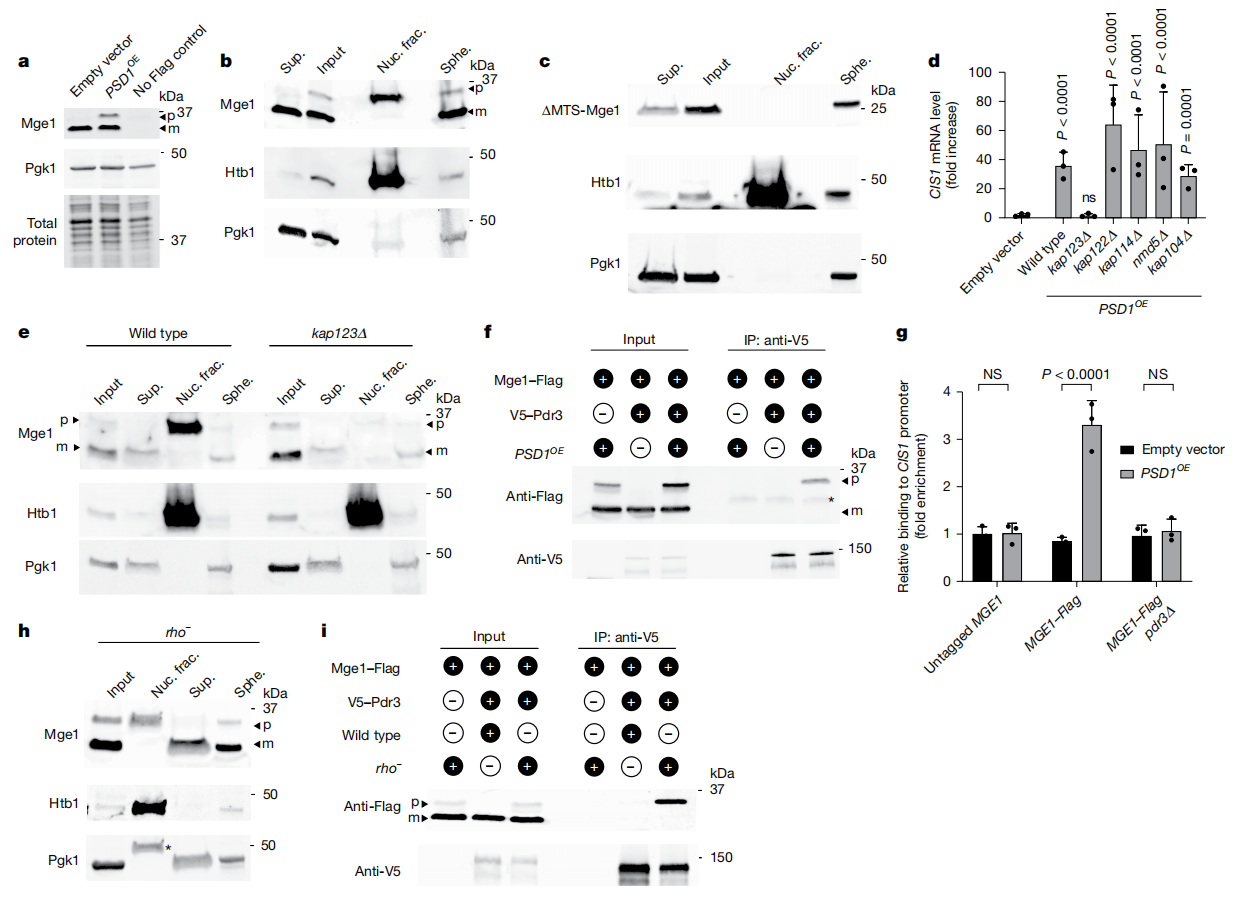
图二 内源性Mge1前体转位到细胞核并结合Pdr3[13]
Mge1的核定位现象提示其可能直接影响Pdr3。免疫共沉淀实验显示,仅在蛋白输入应激条件下,V5-Pdr3与Mge1-Flag前体存在相互作用(图二f)。进一步下拉Mge1-Flag进行了ChIP实验,发现仅在线粒体蛋白输入缺陷的条件下,Mge1-Flag才与CIS1启动子结合,并且这种结合在pdr3∆细胞中未被检测到(图二g),表明Mge1是通过与Pdr3的相互作用而定位到染色质上的。测试另一种线粒体蛋白输入受损的酵母模型,线粒体DNA部分缺失的突变体(rho−)存在呼吸缺陷,表现出线粒体膜电位降低和蛋白输入缺陷[18]。与PSD1OE系统类似,在rho−细胞核中检测到Mge1前体,且仅前体与Pdr3发生免疫共沉淀(图二h和i),表明在急性和慢性线粒体蛋白输入缺陷模型中Mge1前体蛋白均与Pdr3存在相互作用。
接下来,研究者验证Mge1是否是触发mitoCPR所必需的。由于MGE1是必需基因[16],研究者采用了生长素诱导降解标签系统(AID系统)。在基础条件下,仅能检测到内源性表达的Mge1-AID成熟形式;而当蛋白质输入受抑制时,其前体出现积累;生长素处理能消除大部分Mge1-AID前体(图三a)。此时,Mge1的耗竭显著削弱了细胞对蛋白质输入应激的CIS1上调反应(图三b)。将Mge1融合出核信号后,可阻断其在细胞核内的积累。表达出核变体的细胞在PSD1OE条件下也无法诱导CIS1转录(图三c)。为考察其他线粒体前体是否与Pdr3结合,研究者通过免疫沉淀结合质谱分析技术系统鉴定了Pdr3的相互作用组。通过比较基础条件与蛋白质输入应激条件下Pdr3复合物的组成,鉴定出应激特异性相互作用蛋白。结果显示,Mge1是唯一显著富集的应激特异互作蛋白,富集倍数超过两倍(图三d)。利用半乳糖诱导的PSD1OE系统,监测应激恢复过程中Mge1前体的动态变化。当添加葡萄糖终止PSD1过表达后,观察到Mge1前体水平和CIS1 mRNA表达量在6小时内均逐渐下降(图三e和f),表明PSD1过表达诱导的Mge1前体积累具有可逆性。
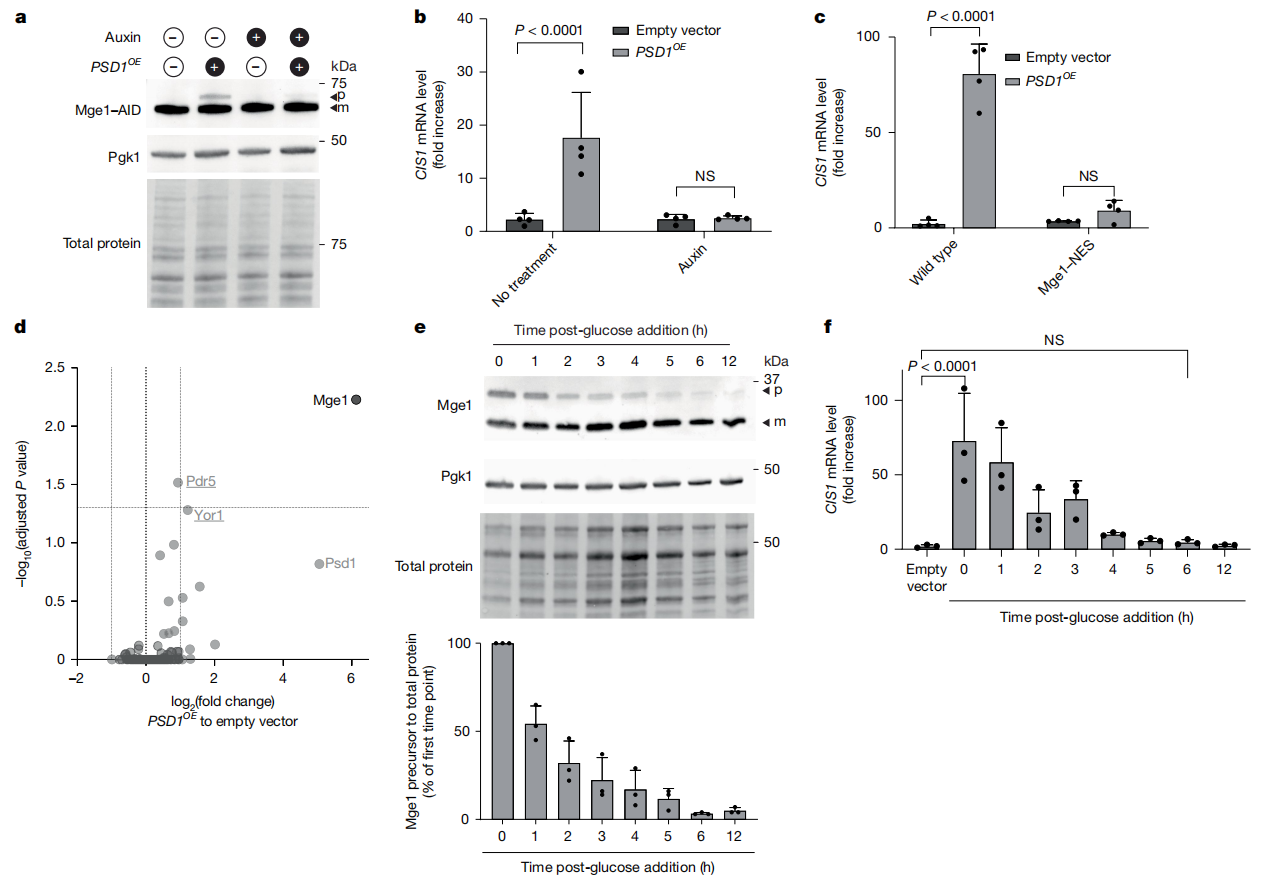
图三 Mge1对mitoCPR的激活至关重要[13]
随后,研究者探究Mge1中负责激活mitoCPR的功能域。Mge1前体包含了介导线粒体导入的MTS和作为Hsp70辅助伴侣蛋白发挥功能的成熟蛋白部分[16]。过表达MTS缺失的截短突变体ΔMTS-Mge1后,发现不能激活mitoCPR(图四a),其呈现出弥散的细胞质分布模式而非明显的核定位。在ΔMTS-Mge1上融合核定位信号,也未能诱导CIS1的表达(图四a),表明成熟形式的Mge1不足以介导mitoCPR的信号传导。有趣的是,单独过表达Mge1 MTS的mCherry融合蛋白能诱导CIS1表达,而Mss116的MTS则不行(图四a),表明发挥激活信号功能的是Mge1 MTS本身,而不是成熟蛋白的辅助伴侣活性。为全面表征Mge1 MTS触发的响应模式,研究者比较了过表达MTS(Mge1)-mCherry与对照MTS(Mss116)-mCherry细胞的全局基因表达谱,分析其与Psd1过表达诱导转录谱的相关性。结果显示,共有35个基因在MTS(Mge1)过表达的背景下被上调,且全部依赖Pdr3(图四b),表明Pdr3是受MTS(Mge1)作用的主要转录激活因子,MTS(Mge1)-mCherry足以完整诱导mitoCPR的全部靶基因谱。
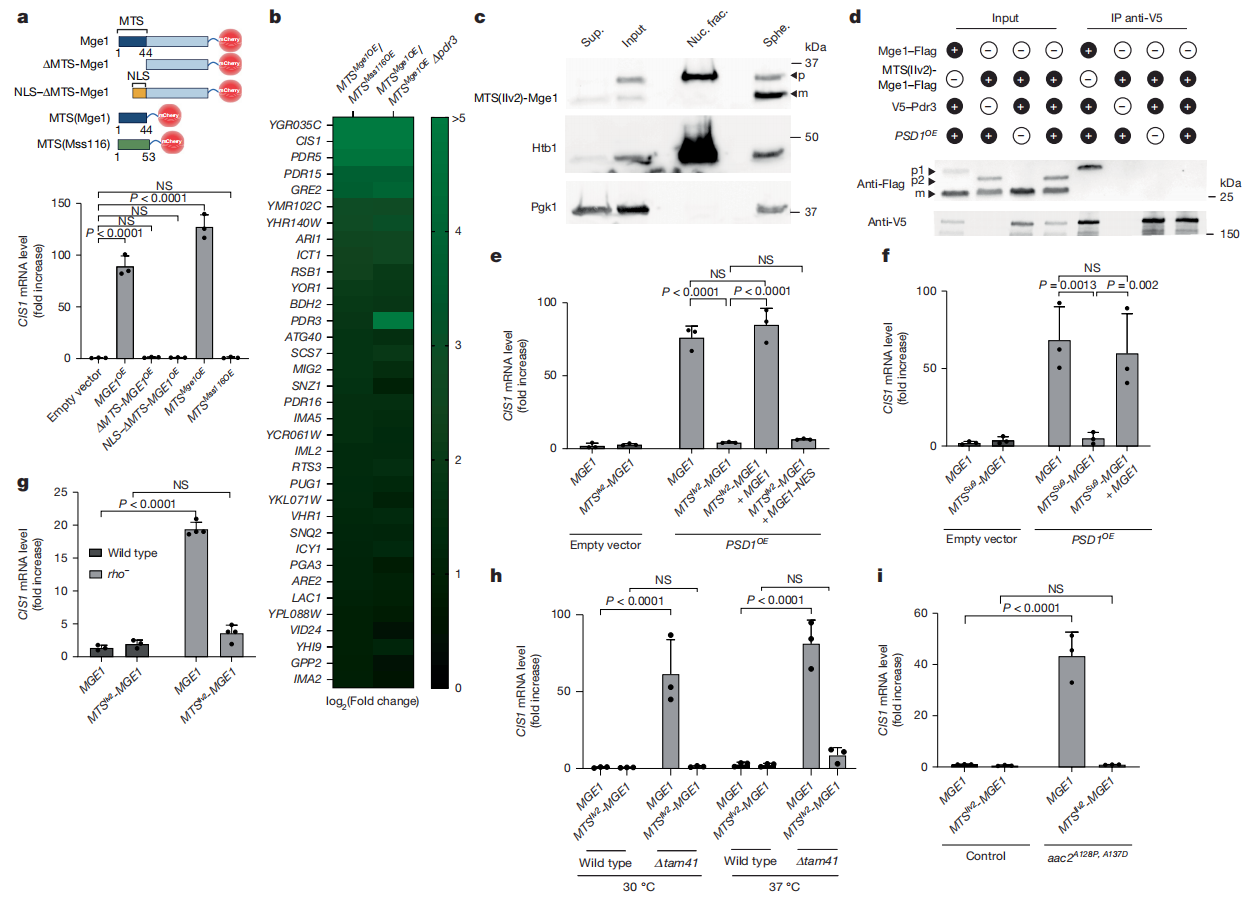
图四 Mge1的MTS在线粒体至细胞核信号传导中发挥作用[13]
研究者进一步在酵母基因组中敲除Mge1的MTS,并替换为粗糙脉孢菌ATP合酶亚基9(Su9)或来自Ilv2的MTS。结果显示,MTS(Ilv2)-Mge1可在分离的细胞核中被检测到(图四c),但不能与Pdr3相互作用,且在PSD1OE时也不能诱导CIS1表达(图四d和e)。在MTSSu9-Mge1细胞中,CIS1也没有显著上调(图四f);但重新引入野生型MGE1拷贝可恢复对蛋白质输入受损的应答反应(图四e和f);而补充表达出核信号MGE1或质膜锚定型MGE1的菌株在应激条件下均无法触发mitoCPR(图四e)。这些数据表明MTSIlv2-Mge1和MTSSu9-Mge1均可作为功能分离等位基因使用,它们能维持细胞存活,却无法介导Mge1依赖的mitoCPR激活。研究者又在多种模型中验证MTS的必要性,在rho-细胞模型、tam41∆细胞模型和aac2A128P, A137D模型[19]中,均获得一致结果(图四g-i)。以上数据表明,Mge1的MTS对于细胞响应急性和慢性线粒体蛋白输入缺陷的线粒体至细胞核信号传导至关重要。
最后,研究者分析Mge1 MTS的特性。进化保守性分析显示,Mge1 MTS序列保守性较低,其中前25个残基具有较高的同源性,提示该区域具有关键功能作用(图五a)。仅过表达N端前20个残基(MTSMge1(1–20)-mCherry)诱导的CIS1表达程度与全长MTS对照组相似(图五b)。进一步在MTSSu9-Mge1菌株中重新引入了由天然MGE1启动子驱动的MTSMge1-mCherry表达,能完全挽救PSD1诱导的CIS1上调;而MTSMge1(1–20)-mCherry也能部分恢复CIS1诱导,证实该短肽参与触发mitoCPR(图五c)。利用AlphaFold3结构建模预测了Mge1的N端可能与Pdr3相互作用,其N端17个残基会形成一个短螺旋结构,并与Pdr3调节性中间同源区内的一个带负电荷的口袋相结合,其第2位和第10位的精氨酸残基与Pdr3形成离子相互作用,其第4位苯丙氨酸则与Pdr3口袋中的一个空腔对齐,这可能有助于结合特异性(图五d)。研究者在全长MGE1中引入了这三个位点的点突变,并通过天然MGE1启动子表达相应突变体。在PSD1OE条件下,R2Q、R10Q和F4A三种突变体的前体形式均出现积累并定位于细胞核(图五e)。然而,与野生型Mge1不同,三种突变体均未能在MTSSu9-Mge1菌株中恢复mitoCPR的激活(图五f)。以上数据表明,Mge1的MTS序列包含了mitoCPR信号传导所必需的特征组合。
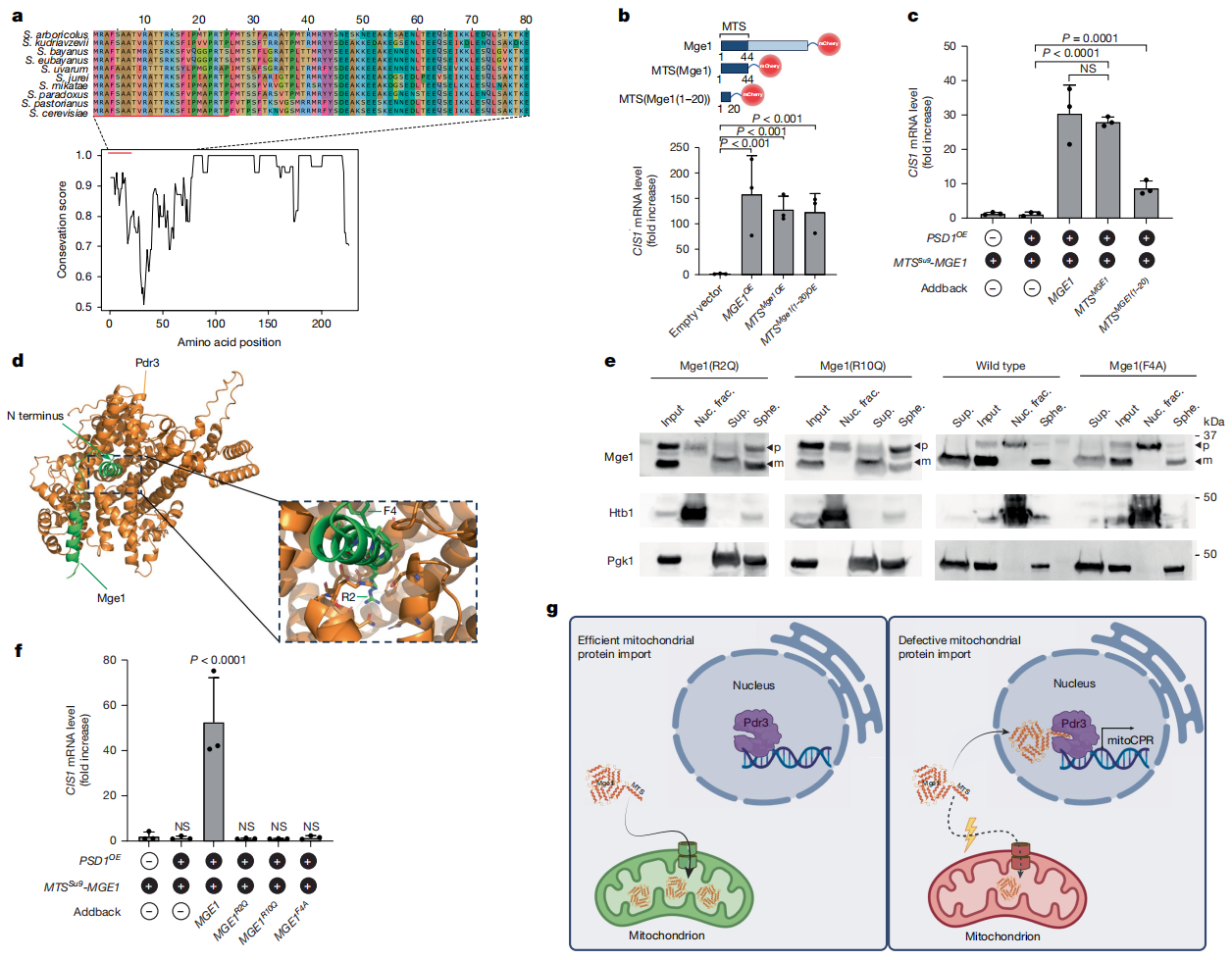
图五 Mge1 MTS的特定残基对于mitoCPR激活至关重要[13]
综上所述,该研究揭示了酵母线粒体Hsp70辅助伴侣蛋白Mge1是线粒体蛋白输入受损反应(mitoCPR)的核心调控因子。在基础状态下,Mge1的线粒体靶向序列(MTS)介导其进入线粒体,而当输入功能受损时,其前体蛋白则进入细胞核传递应激信号,这一信号传导作用依赖于Mge1的MTS结合并激活Pdr3(图五g)。该研究突破性阐明了信号传递的核心元件是Mge1自身的MTS,该序列不仅负责线粒体靶向,其N端约20个氨基酸构成的特定结构更是直接结合并激活Pdr3的充分必要条件。该研究首次提出并证实了MTS本身可作为一类灵活的信号模块,通过其核转位行为直接向细胞核报告线粒体的健康状态,为理解细胞器间通讯提供了全新范式,以及为相关线粒体疾病机制研究开辟了新的方向。

GTP研发中心负责实施基因组标签计划(Genome tagging project, GTP),基于自主知识产权的类精子干细胞介导半克隆技术,为全基因组的功能基因一一贴上标签,致力于构建标签细胞和标签小鼠资源库。类精子干细胞是从精子来源单倍体囊胚中建系获得的一种孤雄单倍体胚胎干细胞,将其注入卵母细胞,能够像精子一样支持整个胚胎发育过程,产生健康的半克隆小鼠。GTP研发中心在类精子干细胞的蛋白质编码基因上原位敲入标签序列,建立了液氮保存的标签细胞资源库。研究需要时,利用半克隆技术将标签细胞注射到小鼠卵母细胞中,一步法获得标签小鼠。

已有标签产品可直接订购,详情查阅以下官网链接。如有需要欢迎联系,我们将竭诚为您服务。
标签细胞网址:
标签小鼠网址:
http://www.sibcb.ac.cn/gtp/msearch.jsp
地址:上海市岳阳路320号
责任编辑:甜点
新媒体运营:suway
参考文献
1. Endo T, Wiedemann N: Molecular machineries and pathways of mitochondrial protein transport. Nat Rev Mol Cell Biol 2025, 26(11):848-867.
2. Nashed S, El Barbry H, Benchouaia M, Dijoux-Marechal A, Delaveau T, Ruiz-Gutierrez N, Gaulier L, Tribouillard-Tanvier D, Chevreux G, Le Crom S et al: Functional mapping of N-terminal residues in the yeast proteome uncovers novel determinants for mitochondrial protein import. PLoS Genet 2023, 19(8):e1010848.
3. Vogtle FN, Wortelkamp S, Zahedi RP, Becker D, Leidhold C, Gevaert K, Kellermann J, Voos W, Sickmann A, Pfanner N et al: Global analysis of the mitochondrial N-proteome identifies a processing peptidase critical for protein stability. Cell 2009, 139(2):428-439.
4. Craig EA: Hsp70 at the membrane: driving protein translocation. BMC Biol 2018, 16(1):11.
5. Pfanner N, den Brave F, Becker T: Mitochondrial protein import stress. Nat Cell Biol 2025, 27(2):188-201.
6. Boos F, Labbadia J, Herrmann JM: How the Mitoprotein-Induced Stress Response Safeguards the Cytosol: A Unified View. Trends Cell Biol 2020, 30(3):241-254.
7. Nowicka U, Chroscicki P, Stroobants K, Sladowska M, Turek M, Uszczynska-Ratajczak B, Kundra R, Goral T, Perni M, Dobson CM et al: Cytosolic aggregation of mitochondrial proteins disrupts cellular homeostasis by stimulating the aggregation of other proteins. Elife 2021, 10:e65484.
8. Balzarini M, Kim J, Weidberg H: Quality control of un-imported mitochondrial proteins at a glance. J Cell Sci 2025, 138(9):jcs263757.
9. Sutandy FXR, Gossner I, Tascher G, Munch C: A cytosolic surveillance mechanism activates the mitochondrial UPR. Nature 2023, 618(7966):849-854.
10. Hsu MC, Kinefuchi H, Lei L, Kikuchi R, Yamano K, Youle RJ: Mitochondrial YME1L1 governs unoccupied protein translocase channels. Nat Cell Biol 2025, 27(2):309-321.
11. Kim J, Goldstein M, Zecchel L, Ghorayeb R, Maxwell CA, Weidberg H: ATAD1 prevents clogging of TOM and damage caused by un-imported mitochondrial proteins. Cell Rep 2024, 43(8):114473.
12. Martensson CU, Priesnitz C, Song J, Ellenrieder L, Doan KN, Boos F, Floerchinger A, Zufall N, Oeljeklaus S, Warscheid B et al: Mitochondrial protein translocation-associated degradation. Nature 2019, 569(7758):679-683.
13. Yuan Z, Balzarini M, Volpe M, Goldstein M, Peng TS, Hui E, Fang NN, Albihlal WS, Hajimohammadi M, Wei K et al: A direct role for a mitochondrial targeting sequence in signalling stress. Nature 2026, 649(8099):1302-1311.
14. Kramer L, Dalheimer N, Raschle M, Storchova Z, Pielage J, Boos F, Herrmann JM: MitoStores: chaperone-controlled protein granules store mitochondrial precursors in the cytosol. EMBO J 2023, 42(7):e112309.
15. Shakya VP, Barbeau WA, Xiao T, Knutson CS, Schuler MH, Hughes AL: A nuclear-based quality control pathway for non-imported mitochondrial proteins. Elife 2021, 10.e61230
16. Westermann B, Prip-Buus C, Neupert W, Schwarz E: The role of the GrpE homologue, Mge1p, in mediating protein import and protein folding in mitochondria. EMBO J 1995, 14(14):3452-3460.
17. Nguyen Ba AN, Pogoutse A, Provart N, Moses AM: NLStradamus: a simple Hidden Markov Model for nuclear localization signal prediction. BMC Bioinformatics 2009, 10:202.
18. Veatch JR, McMurray MA, Nelson ZW, Gottschling DE: Mitochondrial dysfunction leads to nuclear genome instability via an iron-sulfur cluster defect. Cell 2009, 137(7):1247-1258.
19. Coyne LP, Wang X, Song J, de Jong E, Schneider K, Massa PT, Middleton FA, Becker T, Chen XJ: Mitochondrial protein import clogging as a mechanism of disease. Elife 2023, 12:e84330.
转载请注明来源于【GTP研发中心】
声明:本文仅用于分享,不代表GTP研发中心立场,若有侵权,请及时联系我们第一时间更正!



