技术分享:vCATCH技术实现共价药物的小鼠全身细胞靶点成像
药物分子的主要结合位点是决定药效与毒性的关键因素。尽管化学蛋白质组学、化学基因组学和热位移分析等分子靶点鉴定技术已革新了人们对药物作用机制的理解[1-3],但在空间与细胞分辨率层面上定位药物靶点的体内分布仍具挑战。目前,在生物系统内追踪药物的体内相互作用仍主要依赖放射性成像等低分辨率方法。荧光成像是实现药物靶点可视化的前景路径之一,该技术已广泛应用于DNA、mRNA和蛋白质等内源性生物分子的可视化。然而,将药物分子直接偶联荧光标记的方案并不可行,因为大尺寸的荧光标记物可能改变药物的体内活性及其分布。作为替代方案,近期开发了一种结合组织透明化与原位点击化学的CATCH技术,已实现药物分子在组织切片层面上的可视化[4]。但将CATCH技术从薄切片拓展应用至大体积、异质性的三维组织环境时,面临着严峻的挑战,存在探针在组织表面堆积、染色深度不均、大样本中心区域标记不足等问题[5-7]。因此,亟需开发能在组织区域甚至器官系统中以细胞分辨率可视化药物结合靶点的技术,以深入理解药物的在体作用机制,尤其针对共价抑制剂。
2026年2月,Cell期刊报道了一项研究,开发了一种体积透明化辅助组织点击化学(vCATCH)技术,实现了小鼠体内三维深度且均匀的原位点击标记。vCATCH只需简单被动的孵育步骤,在完整成年小鼠体内实现了细胞分辨率的药物结合成像。将其与水凝胶增强型HYBRiD透明化技术及虚拟现实技术相结合,对两种临床抗癌药物阿法替尼和伊布替尼的体内靶点进行了可视化与定量分析,不仅复现了已知的药物分布特征,更揭示了可能与脱靶效应相关的、此前未被报道的组织与细胞类型结合现象。vCATCH技术为在全生物体尺度上以前所未有的精度绘制共价药物作用图谱提供了一个无偏倚的研究平台[8]。
为实现深度组织抗体渗透,研究者借鉴了全脑与全身免疫染色技术,主要采用了两种策略:1) 增强探针如抗体向组织内的扩散能力;2) 在扩散阶段尽可能减少探针与靶标的相互作用如抗体-抗原结合,同时在染色阶段最大化反应效率,利用两个阶段反应速率的巨大差异防止探针在组织表面被耗竭,从而促进均质的组织标记[9]。于是,研究者采用类似策略实现三维深度点击反应。原位点击化学CATCH技术依赖于铜催化的叠氮-炔环加成反应(CuAAC),将靶标结合的药物分子与荧光信号相连接。CuAAC的反应动力学严格依赖于催化性Cu(I)-配体复合物。为便于操作,在扩散阶段通常使用Cu(II)化合物如CuSO₄,随后在结合阶段添加还原剂如抗坏血酸钠(NaAsb)生成Cu(I)。因此,通过暂缓添加还原剂NaAsb以阻止Cu(II)向Cu(I)的转化,理论上可在扩散与结合阶段之间实现探针-靶标反应速率的7至8个数量级增幅,从而显著提升CATCH技术在大体积组织中的渗透深度。
在开发阶段,研究者选用共价单胺氧化酶(MAO)抑制剂帕吉林,其炔烃标志物为帕吉林-炔基。在小鼠脑半球测试时,采用上述催化剂延迟策略,仅能实现N3-染料均质点击标记大脑表层至0.4毫米深度(图一A),且N3-染料扩散并非限制因素。已知铜离子与多种氨基酸侧链如半胱氨酸和组氨酸相结合[10],无处不在的铜结合位点可能使得Cu(II)向组织深处扩散时消耗游离铜离子,导致深层组织催化剂转化不足(图一B)。因此,研究者推测过量Cu(II)可用于预饱和潜在的铜结合位点,以增强深层组织的催化活性。重要的是,该策略不会增加非特异性标记或导致高背景。实验证实,加入10倍过量Cu的预反应铜饱和(PRCS)步骤后,在单次1小时反应中,标记深度提升至1毫米,且信噪比保持稳定(图一A-C)。虽然延长反应时间可能增加标记深度,但持续反应会耗尽缓冲液中的还原剂,最终可能导致活性氧(ROS)积累及副反应发生。因此改良为每小时更换点击反应混合液,并将该流程命名为重复迭代反应(RIR)。实验表明,PRCS结合两轮RIR即可实现小鼠脑半球全深度的均质CATCH标记(图一A-C),将此方法命名为体积CATCH(vCATCH)。
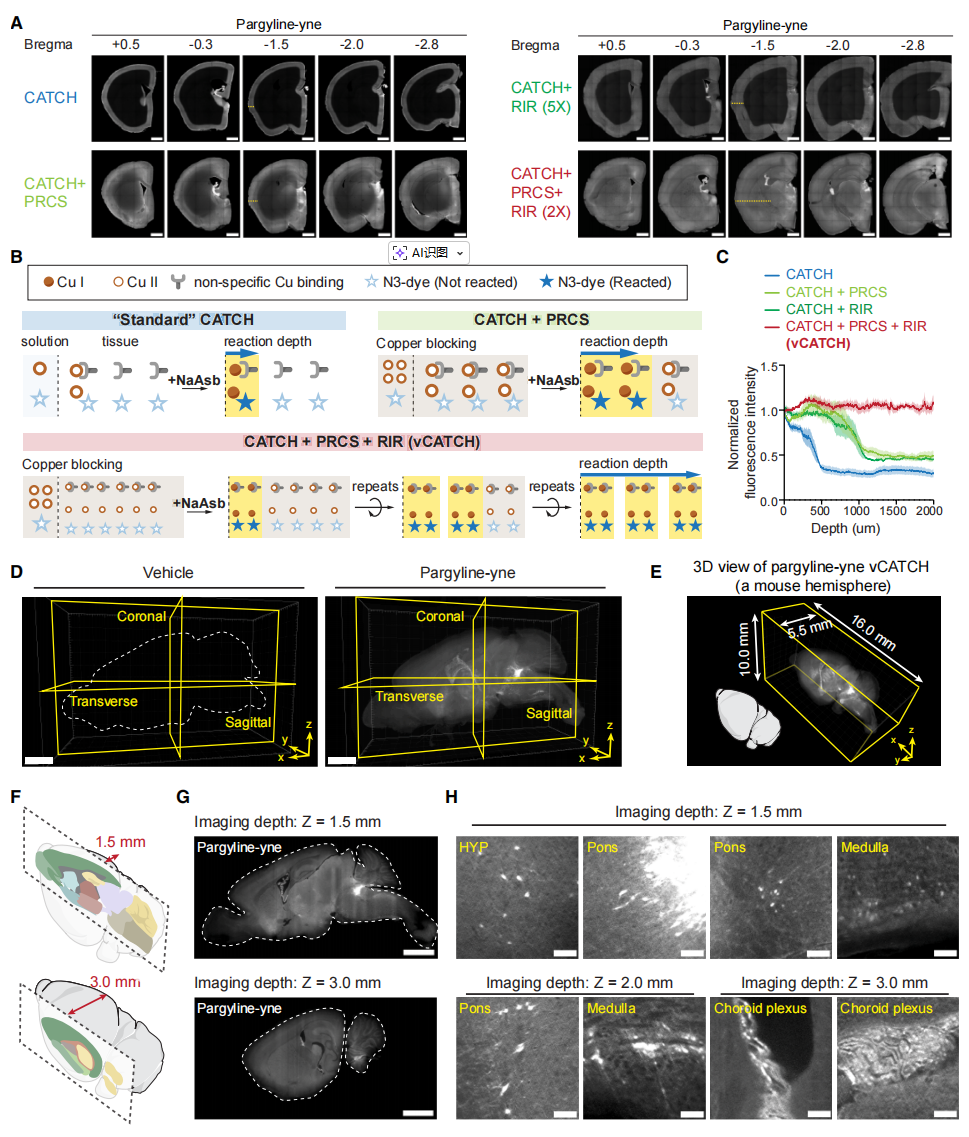
图一 vCATCH的改良开发[8]
在实现全脑标记后,研究者运用vCATCH技术对帕吉林的药物靶点进行无偏倚图谱绘制。通过在野生型小鼠腹腔注射帕吉林-炔基探针(10 mg/kg)或对照溶剂,HYBRiD技术透明化处理小鼠脑半球,随后进行为期1天的PRCS预处理与两轮RIR反应,最后通过光片荧光显微镜成像(图一D)。vCATCH技术支持高通量、平行化的被动处理流程,能够生成具有显著重复性的批量化帕吉林-炔基标记脑样本(图一E-H)。依据既往报道的脑区靶点信息对帕吉林-炔基探针在大脑中的结合情况进行人工验证[4]。这些区域包括脑桥和下丘脑(HYP)中独特的细胞结构(图一H)。此外,在脉络丛(脑室)和延髓中发现帕吉林-炔基探针富集的细胞(图一H),并在中脑观察到更多神经元样结构。以上数据表明,vCATCH技术在大体积组织及全脑范围内均保持高保真度。
采用最新开发的基于人工智能的集合图谱(ACE)流程[11] 分析这些数据集(图二A-C)。将三维体积数据配准至艾伦脑图谱(ABA)[12]后,首先量化了全脑各区域的荧光强度,反映药物结合丰度(图二B)。强度定量结果显示药物在脑桥、丘脑和中脑等区域呈现高丰度分布,例如蓝斑核(LC)和伏隔核(ACB)等特定核团(图二D)。借助vCATCH技术提供的细胞分辨率成像能力,进一步对帕吉林的细胞靶点进行无偏倚定量分析。基于大规模训练数据集和人工智能分割算法,通过ACE流程在全脑范围内识别帕吉林-炔基探针阳性细胞(图二C)。分割结果显示,细胞密度分布模式与荧光强度谱基本吻合。无偏倚的ACE分析还揭示了荧光强度与细胞计数之间的意外差异。例如,在伏隔核(ACB)、终纹床核(BST)和背侧丘脑内侧群(MED)等区域虽显示出广泛的药物强度信号,却几乎未检测到神经元结构,提示药物结合可能与非胞体结构相关(图二D和E)。相反,在中缝背核(DR)和脑桥被盖前核(AT)等区域,尽管整体荧光强度未见提升,却鉴定出帕吉林亲和靶点MAO-B染色阳性的药物结合细胞(图二D和E),表明帕吉林在这些区域靶向的是稀疏分布的神经元群体。以上数据表明,vCATCH技术可与组织透明化方法及高通量计算流程兼容,实现对共价药物在小鼠大脑中区域富集与细胞靶点的无偏倚定量分析。
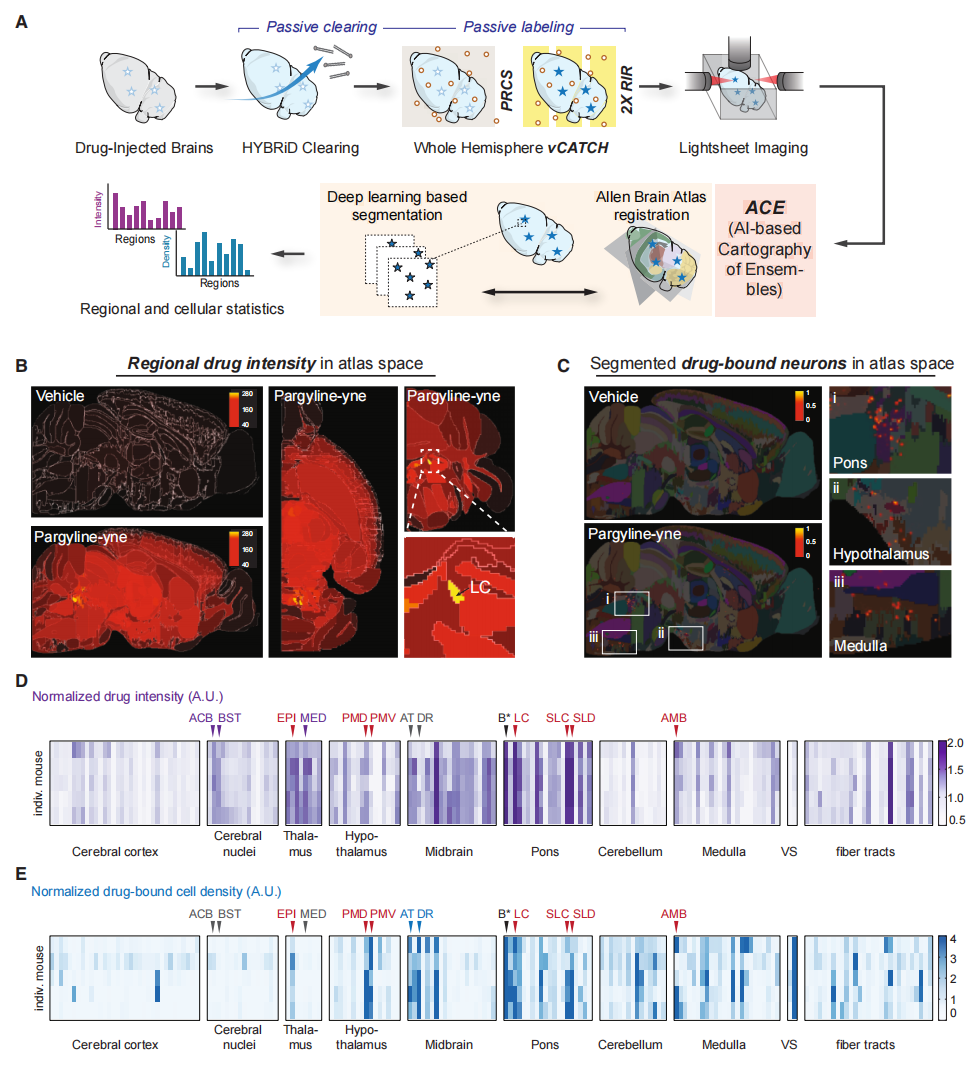
图二 全脑半球帕吉林-炔基靶点的ACE分析[8]
接下来,研究者将vCATCH靶点图谱技术拓展至完整动物体。选取两种广泛应用的非共价靶向激酶抑制剂(TKI)阿法替尼和伊布替尼。向野生型小鼠腹腔注射10 mg/kg已建立的伊布替尼-炔基探针或阿法替尼-炔基探针,这些探针基本保留了原药的药代动力学特性和组织分布特征。通过为期4天的PRCS预处理及5轮RIR反应的vCATCH方案,成功在经HYBRiD透明化处理的1周龄小鼠中实现全身均质标记,总体积超过38×18×12 mm(图三A-D),随后进行光片成像(图三A-H)。将其拓展至成年个体。通过优化为7天PRCS预处理和8轮RIR反应,在总体积达70×30×20 mm的成年小鼠体内成功完成伊布替尼-炔基探针标记(图三A)。该整体体积超出了多数商业光片系统的视野范围,研究者聚焦于躯干中心区域(37×30×8 mm;图三I),系统检测了主要器官的药物分布特征(图三J-M)。从全局分布来看,两种靶向激酶抑制剂在肝脏和胃肠道中的结合均呈现高度富集(图三F和K)。
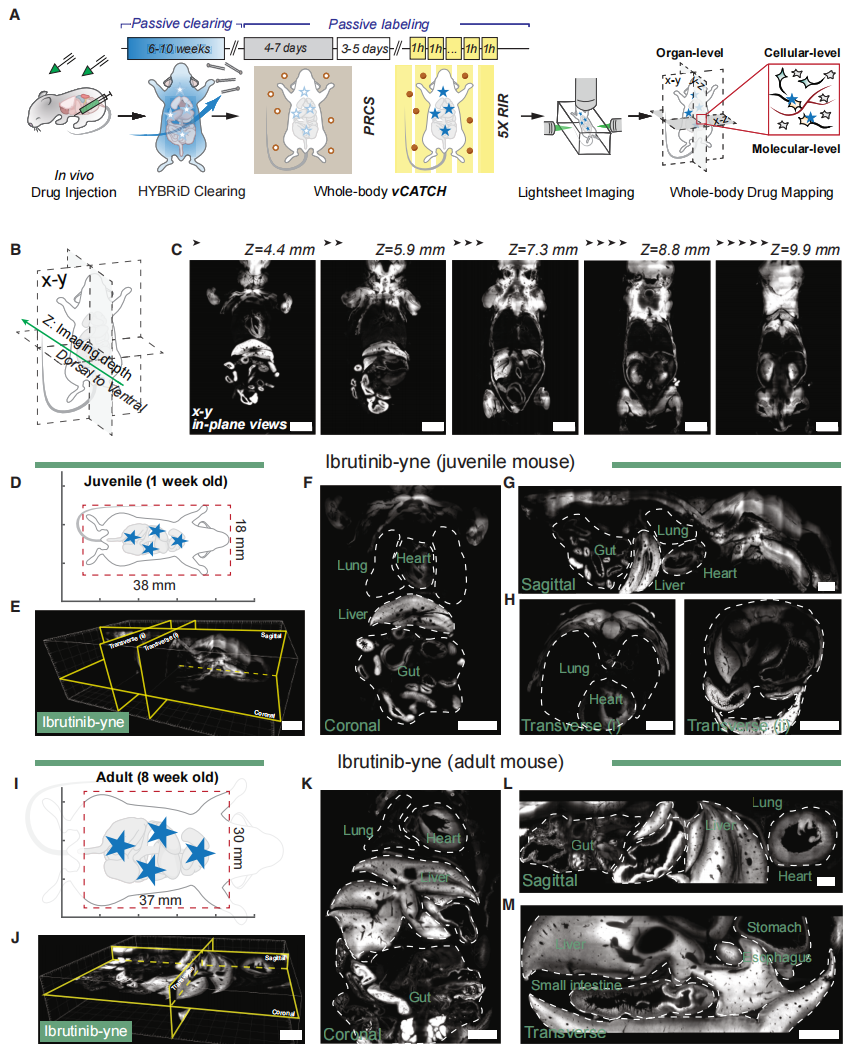
图三 vCATCH以高空间分辨率揭示全身TKI分布情况[8]
在上胸部区域,伊布替尼在心脏的结合水平显著高于肺部,而阿法替尼则呈现相反的富集模式(图四A、F和K)。在其他器官中,观察到这两种药物呈现截然不同的靶点分布模式。例如,伊布替尼在胃内壁黏膜及鼻腔通道呈现显著的组织富集,而阿法替尼则未显示此类特征。此外,发现阿法替尼在肺部存在广泛分布的靶点,而伊布替尼的肺内标记仅局限于支气管周围区域(图四B、C、G、H、L和M)。两种TKI均在肝脏富集(图四D、I和N),这与文献报道一致。但更高分辨率的vCATCH成像揭示了它们在器官内分布的差异:阿法替尼在整个肝组织中呈现冠状信号分布,而伊布替尼则与稀疏散布的单个细胞相关(图四E、J和O)。
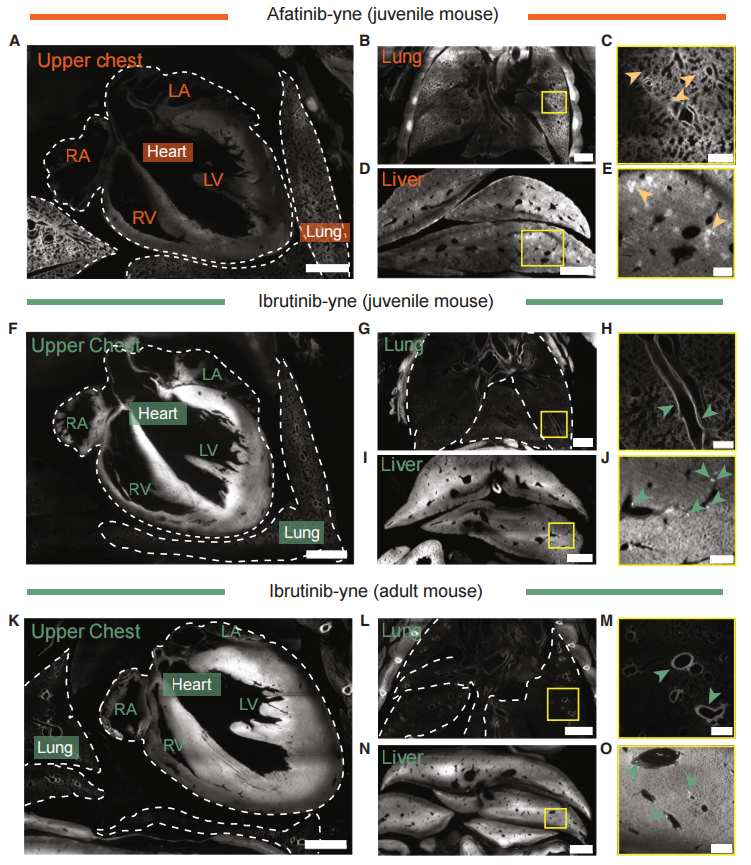
图四 vCATCH揭示器官内部TKI分布情况[8]
使用更高放大倍率的共聚焦成像进一步揭示各器官中两种TKI药物结合的精细结构(图五A-F)。值得注意的是,两种药物在骨骼中均与环状结构紧密结合(图五A和D),该现象在脾脏中亦有发现。在药物分布模式的引导下,进一步对药物靶向细胞进行分子特征解析。基于经典的靶向作用机制[13],聚焦于阿法替尼在肺部的结合以及伊布替尼在脾脏的结合。正如预期,免疫染色结果显示阿法替尼-炔基探针与伊布替尼-炔基探针信号分别主要位于EGFR阳性与BTK阳性细胞上(图五G和H)。关键的是,用各探针的母体化合物预处理动物能显著降低探针标记信号(图五G-J),进一步验证了这些探针的特异性。在肝脏中,观察到两种探针呈现出富集但截然不同的结合模式(图五C和F),随后通过分子分析确定各探针的靶向细胞类型。首先,与肝细胞中EGFR高表达的特征一致,发现阿法替尼结合的细胞中大部分(59.17% ± 10.91%)为肝细胞,其余小部分为巨噬细胞(F4/80阳性)和T细胞(CD3e阳性)(图五K-M)。与之形成对比,伊布替尼结合的细胞中仅小部分(13.95% ± 1.32%)为肝细胞,而较大比例(39.53% ± 4.42%)为F4/80阳性巨噬细胞(图五N-P),这与肝脏巨噬细胞中已知的BTK表达特征相符。值得注意的是,尽管T细胞的BTK表达水平较低,但伊布替尼结合细胞中最大群体(52.78% ± 3.25%)为CD3e阳性T细胞(图五O),提示可能存在非BTK靶点参与作用。以上数据表明,vCATCH数据显示两种TKI在单个组织与器官中富集于不同的细胞类型,彰显了vCATCH技术在全局、器官、组织及细胞尺度上解析药物靶点的强大能力。
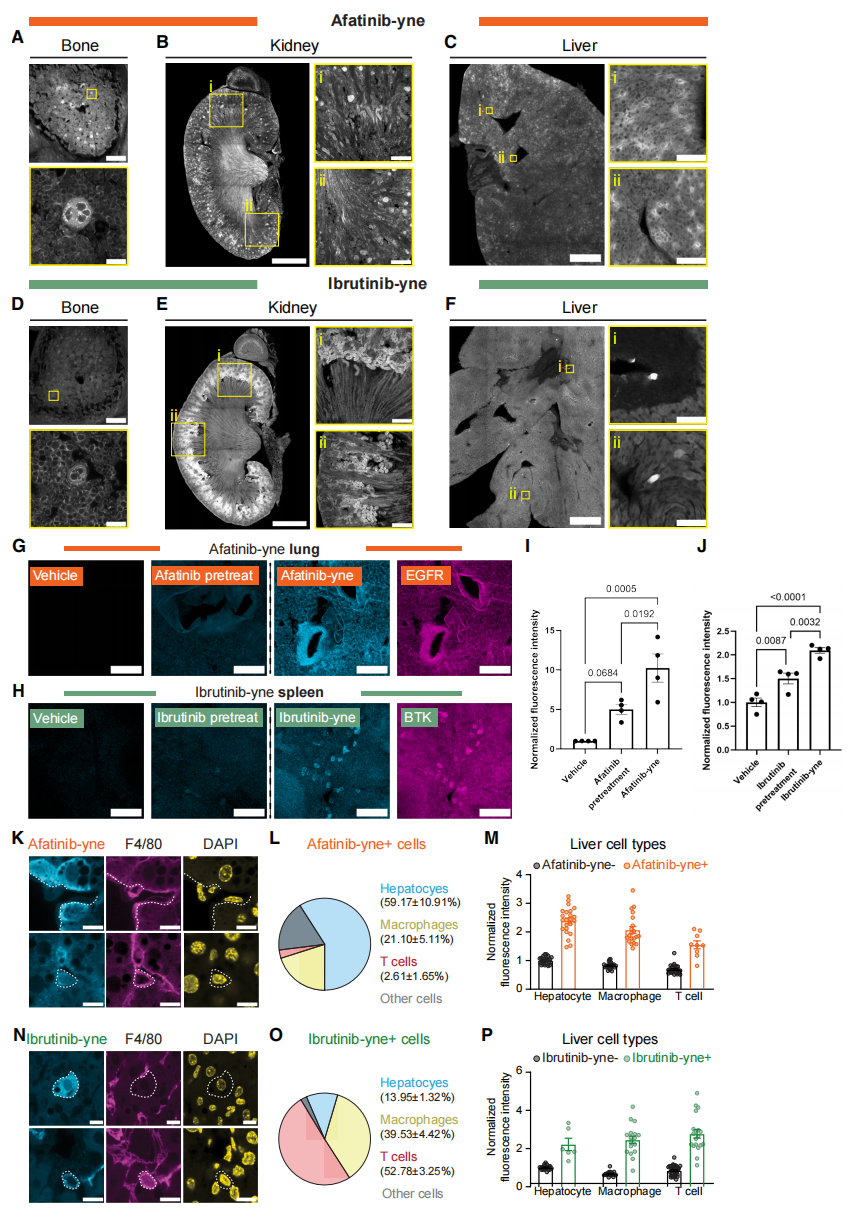
图五 药物富集组织中TKI作用的细胞类型解析[8]
综上所述,该研究通过采用预反应铜饱和(PRCS)与重复迭代反应(RIR)策略,充分发挥点击化学的独特优势,建立了体积透明化辅助组织点击化学(vCATCH)技术。通过将vCATCH与水凝胶增强型HYBRiD透明化技术结合,实现了共价药物在小鼠全身的细胞靶点成像。除复现已知的药物分布特征以外,还揭示了可能与脱靶效应相关的、此前未被报道的结合细胞类型。vCATCH技术为全生物体尺度上在体亚器官空间分辨率的药代动力学研究,特别是靶向药物在肿瘤、正常组织细胞的分布可视化提供了一个全新平台,有望深入理解药物的在体结合靶标及其作用机制,助力药物开发及其安全性验证流程。

GTP研发中心负责实施基因组标签计划(Genome tagging project, GTP),基于自主知识产权的类精子干细胞介导半克隆技术,为全基因组的功能基因一一贴上标签,致力于构建标签细胞和标签小鼠资源库。类精子干细胞是从精子来源单倍体囊胚中建系获得的一种孤雄单倍体胚胎干细胞,将其注入卵母细胞,能够像精子一样支持整个胚胎发育过程,产生健康的半克隆小鼠。GTP研发中心在类精子干细胞的蛋白质编码基因上原位敲入标签序列,建立了液氮保存的标签细胞资源库。研究需要时,利用半克隆技术将标签细胞注射到小鼠卵母细胞中,一步法获得标签小鼠。

已有标签产品可直接订购,详情查阅以下官网链接。如有需要欢迎联系,我们将竭诚为您服务。
标签细胞网址:
标签小鼠网址:
http://www.sibcb.ac.cn/gtp/msearch.jsp
地址:上海市岳阳路320号
责任编辑:多一百
新媒体运营:suway
参考文献
1. Offensperger F, Tin G, Duran-Frigola M, Hahn E, Dobner S, Ende CWA, Strohbach JW, Rukavina A, Brennsteiner V, Ogilvie Ket al: Large-scale chemoproteomics expedites ligand discovery and predicts ligand behavior in cells. Science 2024, 384(6694):eadk5864.
2. Li H, Ma T, Remsberg JR, Won SJ, DeMeester KE, Njomen E, Ogasawara D, Zhao KT, Huang TP, Lu Bet al: Assigning functionality to cysteines by base editing of cancer dependency genes. Nature chemical biology 2023, 19(11):1320-1330.
3. Ji H, Lu X, Zhao S, Wang Q, Liao B, Bauer LG, Huber KVM, Luo R, Tian R, Tan CSH: Target deconvolution with matrix-augmented pooling strategy reveals cell-specific drug-protein interactions. Cell chemical biology 2023, 30(11):1478-1487.e1477.
4. Pang Z, Schafroth MA, Ogasawara D, Wang Y, Nudell V, Lal NK, Yang D, Wang K, Herbst DM, Ha Jet al: In situ identification of cellular drug targets in mammalian tissue. Cell 2022, 185(10):1793-1805.e1717.
5. Sylwestrak EL, Rajasethupathy P, Wright MA, Jaffe A, Deisseroth K: Multiplexed Intact-Tissue Transcriptional Analysis at Cellular Resolution. Cell 2016, 164(4):792-804.
6. Murray E, Cho JH, Goodwin D, Ku T, Swaney J, Kim SY, Choi H, Park YG, Park JY, Hubbert Aet al: Simple, Scalable Proteomic Imaging for High-Dimensional Profiling of Intact Systems. Cell 2015, 163(6):1500-1514.
7. Tyler DS, Vappiani J, Cañeque T, Lam EYN, Ward A, Gilan O, Chan YC, Hienzsch A, Rutkowska A, Werner Tet al: Click chemistry enables preclinical evaluation of targeted epigenetic therapies. Science 2017, 356(6345):1397-1401.
8. Pang Z, Leung VH, Wang CC, Attarpour A, Rinaldi A, Shen H, Moya-Garzon MD, Sigua LH, Rammel C, Selke Aet al: Mapping cellular targets of covalent cancer drugs in the entire mammalian body. Cell 2026, 189(3):725-738.e715.
9. Susaki EA, Shimizu C, Kuno A, Tainaka K, Li X, Nishi K, Morishima K, Ono H, Ode KL, Saeki Yet al: Versatile whole-organ/body staining and imaging based on electrolyte-gel properties of biological tissues. Nature communications 2020, 11(1):1982.
10. Festa RA, Thiele DJ: Copper: an essential metal in biology. Current biology : CB 2011, 21(21):R877-883.
11. Attarpour A, Osmann J, Rinaldi A, Qi T, Lal N, Patel S, Rozak M, Yu F, Cho N, Squair Jet al: A deep learning pipeline for three-dimensional brain-wide mapping of local neuronal ensembles in teravoxel light-sheet microscopy. Nature methods 2025, 22(3):600-611.
12. Wang Q, Ding SL, Li Y, Royall J, Feng D, Lesnar P, Graddis N, Naeemi M, Facer B, Ho Aet al: The Allen Mouse Brain Common Coordinate Framework: A 3D Reference Atlas. Cell 2020, 181(4):936-953.e920.
13. Alam O: A single-cell-type transcriptomics map of human tissues. Nature genetics 2021, 53(9):1275.



