技术分享:活细胞沉默线粒体基因表达
线粒体在细胞代谢和能量生成中扮演着核心角色。人类线粒体DNA(mtDNA)编码2种rRNA、22种tRNA以及11种mRNA,其中2种为双顺反子,即13种蛋白质是由线粒体编码的[1]。线粒体mRNA的翻译过程发生在膜结合核糖体上,这些核糖体通过与OXA1L插入酶协作,促进翻译产物插入线粒体内膜[2]。线粒体编码蛋白质的合成缺陷与多种严重的人类疾病相关。然而,线粒体编码基因表达机制的核心问题仍未阐明。例如:尚不清楚线粒体基因与核基因的表达是如何相互协调,如何将双遗传来源的亚基组装成氧化磷酸化系统(OXPHOS)的酶复合体[3]。尽管已有体外重建线粒体翻译的初步尝试,以及通过核糖体图谱分析其动态,人们对协调线粒体基因表达并引导mRNA进行翻译的蛋白质仍知之甚少[4, 5]。与核DNA不同,mtDNA无法通过CRISPR进行基因编辑,因为将RNA导入线粒体的方法尚未建立[6, 7]。近年来,利用细菌胞苷脱氨酶实现了mtDNA的靶向基因编辑[8]。然而,目前仍缺乏活细胞简单操作、选择性沉默线粒体蛋白质表达的技术方法。
2025年7月,Science期刊报道了一项研究,开发了一种选择性沉默活细胞特定线粒体mRNA的方法。具体而言,研究者构建了由线粒体前序列肽和吗啉寡核苷酸(morpholino,MO)组成的嵌合体,前者靶向线粒体,后者靶向敲降的特定线粒体mRNA。将嵌合体转染入细胞后,可从细胞质运输到线粒体,与靶向线粒体mRNA结合并阻断翻译。该方法能有效地选择性靶向沉默活细胞中单个线粒体mRNA,也能同时靶向多个线粒体mRNA,并且适用于多种细胞类型。基于该方法,研究者监测了线粒体mRNA沉默后线粒体蛋白质组的动力学变化及其对核基因表达的影响,为理解线粒体生物合成和基因表达,线粒体基因组-核基因组通讯提供了全新见解[9]。
研究者之前构建了一种沉默线粒体基因表达系统[10],利用线粒体前体蛋白将MO带入线粒体基质。然而,这种方法的应用范围有限,需要在体外分离的线粒体中进行导入和随后的基因表达分析,无法在活细胞内进行敲降。因此,研究者设计了一种替代嵌合体,将线粒体靶向模块换成前序列肽,以直接靶向活细胞线粒体。在测试了各种前序列肽后,筛选出酿酒酵母的Cox4前序列肽(pCox41-25),通过点击化学反应将pCox4-N3与环辛炔修饰的MO连接起来,合成出嵌合体。选择敲降线粒体COX1来比较2种嵌合体,并通过[35S]甲硫氨酸标记线粒体翻译产物来监测翻译。发现将2种嵌合体导入纯化的线粒体,都能显著且特异性减少线粒体中COX1的翻译,但pCox4-COX11-19嵌合体的效率是之前版本Jac1-COX11-19[10]的五倍(图一A-C)。进一步测试靶向其他人类线粒体mRNA(ND6除外)的嵌合体,在纯化的线粒体中显示出类似的翻译阻断活性,还有效阻断了双顺反子ATP8/ATP6(图一D和E)、CYTB和ND2(图一F和G)mRNA的翻译。为评估pCox4前序列肽是否可以并行靶向多个mRNA,将针对不同mRNA的多种嵌合体组合导入纯化的线粒体,结果显示可以同时特异性沉默三种不同的线粒体mRNA(图一H)。已知MO通过阻断mRNA与核糖体的相互作用来抑制翻译,为了阐明它们在线粒体中的作用机制,研究者评估了靶向COX1 mRNA 5′ 区不同位置的多个嵌合体的敲降能力。只有当嵌合体靶向1-42区域时,才能在分离线粒体中观察到有效沉默(图一I)。通过mL45FLAG分离线粒体核糖体,并通过nanoString评估洗脱液中的转录本时,仅有靶向COX11-19和COX119-42嵌合体处理后,COX1 mRNA与核糖体的结合特异性减少,而用靶向该区域下游mRNA的嵌合体处理时则没有(图一J)。以上数据表明,由Cox4前序列肽和靶向线粒体mRNA的MO组成的嵌合体(pCox4-MO)通过抑制核糖体-mRNA相互作用有效地阻断翻译(图一K)。
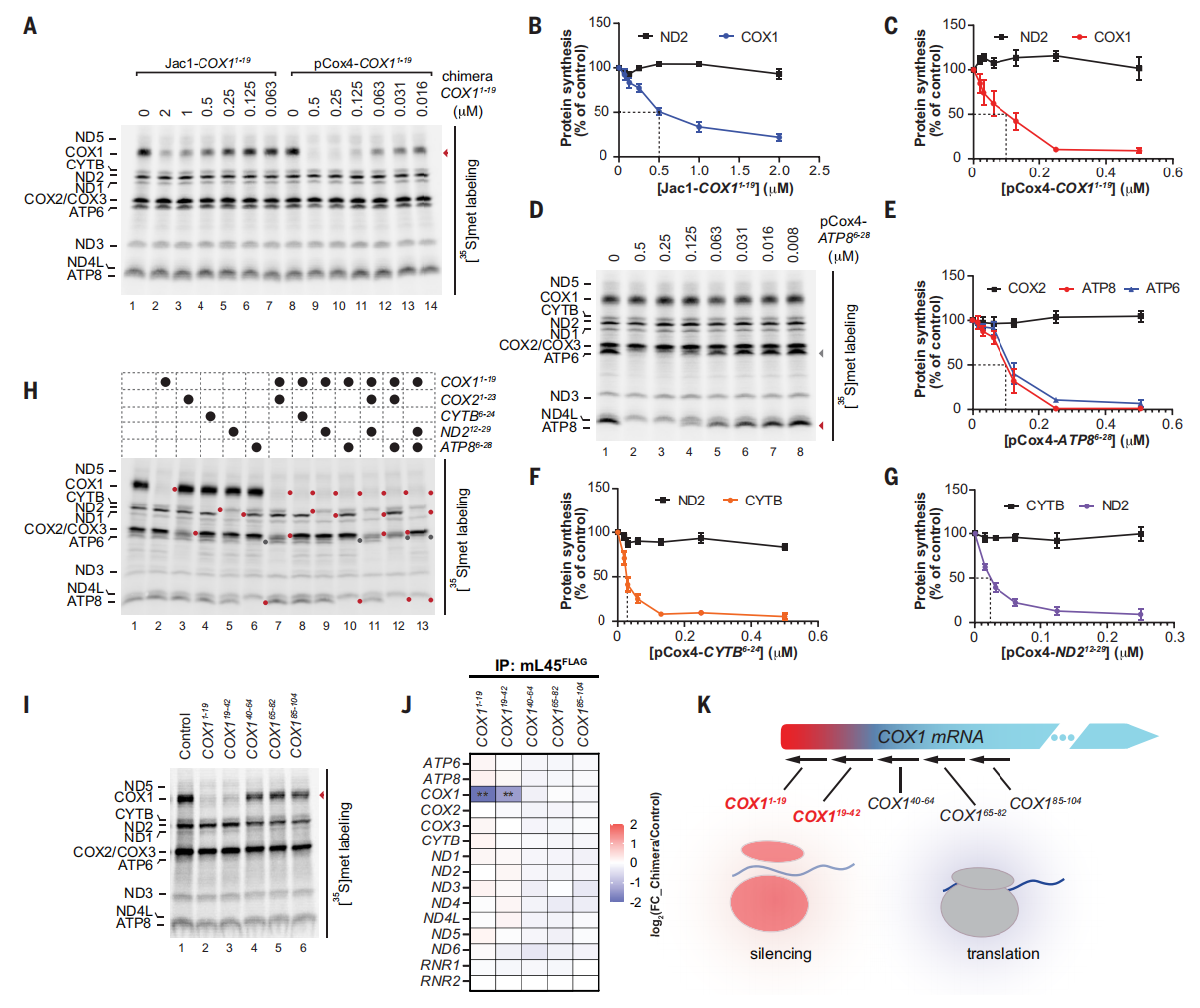
图一 pCox4-MO嵌合体高效沉默分离线粒体的基因表达[9]
接下来,研究者测试pCox4-MO嵌合体敲降哺乳动物活细胞线粒体基因表达的能力。转染后24、48和72小时,pCox4-COX11-19嵌合体有效抑制了HEK293T细胞的COX1合成,COX1蛋白水平随剂量增加和时间推移而逐步降低,72小时敲降效果最佳(图二A),且mtDNA丰度不受影响。转染3小时后,COX1翻译抑制已经很明显(图二B)。在活细胞中靶向不同COX1 mRNA 5′ 区的沉默效应与分离线粒体中观察到的模式相似(图二C)。研究者还构建了针对OXPHOS复合物I(ND1-5)、III(CYTB)、IV(COX1-3)和V(ATP6和ATP8)亚基mRNA的嵌合体。细胞转染24小时后,所有嵌合体都阻断了对应的翻译(图二D)。此外,通过共转染两种嵌合体,可实现特异性阻断双重目标mRNA的翻译过程(图二E)。靶向COX1、COX2和CYTB mRNA的5′ 区导致mRNA与线粒体核糖体的结合特异性减少(图二F)。进一步将嵌合体分别转染到人诱导多能干细胞(iPS)衍生的心肌细胞(图二G)和小鼠肝细胞(图二H)中,发现所有测试的嵌合体都被有效地转染到细胞中,并阻断线粒体mRNA的翻译。以上数据表明,将pCox4-MO嵌合体转染到多种细胞中,均能高效沉默活细胞线粒体编码基因的表达。
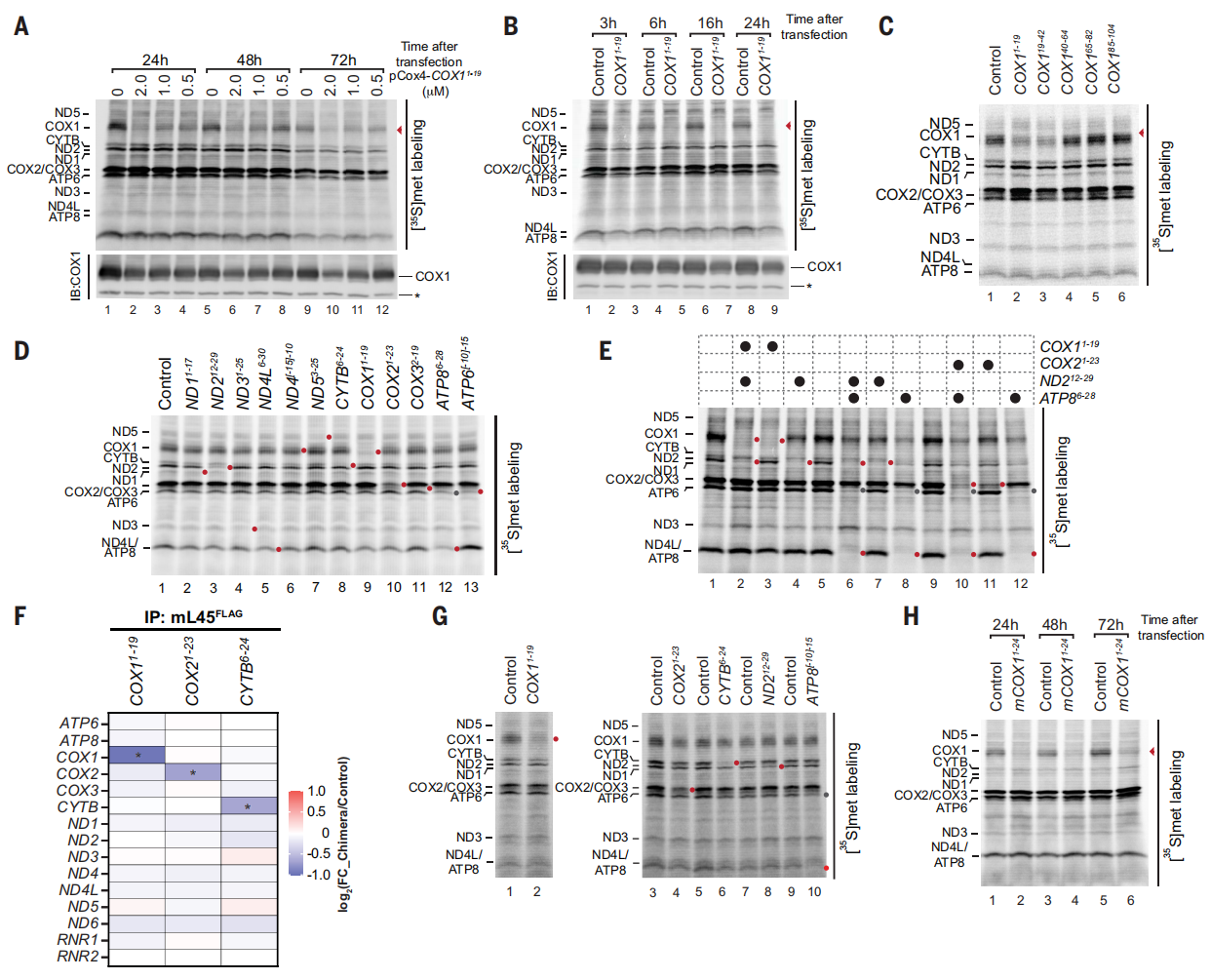
图二 pCox4-MO嵌合体高效沉默活细胞线粒体编码基因的表达[9]
随后,研究者监测COX1沉默后的线粒体mRNA水平。用嵌合体处理后,COX1转录水平迅速下降,相比之下,其他转录本在最初的48小时内没有受到实质性影响,但在沉默72小时后开始显示出轻微的减少(图三A)。在测试的转录本和嵌合体中,COX1 mRNA降低效果很显著,同样靶向mRNA中间区域的COX1181-199嵌合体没有敲降效果(图三B)。利用活细胞沉默线粒体基因表达可探究线粒体翻译与细胞生理的整合机制。于是,研究者分别靶向线粒体复合物I(ND1、ND2、ND3、ND4L、ND5)、复合物III(CYTB)、复合物IV(COX1、COX2、COX3)和复合物V(ATP6、ATP8)亚基(图三C),48小时后通过mRNA测序监测核基因组的表达变化,发现不同处理组间mRNA丰度模式呈现显著差异(图三D)。此外,敲降某些线粒体基因如ND1、ND4L、CYTB和COX2引发了更广泛的细胞反应(图三E)。采用UpSet可视化方法分析了各条件下所有显著变化转录本的排他性交集子集,显示在敲降ND1、ND4L、ND5、CYTB、COX2或COX3的处理中,主要交集均来自各自独有的特异性变化转录本。但也观察到不同处理间存在共同反应,如ND1_COX2、COX2_CYTB组合(图三F)。
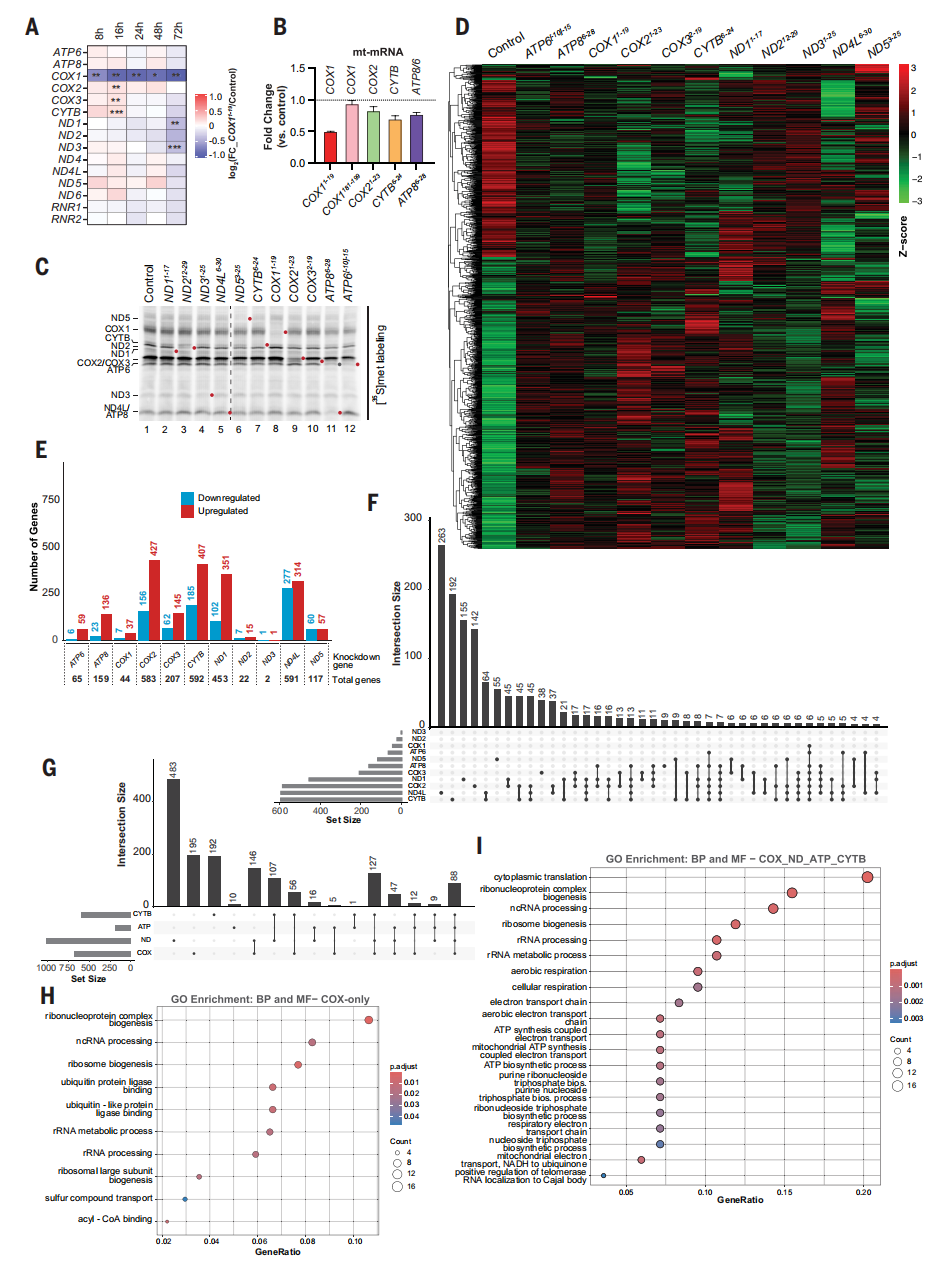
图三 活细胞沉默线粒体编码基因会改变RNA丰度[9]
为降低数据维度并聚焦全局变化,研究者将OXPHOS复合物亚基沉默后发生改变的mRNA并集归类为ND组(复合物I)、CYTB组(复合物III)、COX组(复合物IV)和ATP组(复合物V),分析各组转录本的排他性交集情况。与单基因处理数据结果一致(图三F),最具代表性的子集为ND组、COX组和CYTB组独有子集,分别包含483、195和192个基因(图三G)。进一步对生物过程与分子功能进行GO富集分析,显示尽管COX组与ND组独有子集的富集通路相似,但所涉基因并不相同,也观察到各自特有的通路富集特征(图三H)。在排他性交集中,有127个转录本在电子传递链复合物对应组中特异性变化,以及88个转录本在所有四组中均发生变化(图三G),四组共性差异基因主要参与细胞质与线粒体翻译、细胞呼吸过程(图三I)。以上数据表明,线粒体-细胞核通讯呈现与靶向线粒体mRNA相关的特定模式,且核基因表达响应显示出比以往认知更具层级性的调控特征[11, 12],敲降不同OXPHOS复合物亚基或同一复合物内不同核心组分,对细胞基因表达谱的影响也具有差异性。
最后,研究者评估了沉默线粒体基因对细胞器的影响。在HEK293T细胞中分别转染靶向ND2(复合物I)、CYTB(复合物III)、COX1(复合物IV)和ATP8(复合物V)的嵌合体,48小时后监测OXPHOS复合物活性。结果显示,敲降ND2、CYTB、COX1和ATP8分别导致对应复合物活性显著且选择性下降(图四A-D)。蓝色天然聚丙烯酰胺凝胶电泳结果显示,敲降ND2与CYTB分别降低了复合物I和III水平,并改变CI-CIII超复合物的组装状态,敲降COX1引起了复合物IV减少,敲降ATP8导致复合物V减少并出现游离的F1结构域,所有处理条件下复合物II水平均未受影响(图四E)。这些发现进一步得到蛋白质组学分析的支持:嵌合体处理48小时后,敲降ND2特异性降低复合物I(图四F),敲降CYTB特异性降低复合物III(图四G)。尽管延长COX1沉默不会间接影响其他线粒体编码蛋白质的合成(图二A),但在用pCox4-COX11-19嵌合体处理72小时后,观察到复合物IV的选择性大量损失(图四H)。相应地,实时呼吸测量显示嵌合体处理样本中O2消耗率显著降低(图四I-K)。OXPHOS能力的丧失导致细胞代谢转变为糖酵解代谢(图四L)。然而,线粒体膜电位仍然保持不变(图四M)。进一步在HEK293T细胞中的沉默COX1表达8、16、24、48和72小时,分离线粒体进行定量质谱分析。COX1沉默8小时后,仅有少数线粒体蛋白的丰度发生了变化,其中ZNF703和PNKD变化最大(图四N)。随着沉默时间的延长,线粒体蛋白质组变化的数量随之增加,丰度也发生了变化(图四N)。复合物IV亚基的蛋白量随时间逐渐减少,而对其他OXPHOS复合物影响不大(图四O)。以上数据表明,敲降线粒体基因表达会导致线粒体蛋白质组发生高度特异性改变,且这种变化可在数小时至数天的时间尺度内被监测,事件发生的时序规律为:COX1的沉默首先影响COX1模块蛋白、复合物IV组装因子、COX2和COX3模块,随后通过双功能组装因子如COA3、TMEM186等将效应传递至其他OXPHOS复合物(图四P)。
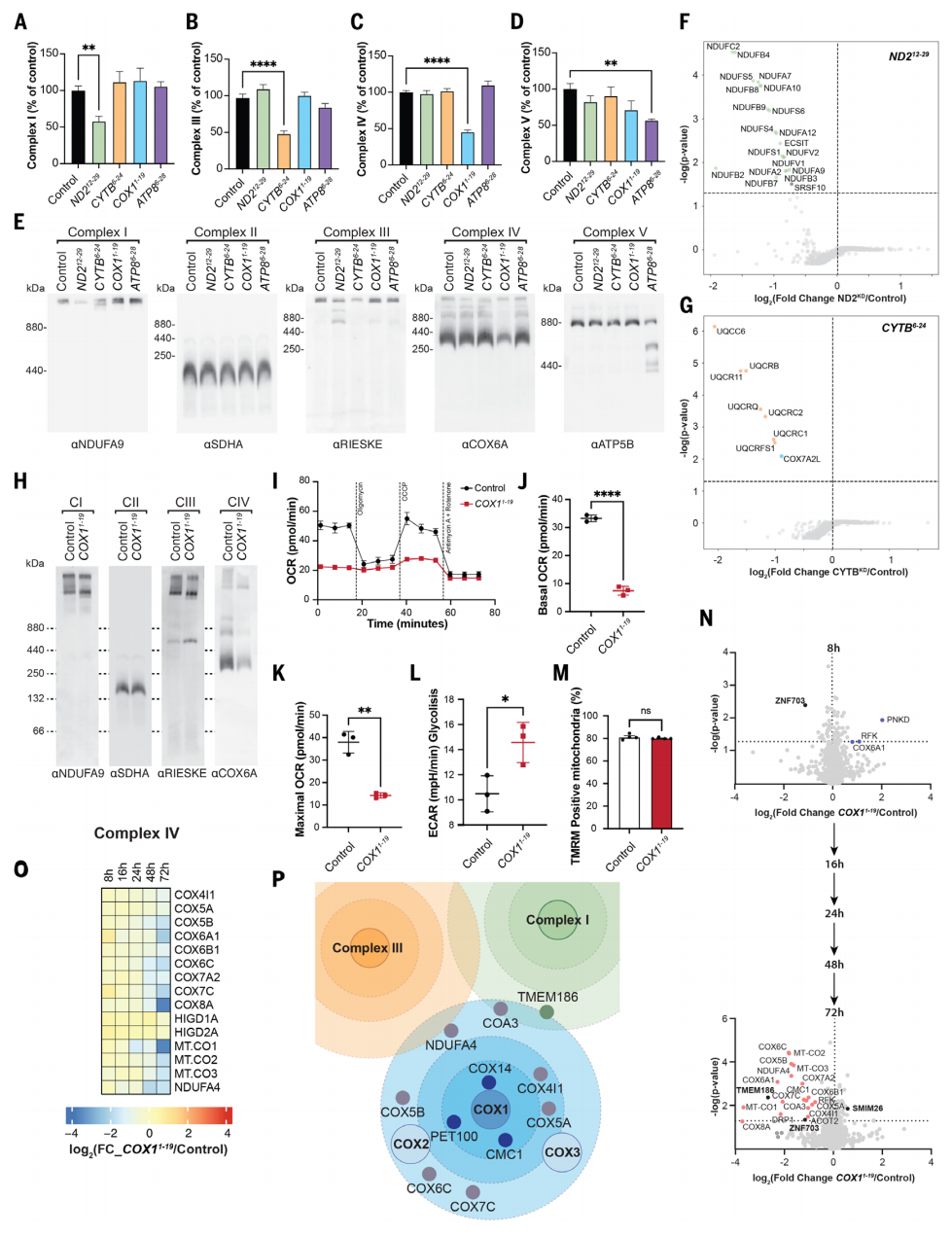
图四 活细胞沉默线粒体基因重塑线粒体蛋白质组[9]
综上所述,该研究开发了一种能够特异性沉默活细胞线粒体中特定mRNA翻译的策略,通过点击化学连接获得线粒体前序列肽-吗啉寡核苷酸嵌合体pCox4-MO。将其转染入活细胞后,可靶向线粒体,特异性阻断线粒体编码基因的翻译。该研究提供了一种调控线粒体基因表达的新工具,揭示了线粒体蛋白质组的重塑逻辑,为理解细胞器质量控制系统与代谢适应性提供了新的视角。

GTP研发中心负责实施基因组标签计划(Genome tagging project, GTP),基于自主知识产权的类精子干细胞介导半克隆技术,为全基因组的功能基因一一贴上标签,致力于构建标签细胞和标签小鼠资源库。类精子干细胞是从精子来源单倍体囊胚中建系获得的一种孤雄单倍体胚胎干细胞,将其注入卵母细胞,能够像精子一样支持整个胚胎发育过程,产生健康的半克隆小鼠。GTP研发中心在类精子干细胞的蛋白质编码基因上原位敲入标签序列,建立了液氮保存的标签细胞资源库。研究需要时,利用半克隆技术将标签细胞注射到小鼠卵母细胞中,一步法获得标签小鼠。

已有标签产品可直接订购,详情查阅以下官网链接。如有需要欢迎联系,我们将竭诚为您服务。
标签细胞网址:
标签小鼠网址:
http://www.sibcb.ac.cn/gtp/msearch.jsp
地址:上海市岳阳路320号
责任编辑:多一百
新媒体运营:suway
参考文献
1. Rackham O, Filipovska A: Organization and expression of the mammalian mitochondrial genome. Nat Rev Genet 2022, 23(10):606-623.
2. Homberg B, Rehling P, Cruz-Zaragoza LD: The multifaceted mitochondrial OXA insertase. Trends in cell biology 2023, 33(9):765-772.
3. Hock DH, Robinson DRL, Stroud DA: Blackout in the powerhouse: clinical phenotypes associated with defects in the assembly of OXPHOS complexes and the mitoribosome. The Biochemical journal 2020, 477(21):4085-4132.
4. Lee M, Matsunaga N, Akabane S, Yasuda I, Ueda T, Takeuchi-Tomita N: Reconstitution of mammalian mitochondrial translation system capable of correct initiation and long polypeptide synthesis from leaderless mRNA. Nucleic acids research 2021, 49(1):371-382.
5. Gustafsson CM, Falkenberg M, Larsson NG: Maintenance and Expression of Mammalian Mitochondrial DNA. Annual review of biochemistry 2016, 85:133-160.
6. Lightowlers RN: Mitochondrial transformation: time for concerted action. EMBO reports 2011, 12(6):480-481.
7. Silva-Pinheiro P, Mutti CD, Van Haute L, Powell CA, Nash PA, Turner K, Minczuk M: A library of base editors for the precise ablation of all protein-coding genes in the mouse mitochondrial genome. Nature biomedical engineering 2023, 7(5):692-703.
8. Mok BY, de Moraes MH, Zeng J, Bosch DE, Kotrys AV, Raguram A, Hsu F, Radey MC, Peterson SB, Mootha VK et al: A bacterial cytidine deaminase toxin enables CRISPR-free mitochondrial base editing. Nature 2020, 583(7817):631-637.
9. Cruz-Zaragoza LD, Dahal D, Koschel M, Boshnakovska A, Zheenbekova A, Yilmaz M, Morgenstern M, Dohrke JN, Bender J, Valpadashi A et al: Silencing mitochondrial gene expression in living cells. Science 2025, 389(6759):eadr3498.
10. Cruz-Zaragoza LD, Dennerlein S, Linden A, Yousefi R, Lavdovskaia E, Aich A, Falk RR, Gomkale R, Schöndorf T, Bohnsack MT et al: An in vitro system to silence mitochondrial gene expression. Cell 2021, 184(23):5824-5837.e5815.
11. Couvillion MT, Soto IC, Shipkovenska G, Churchman LS: Synchronized mitochondrial and cytosolic translation programs. Nature 2016, 533(7604):499-503.
12. Molenaars M, Janssens GE, Williams EG, Jongejan A, Lan J, Rabot S, Joly F, Moerland PD, Schomakers BV, Lezzerini M et al: A Conserved Mito-Cytosolic Translational Balance Links Two Longevity Pathways. Cell metabolism 2020, 31(3):549-563.e547.



