技术分享:分泌组蛋白质翻译主要发生在LNPK富集的内质网-溶酶体接触点
内质网(ER)是一种高度互联的膜状网络结构,是蛋白质合成与成熟的主要场所。分泌组mRNA编码了分泌蛋白、腔内蛋白和整合膜蛋白,它们会被运输到细胞膜上或分泌到细胞外,约占人类蛋白质编码基因的将近三分之一。与胞质mRNA不同,分泌组mRNA经历了共翻译转位过程,需要在翻译与蛋白质插入之间完成精确协调。ER的片层结构富集了大量膜结合多聚核糖体,是分泌组mRNA翻译的主要场所[1]。近期研究表明核糖体,包括多聚核糖体及单体形式,广泛分布于几乎所有ER形态结构中,涵盖了片层、管状结构及管状-管状连接处[2]。相当一部分附着在ER上的核糖体是非翻译亚基,特别是60S大亚基[3, 4],表明核糖体与ER的结合并不等同于活跃的翻译延伸,可能反映了调控状态或翻译起始前状态。而通过Sec易位子组分精确定位翻译位点在技术上仍具挑战性,如对Sec61α或TRAP等核心成分进行遗传标记往往会干扰易位活性,免疫标记方法则受限于腔内或膜嵌入表位的空间不可及性[5]。因此,分泌组mRNA的翻译究竟是发生在空间受限的ER亚区[6-8],还是非选择性地在连续的ER网络中进行,仍是一个悬而未决的问题。
2026年1月,Nature期刊发表了一项研究,通过活细胞单分子成像示踪单个分泌组mRNA的动态与定位,首次揭示了分泌组mRNA翻译的空间组织规律。具体而言,活跃的分泌组mRNA翻译主要位于富含结构蛋白LNPK且紧邻溶酶体的内质网(ER)连接处。LNPK的缺失降低了溶酶体附近的核糖体密度和分泌组mRNA的翻译效率,这一作用依赖于eIF2介导的翻译起始过程,且能被综合应激反应抑制剂ISRIB所逆转。溶酶体接触的翻译进一步受到营养状态的调节,表现为氨基酸剥夺能增强溶酶体邻近翻译。这些发现共同确立了富含LNPK的ER连接处作为组织结构枢纽调控了分泌组mRNA的翻译。该研究揭示了一个由特定ER膜结构、邻近细胞器信号以及翻译起始调控通路共同构成的空间-功能耦合单元,不仅解答了领域内长期存在的翻译空间选择性的疑问,更为理解蛋白质合成质量控制在亚细胞层面的组织原则、以及细胞如何通过区室化协调生物合成与代谢状态提供了全新的认知[9]。
首先,为追踪分泌组mRNA的行为,研究者采用了MS2 mRNA标记技术[10],针对编码多种跨膜蛋白和腔内蛋白的开放阅读框构建了荧光报告系统。以高尔基体定位的II型膜蛋白唾液酸转移酶为模型,将其N端45个氨基酸编码序列与EGFP及MS2结合环融合串联起来(SiT-EGFP)(图一a)。该SiT-EGFP mRNA与MS2蛋白形成复合物(SiT-EGFP–MS2),便于荧光成像可视化单分子mRNA动态,同时使用荧光标记的Sec61β报告蛋白[11]无偏好性地标记ER。结果显示,单个SiT-EGFP–MS2复合物的荧光斑点主要位于ER,并表现出两种截然不同的行为:一些斑点基本上保持静止或被限制在ER上长达数十秒(图一a,区域1),而其他斑点则快速移动,在几秒内短暂地与ER结合并解离(图一a,区域2)。使用均方位移(MSD)对这些轨迹进行定量分析显示,约86%的分子在延迟时间(τ)=1 s时的MSD小于0.055 µm²,符合受限运动特征(图一b,红色虚线),群体平均值为0.011 µm²。使用嘌呤霉素终止翻译后,分子运动显著增强,此时79%的mRNA的MSDτ=1 s大于0.055 µm²,平均值为0.097 µm²,比对照组高出一个数量级(图一b和c)。颜色编码视频分析进一步证实,运动较慢的斑点始终与内质网结合,运动较快的斑点,尤其在嘌呤霉素处理后,常与ER解离(图一d)。以上结果表明,分泌组mRNA在翻译期间表现出ER表面的受限运动,而当翻译受阻时则变得更具运动性。
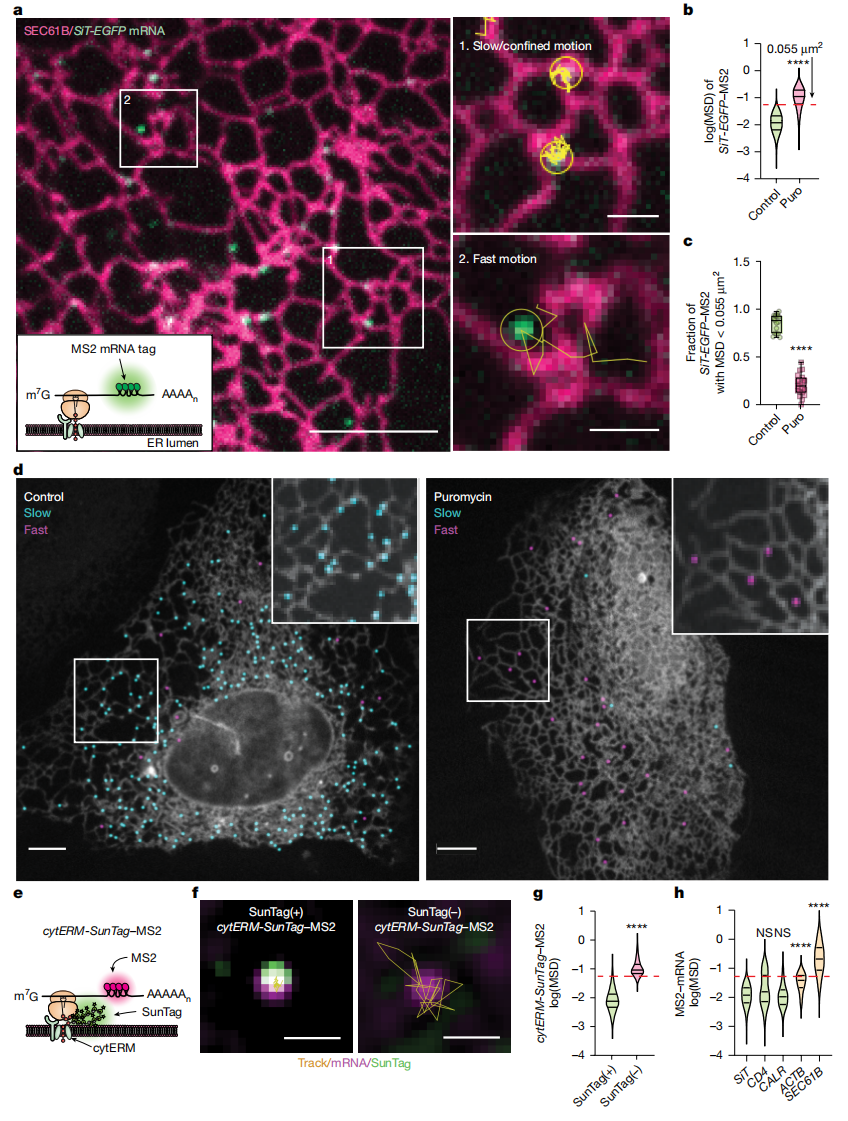
图一 分泌组mRNA在ER上翻译时显示运动受限[9]
为验证这些ER运动受限mRNA是否处于活跃翻译状态,研究者应用SunTag系统来监测新生肽链。构建了包含ER蛋白细胞色素p450的靶向序列和跨膜结构域的报告系统,并融合GCN4重复序列(cytERM-SunTag)及MS2茎环(图一e)。该设计使其C端SunTag表位暴露于细胞质,从而能够对正在翻译的mRNA进行荧光标记。当cytERM-SunTag–MS2斑点与来自翻译肽链的SunTag信号共定位时,即推断翻译正在进行。细胞中约40%的cytERM-SunTag–MS2斑点显示与SunTag信号共定位,这些翻译阳性斑点表现出近乎静止或高度受限的运动,而翻译阴性斑点则沿ER快速移动(图一f和g)。经嘌呤霉素处理后,SunTag信号消失,所有斑点转为高度移动状态。以受限运动作为翻译状态的表征,研究者比较了不同的分泌组mRNA行为。编码SiT-EGFP、CD4-EGFP和钙网蛋白-mEmerald的mRNA均表现出显著的受限斑点比例,表明大多数处于活跃翻译状态(图一h)。相比之下,编码β-肌动蛋白、Sec61β或线粒体蛋白TOMM20等非分泌蛋白的mRNA主要为运动模式,几乎未观察到受限运动现象(图一h)。以上数据表明,ER受限运动的分泌蛋白组mRNA代表了活跃翻译个体,而小部分移动个体为非翻译状态,这与胞质蛋白mRNA的行为形成鲜明对比,后者即使在翻译时仍保持运动性[12]。
ER是一个由管状结构交织形成的复杂膜网络,包含三向连接处、密集连接网络及片层等多种形态。为确定分泌组mRNA翻译的ER亚区,研究者在能分辨形态的外周ER中分析mRNA定位,着重观测ER结合且运动受限即翻译状态的分泌蛋白组mRNA。结果显示,正在翻译的分泌组mRNA富集在ER连接处(图二a),主要位于距离连接处0.2 µm范围内(图二b)。相比之下,运动较快的非翻译分泌蛋白组mRNA未呈现连接处富集的特征,且分布模式与ACTB或SEC61B等非分泌蛋白mRNA相似(图二b)。为探究内源性分泌组mRNA是否也优先在ER连接处翻译,研究者在表达mEmerald-Sec61β的U-2 OS细胞中进行杂交链式反应单分子荧光原位杂交(HCR-smFISH)检测内源性CD9 mRNA。尽管HCR-smFISH无法区分翻译态与非翻译态mRNA,但同样发现CD9 mRNA富集在ER连接处,并在嘌呤霉素处理后ER连接处的富集减少,同时距离增加(图二c和d),表明内源性分泌组mRNA也优先在ER连接处翻译。研究者进一步通过Halo标记的核糖体大亚基蛋白L10A,发现核糖体表现出快、中、慢三种扩散群体,只有慢速移动的群体定位于内质网连接处(图二e),嘌呤霉素处理后,慢速和中速移动的群体转变为快速群体。以上数据表明,分泌组mRNA及其关联核糖体在内质网连接处形成慢速移动的翻译池,首次证明了ER连接处是分泌组mRNA翻译的功能热点区域。
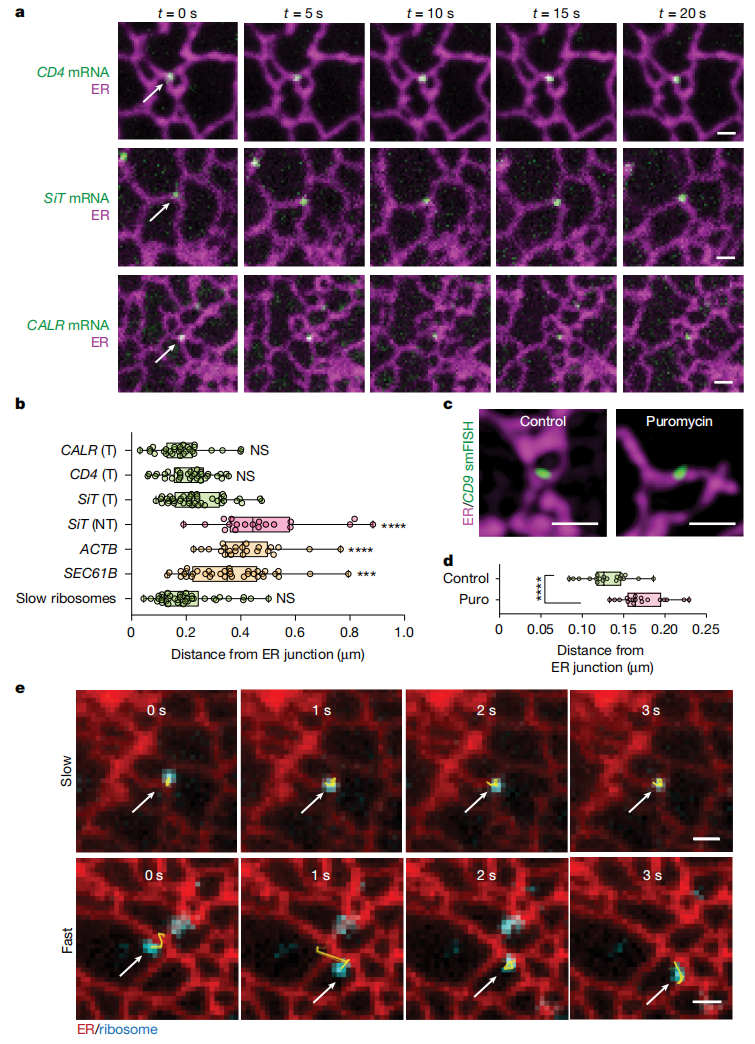
图二 ER连接处是分泌组mRNA翻译的热点区域[9]
ER连接处的形成或稳定被认为依赖于ER驻留的跨膜蛋白LNPK,该蛋白存在于部分的连接位点[13, 14]。当在细胞中表达LNPK-GFP时,确实优先定位于ER连接处(图三a)。为了测试LNPK阳性的内质网连接处是否参与分泌组mRNA翻译,研究者共表达ER翻译报告系统cytERM-SunTag,并对内源性LNPK进行了免疫染色。结果显示,翻译态SunTag(+)荧光斑点与LNPK信号强烈共定位(图三b),80% SunTag(+)荧光位于LNPK信号300 nm范围内,而在同一细胞中,仅有50%的非翻译态SunTag(-)在此范围内(图三c),表明正在翻译的分泌组mRNA优先富集于含有LNPK的ER连接处。为测试LNPK是否调控分泌组mRNA翻译,研究者在表达SiT-EGFP–MS2的细胞中敲降LNPK(LNPK-KD)。发现在LNPK-KD细胞中,SiT-EGFP–MS2显示出运动性增强(图三d)。使用MSD小于0.055 µm²来界定翻译中的分泌组mRNA,发现细胞翻译比例从对照组的86%降至LNPK-KD细胞的39%(图三e)。相比之下,敲降ER形态调控蛋白CLIMP63则没有显著影响,超过80%的SiT-EGFP mRNA仍保持翻译状态(图三d和e)。进一步检测LNPK敲除(LNPK-KO)细胞中的稳态蛋白质水平,发现总蛋白水平未改变,但膜蛋白水平显著降低(图三f),表明LNPK对于维持膜蛋白和分泌蛋白的翻译至关重要。
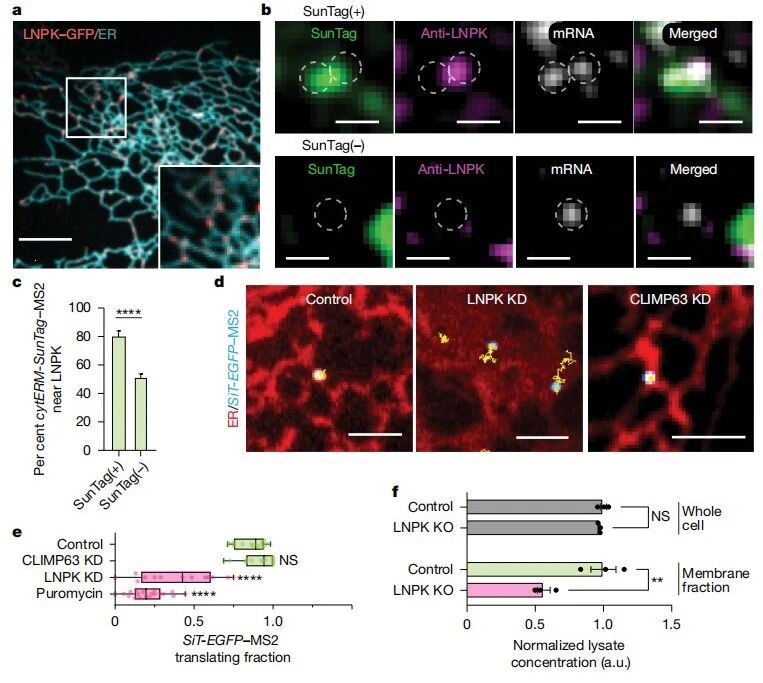
图三 分泌组mRNA翻译在LNPK阳性的ER连接处增强[9]
先前研究表明,溶酶体可以与轴突翻译位点[15]以及ER连接处[16, 17]结合,可能经由LNPK介导。为了直接验证结合,研究者使用LNPK抗体分别与早期内体标志物EEA1、溶酶体标志物LAMP1或线粒体标志物TOMM20进行邻近连接实验(PLA,图四a)。与EEA1和TOMM20相比,与LAMP1产生的PLA信号显著更强(图四b和c),表明富含LNPK的ER区域优先与溶酶体结合。作为特异性对照,研究者使用了一种丰度与LNPK相似但已知与溶酶体无相互作用的ER蛋白REEP5进行PLA实验(图四c),结果仅观察到背景水平的PLA信号,进一步证实溶酶体结合特异性发生在LNPK阳性ER区域。为评估LNPK对ER-溶酶体结合的作用,研究者采用了基于光诱导iLID-sspB二聚化系统的光遗传学募集实验(图四d)。细胞共表达LAMP1-iLID和sspB-Sec61β后,在蓝光刺激下表现出溶酶体向ER的快速募集,最终形成ER紧密包裹溶酶体的结构(图四e和f)。相比之下,LNPK-KO细胞显示出明显更慢的募集速度(图四e和f),表明LNPK促进了ER-溶酶体接触的形成和稳定。为进一步探究溶酶体是否与活跃的翻译位点相关,研究者共表达cytERM-SunTag–MS2报告系统与荧光标记的LAMP1,观察到正在翻译的分泌组mRNA斑点常位于LAMP1阳性的溶酶体旁侧(图四g)。当cytERM-SunTag–MS2荧光紧邻溶酶体时,其SunTag信号强度增强(图四h上),提示靠近溶酶体的分泌组mRNA能募集更多数量的核糖体(图四h下),表明增强的分泌组mRNA翻译在空间上定位于邻近溶酶体的ER亚区。这一SunTag信号增强现象,在LNPK敲降后消失(图四h),表明LNPK对于增强分泌组mRNA翻译的ER-溶酶体接触点建立至关重要。
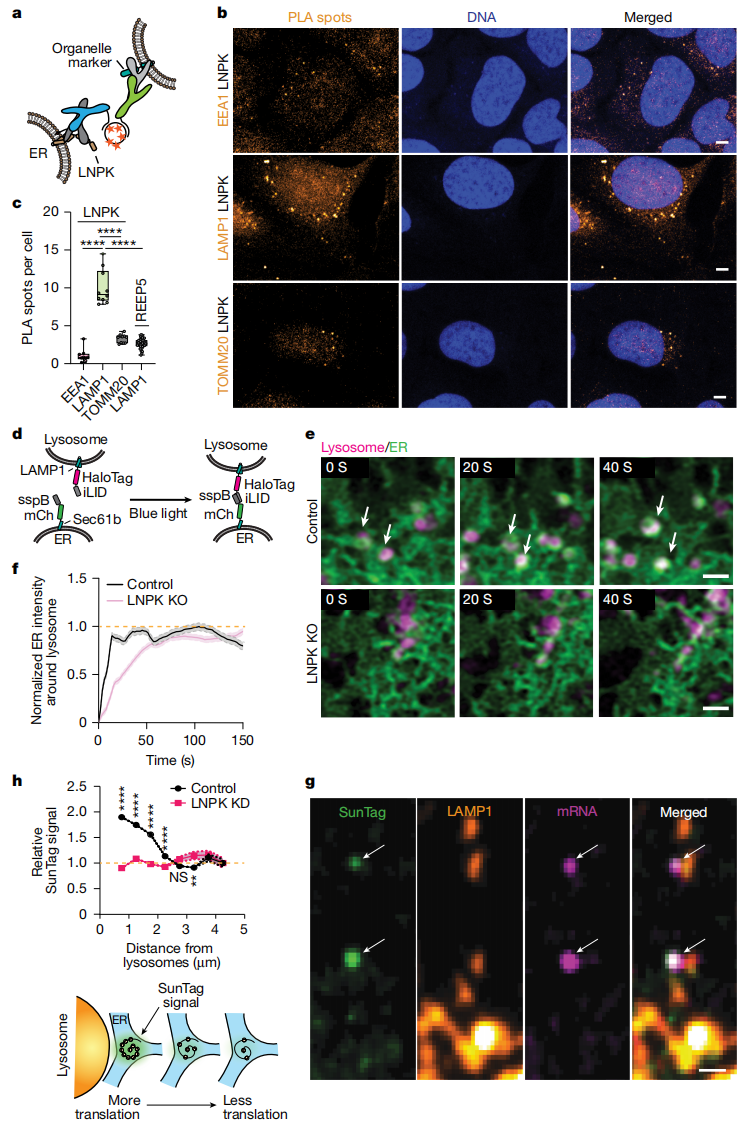
图四 LNPK富集的ER连接处招募溶酶体并促进翻译[9]
溶酶体作为一种酸性降解区室,可将吞噬的蛋白质降解为氨基酸,随后释放到胞质以支持细胞功能。由此,研究者推测溶酶体这一功能与增强分泌组mRNA的翻译相关。发现无论是通过氯喹(CQ)提高溶酶体pH还是抑制溶酶体蛋白酶活性来破坏溶酶体的蛋白质降解功能,都显著降低了SiT-EGFP mRNA的翻译(图五a)。在氨基酸匮乏条件下,溶酶体降解尤为重要。结果发现,氨基酸饥饿显著增强分泌组mRNA翻译与溶酶体邻近性之间的关联(图五b),表明当氨基酸匮乏时,分泌组mRNA的翻译效率更加依赖于与溶酶体的接触,突显了营养可用性与蛋白质合成之间一种特定的空间协调机制。
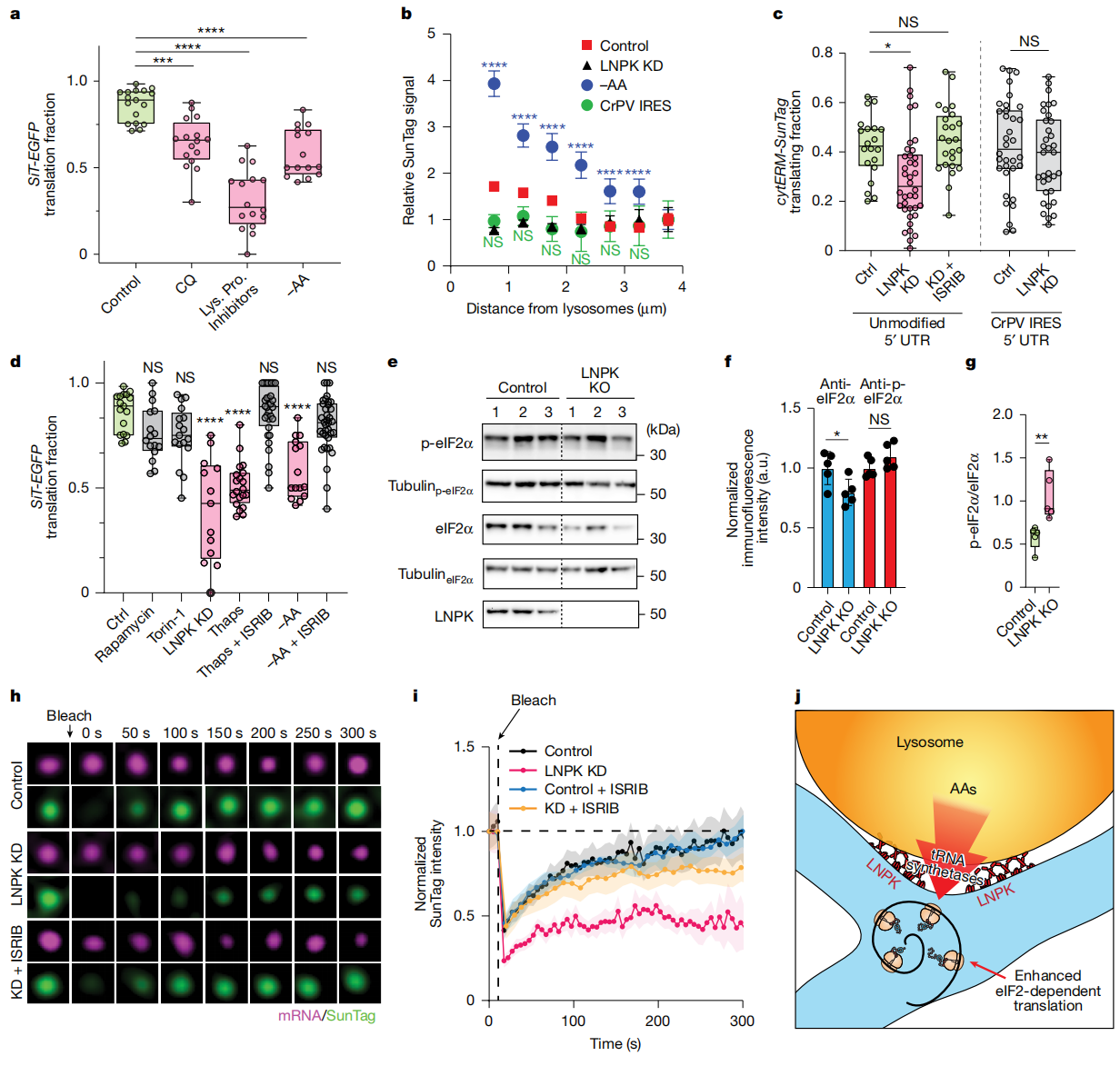
图五 溶酶体活性和LNPK通过eIF2调控分泌组翻译[9]
为了揭示驱动溶酶体附近分泌组mRNA翻译增强的调控机制,研究者聚焦于翻译起始这一哺乳动物蛋白质合成的限速步骤[18]。对cytERM-SunTag–MS2报告基因的5'非翻译区进行改造,使其包含蟋蟀麻痹病毒内部核糖体进入位点(CrPV IRES),该位点能绕过几乎所有经典的翻译起始调控[19]。在表达包含CrPV IRES的报告基因后,改造前观察到的溶酶体邻近SunTag信号增强现象消失了(图五b),表明溶酶体结合后的翻译增强依赖于翻译起始过程。随后研究者在野生型和LNPK-KD细胞中比较两种报告基因的翻译水平,改造前的报告基因翻译在LNPK缺失后显著降低,而含有CrPV IRES的报告基因则没有明显变化(图五c),表明破坏LNPK是通过干扰翻译起始过程来抑制分泌组mRNA翻译的。翻译起始可受综合应激反应(ISR)通路调控,通过磷酸化eIF2α抑制蛋白质合成,可被抑制剂ISRIB所逆转。ISRIB处理后,LNPK-KD细胞的cytERM-SunTag mRNA翻译可恢复至对照水平(图五c)。相比之下,使用不触发ISR的雷帕霉素或Torin-1抑制mTOR信号,对SiT-EGFP的翻译没有影响(图五d)。进一步评估eIF2α的磷酸化状态,发现LNPK-KO细胞中磷酸化eIF2α与总eIF2α的比值升高(图五e-g)。
为直接监测活细胞中分泌组mRNA的新生肽链合成,研究者对SunTag斑点进行荧光漂白恢复(FRAP)实验。在对照组细胞中,单个SunTag斑点经光漂白后能在300秒内完全恢复至漂白前荧光水平。相比之下,LNPK-KD细胞的恢复动力学显著受损,同一时间段内荧光未能恢复至漂白前水平。而用ISRIB处理LNPK-KD细胞后,SunTag的恢复动力学恢复到与对照细胞相似的水平(图五h和i),表明抑制剂ISRIB能够特异性挽救由LNPK缺失诱导的翻译缺陷。以上数据表明,ER连接处的LNPK通过一种eIF2依赖机制来调控分泌组mRNA的新生肽链,同时溶酶体贡献了局部氨基酸库,以及可能提供促进共翻译易位的tRNA(图五j)。
综上所述,该研究全新揭示了分泌组mRNA的翻译并非内质网(ER)随机分布,而是特异性富集于富含LNPK蛋白的ER连接处,并且紧邻溶酶体。LNPK蛋白对维持该区域翻译效率具有关键作用。LNPK缺失会通过损害eIF2依赖性翻译起始,特异性降低这些连接处分泌组mRNA的翻译,而这种效应可被整合应激反应(ISR)抑制剂ISRIB挽救。在氨基酸饥饿条件下,溶酶体-ER接触点的分泌组mRNA翻译被增强,并且与溶酶体活性正相关。该研究将LNPK富集的ER-溶酶体接触点定义为分泌组mRNA翻译的空间调节核心位点,共同构成了一个动态调控单元,协同整合了细胞器结构、营养信号与翻译起始过程,实现精确调控分泌蛋白和膜蛋白的合成。该研究突破了翻译调控的传统认知,为后续探索细胞器间通讯及其影响蛋白质组合成奠定了重要基础。

GTP研发中心负责实施基因组标签计划(Genome tagging project, GTP),基于自主知识产权的类精子干细胞介导半克隆技术,为全基因组的功能基因一一贴上标签,致力于构建标签细胞和标签小鼠资源库。类精子干细胞是从精子来源单倍体囊胚中建系获得的一种孤雄单倍体胚胎干细胞,将其注入卵母细胞,能够像精子一样支持整个胚胎发育过程,产生健康的半克隆小鼠。GTP研发中心在类精子干细胞的蛋白质编码基因上原位敲入标签序列,建立了液氮保存的标签细胞资源库。研究需要时,利用半克隆技术将标签细胞注射到小鼠卵母细胞中,一步法获得标签小鼠。

已有标签产品可直接订购,详情查阅以下官网链接。如有需要欢迎联系,我们将竭诚为您服务。
标签细胞网址:
标签小鼠网址:
http://www.sibcb.ac.cn/gtp/msearch.jsp
地址:上海市岳阳路320号
责任编辑:甜点
新媒体运营:suway
参考文献
1. Shibata Y, Voeltz GK, Rapoport TA: Rough sheets and smooth tubules. Cell 2006, 126(3):435-439.
2. Heinrich L, Bennett D, Ackerman D, Park W, Bogovic J, Eckstein N, Petruncio A, Clements J, Pang S, Xu CS et al: Whole-cell organelle segmentation in volume electron microscopy. Nature 2021, 599(7883):141-146.
3. Zhang Z, Xu A, Bai Y, Chen Y, Cates K, Kerr C, Bermudez A, Susanto TT, Wysong K, Garcia Marques FJ et al: A subcellular map of translational machinery composition and regulation at the single-molecule level. Science 2025, 387(6738):eadn2623.
4. Seiser RM, Nicchitta CV: The fate of membrane-bound ribosomes following the termination of protein synthesis. J Biol Chem 2000, 275(43):33820-33827.
5. Snapp EL, Reinhart GA, Bogert BA, Lippincott-Schwartz J, Hegde RS: The organization of engaged and quiescent translocons in the endoplasmic reticulum of mammalian cells. J Cell Biol 2004, 164(7):997-1007.
6. Bar-Peled L, Chantranupong L, Cherniack AD, Chen WW, Ottina KA, Grabiner BC, Spear ED, Carter SL, Meyerson M, Sabatini DM: A Tumor suppressor complex with GAP activity for the Rag GTPases that signal amino acid sufficiency to mTORC1. Science 2013, 340(6136):1100-1106.
7. Kim S, Yoon I, Son J, Park J, Kim K, Lee JH, Park SY, Kang BS, Han JM, Hwang KY et al: Leucine-sensing mechanism of leucyl-tRNA synthetase 1 for mTORC1 activation. Cell Rep 2021, 35(4):109031.
8. Moon SL, Parker R: Analysis of eIF2B bodies and their relationships with stress granules and P-bodies. Sci Rep 2018, 8(1):12264.
9. Choi H, Liao YC, Yoon YJ, Grimm J, Wang N, Lavis LD, Singer RH, Lippincott-Schwartz J: Secretome translation shaped by lysosomes and lunapark-marked ER junctions. Nature 2026, 649(8095):227-236.
10. Bertrand E, Chartrand P, Schaefer M, Shenoy SM, Singer RH, Long RM: Localization of ASH1 mRNA particles in living yeast. Mol Cell 1998, 2(4):437-445.
11. Obara CJ, Moore AS, Lippincott-Schwartz J: Structural Diversity within the Endoplasmic Reticulum-From the Microscale to the Nanoscale. Cold Spring Harb Perspect Biol 2023, 15(6):a041259.
12. Wu B, Eliscovich C, Yoon YJ, Singer RH: Translation dynamics of single mRNAs in live cells and neurons. Science 2016, 352(6292):1430-1435.
13. Chen S, Desai T, McNew JA, Gerard P, Novick PJ, Ferro-Novick S: Lunapark stabilizes nascent three-way junctions in the endoplasmic reticulum. Proc Natl Acad Sci U S A 2015, 112(2):418-423.
14. Wang S, Tukachinsky H, Romano FB, Rapoport TA: Cooperation of the ER-shaping proteins atlastin, lunapark, and reticulons to generate a tubular membrane network. Elife 2016, 5:e18605.
15. Cioni JM, Lin JQ, Holtermann AV, Koppers M, Jakobs MAH, Azizi A, Turner-Bridger B, Shigeoka T, Franze K, Harris WA et al: Late Endosomes Act as mRNA Translation Platforms and Sustain Mitochondria in Axons. Cell 2019, 176(1-2):56-72 e15.
16. Guo Y, Li D, Zhang S, Yang Y, Liu JJ, Wang X, Liu C, Milkie DE, Moore RP, Tulu US et al: Visualizing Intracellular Organelle and Cytoskeletal Interactions at Nanoscale Resolution on Millisecond Timescales. Cell 2018, 175(5):1430-1442 e1417.
17. Yuniati L, Lauriola A, Gerritsen M, Abreu S, Ni E, Tesoriero C, Onireti JO, Low TY, Heck AJR, Vettori A et al: Ubiquitylation of the ER-Shaping Protein Lunapark via the CRL3(KLHL12) Ubiquitin Ligase Complex. Cell Rep 2020, 31(7):107664.
18. Gebauer F, Hentze MW: Molecular mechanisms of translational control. Nat Rev Mol Cell Biol 2004, 5(10):827-835.
19. Petrov A, Grosely R, Chen J, O'Leary SE, Puglisi JD: Multiple Parallel Pathways of Translation Initiation on the CrPV IRES. Mol Cell 2016, 62(1):92-103.



