技术分享:开发超亮化学标记技术LINCS,快速绘制大组织神经连接图谱
哺乳动物大脑是一个由数十亿神经元通过数万亿突触连接而成的精密神经网络。在这个复杂结构中,单个神经元在形态特征、转录特性及功能作用方面都具有显著差异[1]。为揭示大脑的组织规律与功能连接,急需能捕捉这种多样性的单细胞分辨率技术。近年来,随着基因标记技术、高精度成像和计算分析手段的不断进步,推动着哺乳动物全脑神经元形态重构的研究进程[2],为理解大脑功能背后的介观尺度连接机制和结构特征提供了关键见解[3]。目前单神经元重构策略主要依赖于荧光蛋白标记神经元,并在亚微米级尺度上进行高分辨率成像,而这一过程需耗时较长的样本制备和成像时间[2]。光片荧光显微技术结合组织透明化技术,已成为快速获取大体积组织高分辨率成像的革命性方法,可实现群体层面的介观尺度连接图谱绘制[4],但在单神经元重构中的应用仍受限于现有标记方法的局限性。例如,荧光蛋白在组织透明化过程中易发生淬灭现象[5],而替代信号放大策略的抗体或纳米抗体可能存在组织穿透力不足、处理时间较长或信号放大效果不理想等问题[6]。此外,有效的单神经元重构需要采用稀疏标记技术来达到最佳密度和分辨率[7]。因此,迫切需要开发新型标记系统,可在标记精度和成像效率方面获得提升,既具备稳定性、高效性和可扩展性,又能兼容光片显微镜与组织透明化处理流程。
2025年11月,Neuron期刊报道了一种单神经元化学染料与可控稀疏性标记技术(LINCS),实现小鼠全脑与全身范围内快速、超亮且光稳定的细胞类型特异性化学标记。LINCS技术采用工程化可溶性增强型的生物素连接酶(seTurboID)进行在体生物素化修饰[8],随后使用荧光染料偶联的高亲和力单价链霉亲和素变体实现快速低背景的全脑染色,将生物素标记转化为荧光信号,从而实现细胞类型和神经环路特异性的靶向神经元标记。结合组织透明化处理与光片显微镜技术,该系统构建了高效分析中枢与外周神经系统长程神经投射的完整流程。此外,还开发了基于Cas9介导Cre基因敲除的腺相关病毒(AAV)策略,实现稳定稀疏标记,从而在大规模尺度上精确重构单个神经元的形态结构。LINCS技术显著降低了大规模神经连接图谱绘制的门槛,实现了全脑神经元重构的快速便捷操作,可加速哺乳动物神经回路的解剖学与功能解析进程[9]。TurboID在细胞内表达时,能够催化生物素基团与邻近蛋白质发生共价结合。随后,通过链霉亲和素介导的下拉实验分离生物素化蛋白质,进行鉴定和定量分析。
TurboID已成功用于活体神经元的细胞类型特异性蛋白质组学分析,尚不清楚其介导的细胞内生物素标记能否产生足够的信号分子,用于神经元精细结构的荧光成像,尤其是长距离轴突投射。为了验证这种可能性,研究者首先在背侧中缝核(DRN)的血清素能神经元中测试TurboID,这是一个广泛轴突投射的神经元群体[10]。构建了Cre依赖性的AAV9-FLAG-TurboID载体,通过立体定位注射到Sert-Cre小鼠的DRN区域,等待3周使病毒充分表达后,通过对脑切片进行FLAG标签的免疫染色来评估TurboID在血清素能神经元中的表达。结果显示,在注射位点周围的血清素能神经支配的下游脑区检测到稀疏且微弱的FLAG阳性神经元(图一B),表明TurboID在神经元中的表达很弱。为此,研究者在TurboID的C端融合了促溶标签GB1(链球菌蛋白G的B1结构域)[11],构建了可溶性增强型生物素连接酶(seTurboID),并将相应AAV9表达载体注射到Sert-Cre小鼠的DRN区域(图一A)。随后,在小鼠饮用水中为期1周补充2 mM生物素,诱导在体生物素化。引入GB1标签使得TurboID在神经元胞体和远端轴突以及多个下游脑区中的表达量均显著提升(图一B和C)。使用荧光染料偶联的链霉亲和素进行全脑染色,样本经透明化处理后,进行光片显微镜成像(图一D)。虽然在DRN和皮层区域观察到强烈的荧光信号,但在深部脑区及致密纤维束中却未见明显标记(图一F和G)。鉴于链霉亲和素的四价特性可能导致探针聚集并限制组织渗透,研究者采用一种仅保留单个高亲和力生物素结合位点的单价链霉亲和素变体[12](图一E)。这一改进实现了全脑均匀渗透,与野生型链霉亲和素形成鲜明对比(图一F和G)。更重要的是,它实现了高特异性标记,避免了四价同源物常见的非特异性血管标记(图一H)。研究者将这种基于seTurboID和单价链霉亲和素技术的全脑细胞荧光标记方案称为单神经元化学染料与可控稀疏性标记技术(LINCS)。
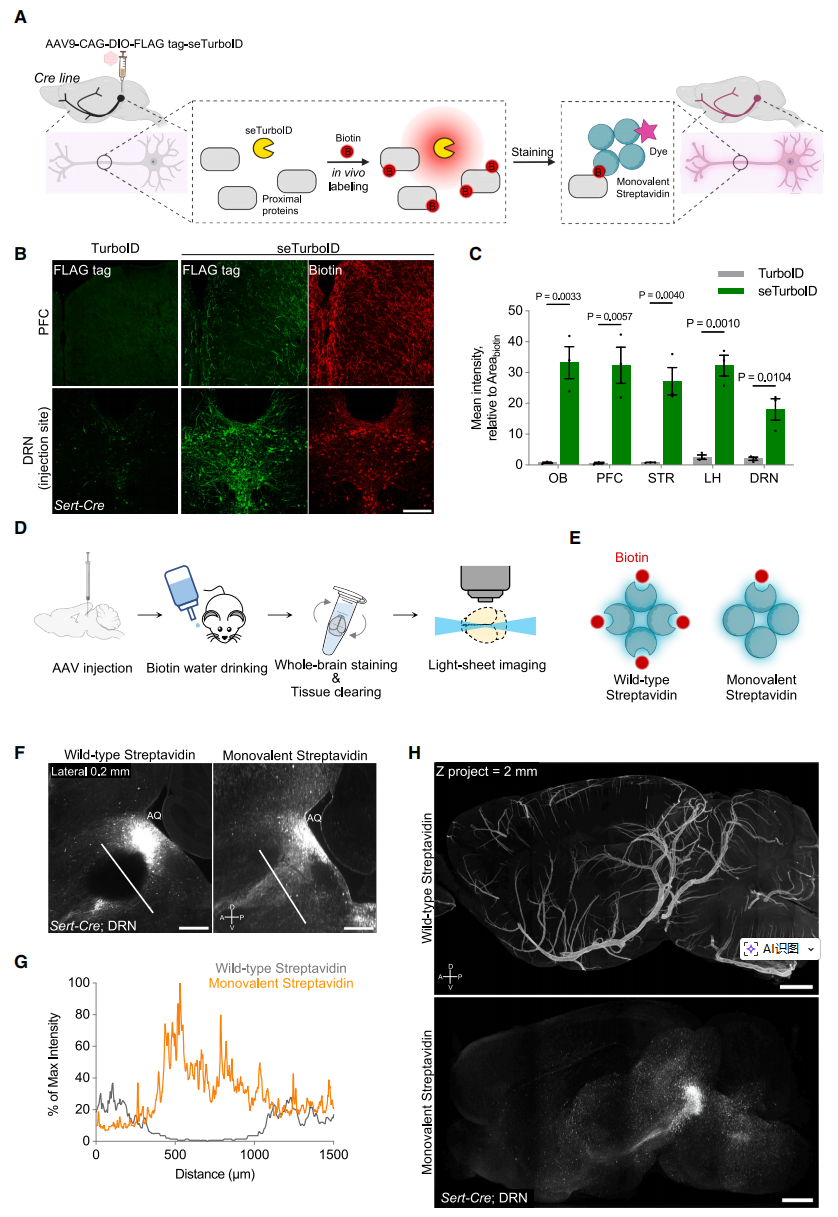
图一 基于seTurboID和单价链霉亲和素的LINCS技术开发[9]
与依赖荧光蛋白表达和抗体信号级联放大的传统方法相比,LINCS显著缩短样本制备时间(图二A)。具体而言,它将病毒表达所需时间从传统方法的1个月以上缩减至3周。更重要的是,采用小且热稳定的单价链霉亲和素,规避了大分子IgG抗体所需的漫长孵育步骤,单次仅需3天染色孵育,且可耐受42℃加热加速反应。该方案适用于从小鼠全脑到成年个体全身的各种组织样本(图二A)。除了速度更快之外,LINCS技术还通过双重信号放大策略实现了超亮标记。首先,seTurboID酶的活性为体内生物素化提供了强大的支持;其次,每个生物素都能被荧光标记的链霉亲和素精准捕获。这种组合产生的荧光信号不仅强度惊人、光稳定性优异,更能经受住严苛的化学透明化处理,从而实现高保真的解剖结构成像。
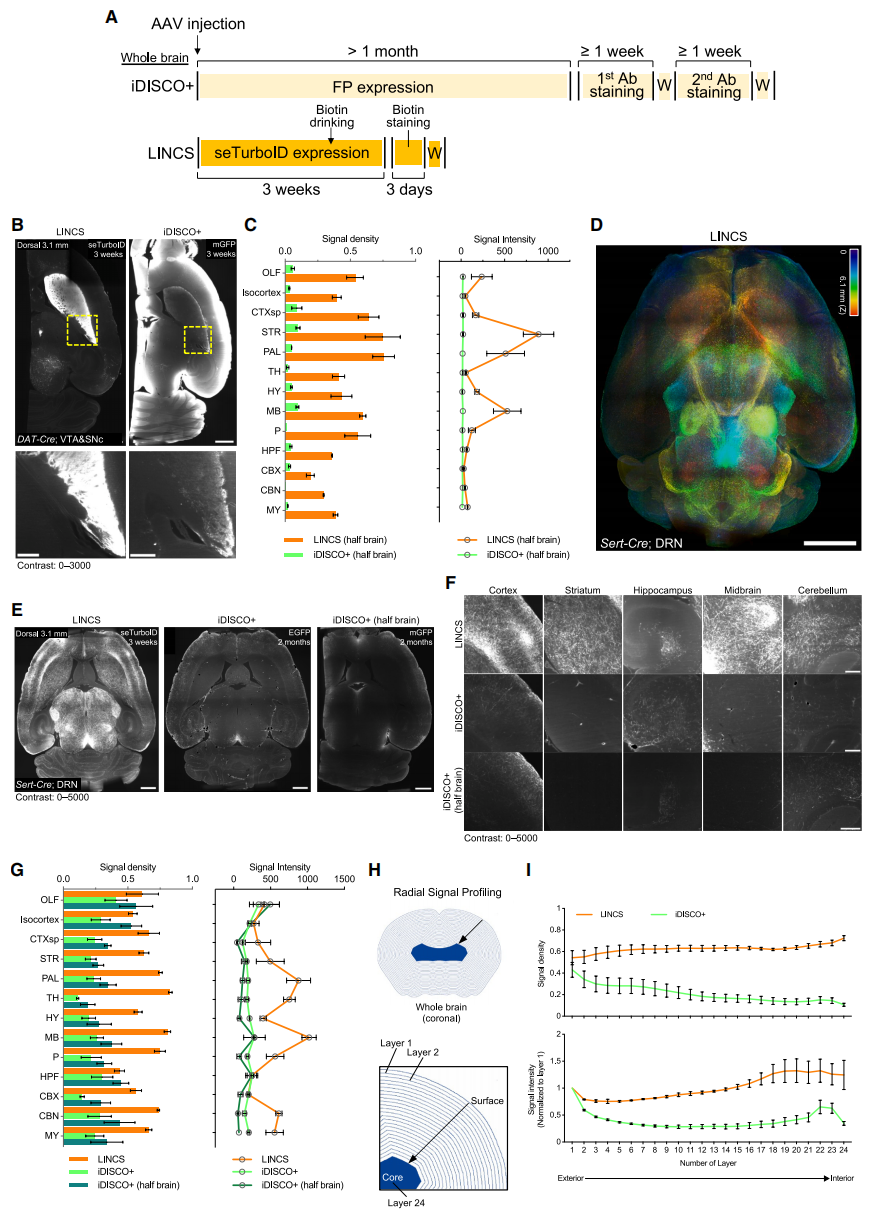
图二 LINCS技术实现全脑神经元投射的快速测绘[9]
随后,研究者将LINCS技术应用于DAT-Cre小鼠,标记其腹侧被盖区(VTA)和黑质致密部(SNc)的多巴胺能神经元[13],采用基于DISCO的方案进行组织透明化处理。同步制备了使用病毒表达膜结合绿色荧光蛋白(mGFP;可优化轴突末梢靶向性)和基于IgG的iDISCO+全脑染色方案的对比样本。运用光片显微镜对LINCS和iDISCO+标记的多巴胺能神经投射进行成像定位,在1 mm厚脑切片和半脑样本中评估两种技术的性能(图二B)。在1 mm切片中,LINCS展现出比iDISCO+更优的信噪比,确保了信号高效可视化。在半脑样本中,LINCS实现了稳定标记,而iDISCO+则出现标记强度减弱和背景信号升高的现象,尤其在组织表面更为明显(图二B)。定量比较两种技术,从原始荧光图像中提取轴突信号,测定不同脑区的信号密度和强度,发现在半脑样本中LINCS产生的信号密度和强度显著高于iDISCO+(图二C)。在Sert-Cre小鼠中进行类似对比,在LINCS标记样本中,皮层及大脑深部区域存在广泛的血清素能神经投射(图二D-F)。与iDISCO+相比,LINCS在丘脑、中脑等深层组织区域显示出更强的荧光信号和更密集的轴突标记(图二E-G)。通过测量从脑表面到中心的径向信号,发现iDISCO+处理样本的轴突信号强度和密度均随深度增加而显著衰减(图二H和I)。相比之下,LINCS的信号分布更为均匀,且在对应DRN胞体信号的脑最深区域呈现增强趋势(图二I)。
在脑组织样本中成功应用LINCS技术后,研究者进一步测试在中枢神经系统外长程神经投射图谱绘制中的应用。利用LINCS技术对皮质脊髓束进行可视化研究。通过在CaMKII-Cre小鼠颈段脊髓(C7和C8节段)单侧注射AAV2-retro病毒,逆行递送Cre依赖性膜结合型seTurboID(mem-seTurboID)实现神经元标记(图三A)。注射三周后,对保留部分脊髓(至L3椎骨)的完整脑组织进行LINCS全组织染色(图三B),可清晰辨识脊髓全段的轴突束及单个轴突(图三C和D)。通过将脑组织匹配至艾伦小鼠脑通用坐标框架(CCFv3)脑区[14](图三E),在对侧次级体感皮层(S2,特别是第5层;图三F)、初级运动皮层(M1)、次级运动皮层(M2)及初级体感皮层(S1)均观察到明亮标记的神经元胞体(图三G)。
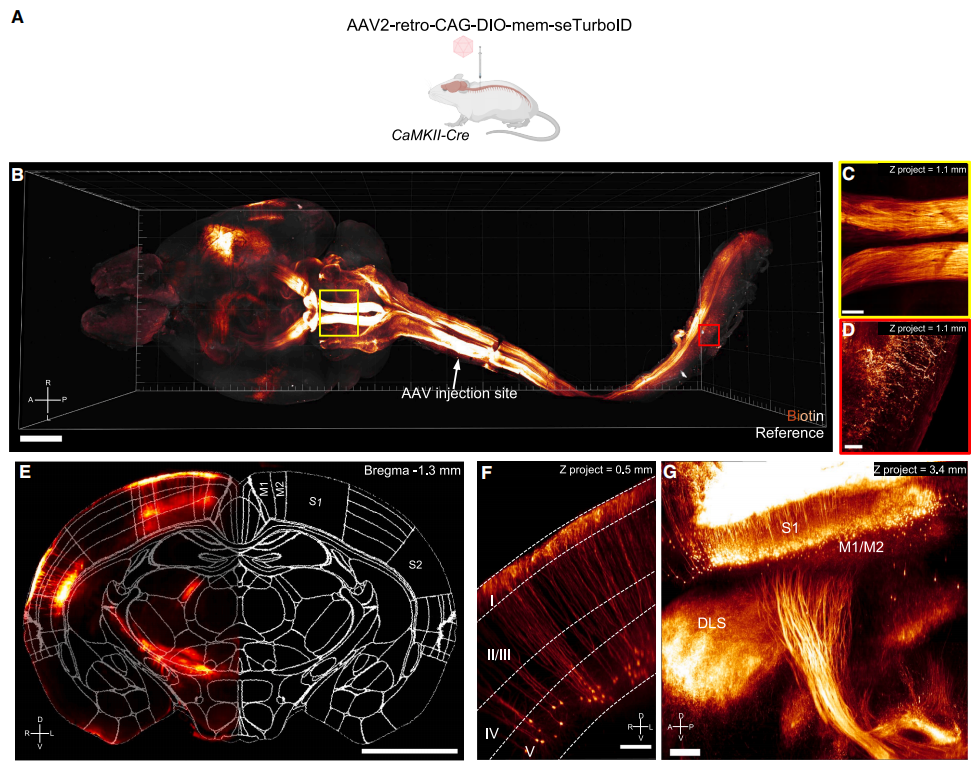
图三 LINCS实现长程轴突投射的高效标记[9]
随后,研究者评估LINCS技术在小鼠全身样本中的表现。通过静脉注射AAV-MaCPNS2-hSyn-mem-seTurboID至成年小鼠体内,标记外周神经系统神经元,通过血管灌注单价链霉亲和素以确保其在全身均匀分布。值得注意的是,即便对于成年小鼠全身样本,LINCS仅需3天短暂孵育/灌注周期即可实现高效标记(图四A和B),结果显示在多种器官中观察到强烈标记的细胞与神经突起,例如皮肤支配轴突(图四C和D)、沿胃肠分布的肠道神经系统(图四E-K)、尾部(图四L)及爪部(图四M和N)等。以上数据表明,LINCS技术在处理各类大体积组织样本时具有高度适应性,有助于绘制超越大脑范围的神经元连接网络。
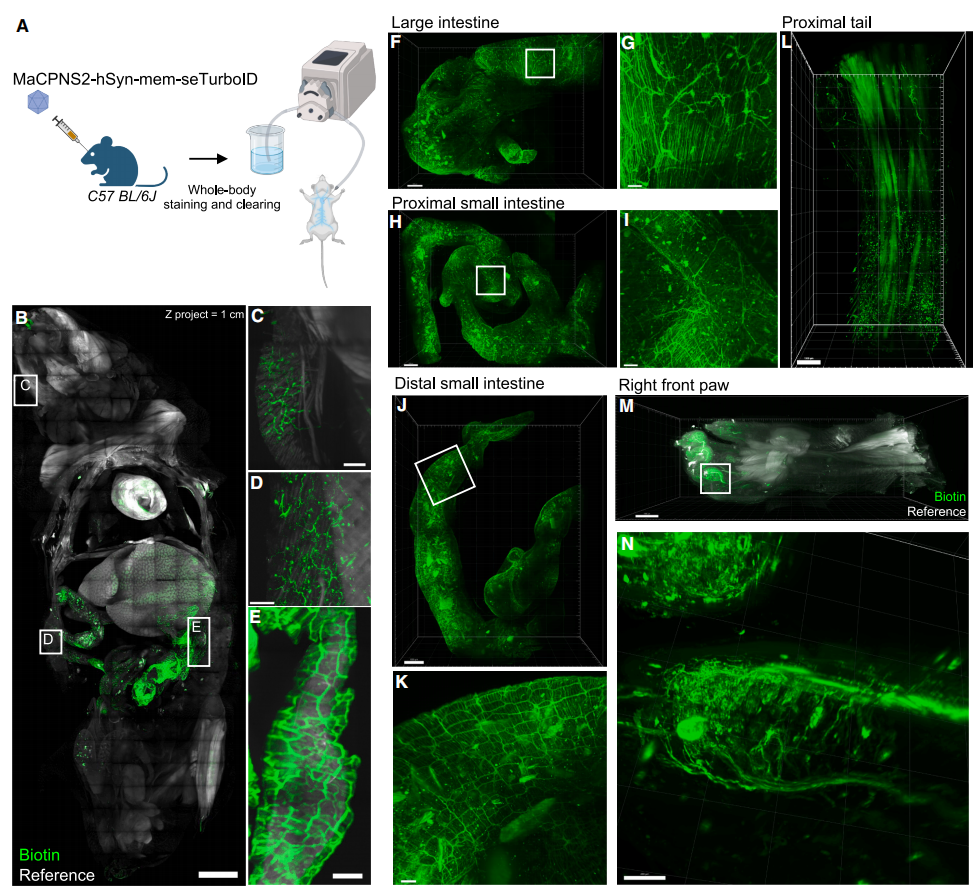
图四 LINCS实现小鼠全身样本外周神经系统的高效标记[9]
稀疏标记技术对于精确重构单个神经元至关重要。研究者先前开发的双AAV表达系统能够实现荧光蛋白对单个神经元的强效稀疏标记[15]。然而,当前基于AAV的稀疏标记技术存在随时间推移标记密度逐渐增加的问题,导致细胞计数不稳定且样本间差异显著。这对长距离投射的稀疏标记构成特殊挑战,需要延长病毒表达周期才能获得最大标记强度。为解决该问题,研究者开发了一种通过CRISPR-Cas9介导体内Cre敲除的稳定稀疏标记系统,采用AAV表达SaCas9和靶向Cre的sgRNA。在细胞特异性Cre转基因小鼠模型中,向特定脑区靶向递送Cre-KO AAV后,仅保留Cre表达的神经元可实现后续Cre依赖性标记(图五A)。由此产生的标记稀疏度由Cre-KO效率决定,从而规避了基于AAV的稀疏标记技术常伴随的时间依赖性标记密度增加问题。通过调整sgRNA数量、滴定Cre-KO AAV浓度或优化其表达时间,可调节标记稀疏度(图五B-F)。与先前的双AAV稀疏标记系统相比,Cre-KO AAV系统在维持稳定标记密度方面展现出更优的长期稳定性(图五G和H)。
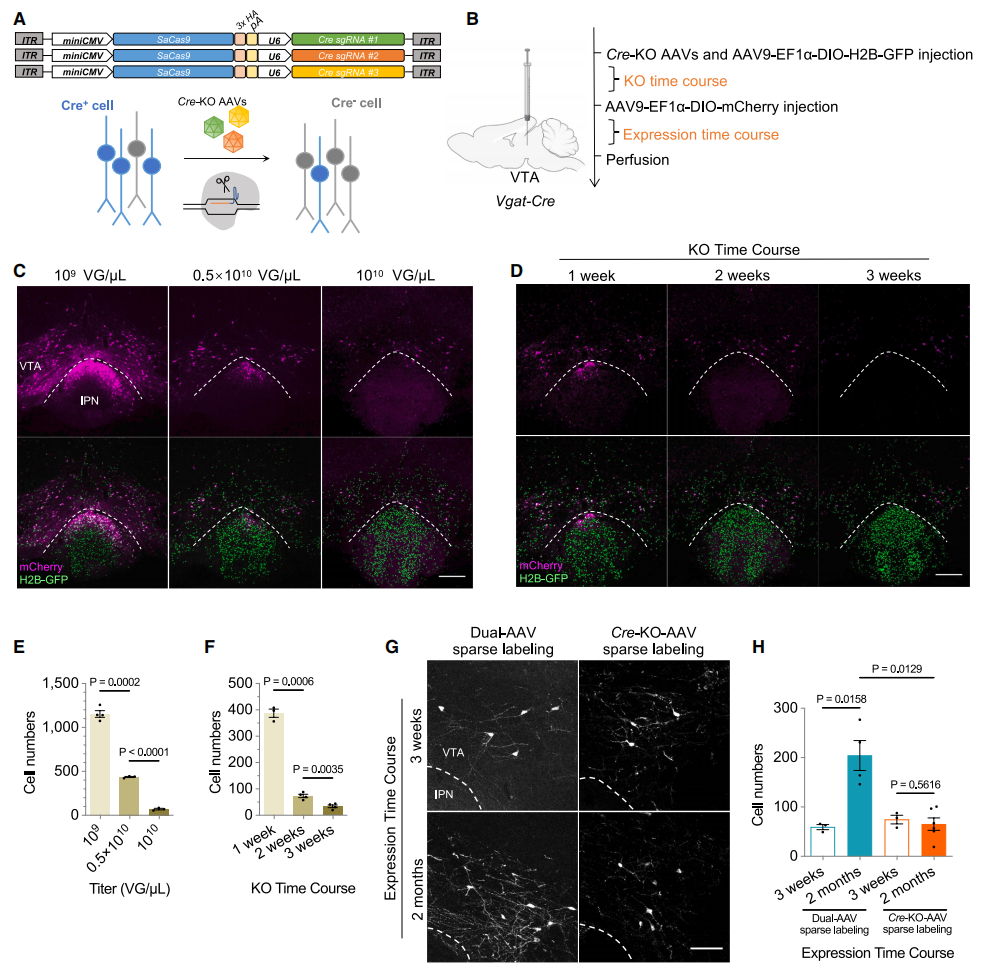
图五 开发可调控稳定稀疏标记神经元的Cre-KO AAV系统[9]
最后,研究者展示了LINCS技术在基于组织透明化和标准光片显微镜的高效全脑单神经元重构流程(图六A)。案例1,通过在纹状体(STR)注射逆向控制AAV,同时在VTA和SNc注射编码膜结合型seTurboID的放大器AAV(图六B和C),从五只DAT-Cre小鼠中重构了11个STR投射至中脑的多巴胺能神经元,观察到多巴胺能神经元在STR内存在广泛的轴突分支,其特征为局灶性分支模式(图六H),同时发现3个STR投射神经元缺乏密集分支结构(图六H)。接着,将双重AAV与Cre-KO AAV的稀疏标记系统进行整合,利用双重AAV系统实现强效标记,以及Cre-KO AAV系统维持稳定的稀疏标记(图六D和F)。案例2,在两只Vgat-Cre转基因小鼠腹侧被盖区(VTA)和中脑深核(DpMe)注射包含Cre-KO AAV和双重AAV的混合病毒,重构出8个中脑GABA能神经元(图六D和E),其中7个为中间神经元,1个为靶向腹侧STR的投射神经元(图六I)。案例3,分别在单只Vgat-Cre小鼠中脑导水管周围灰质(PAG)区注射逆向控制器AAV,外侧下丘脑(HY)区注射Cre-KO AAV与放大器AAV混合病毒(图六F),成功重构出5个PAG投射的下丘脑GABA能神经元(图六G)。这些神经元均呈现独特的投射模式,凸显了该神经元群的形态多样性(图六J)。以上数据表明,通过将光片显微镜与稀疏标记技术相结合,LINCS技术为细胞类型特异性的单神经元连接网络图谱绘制提供了强大技术支持。
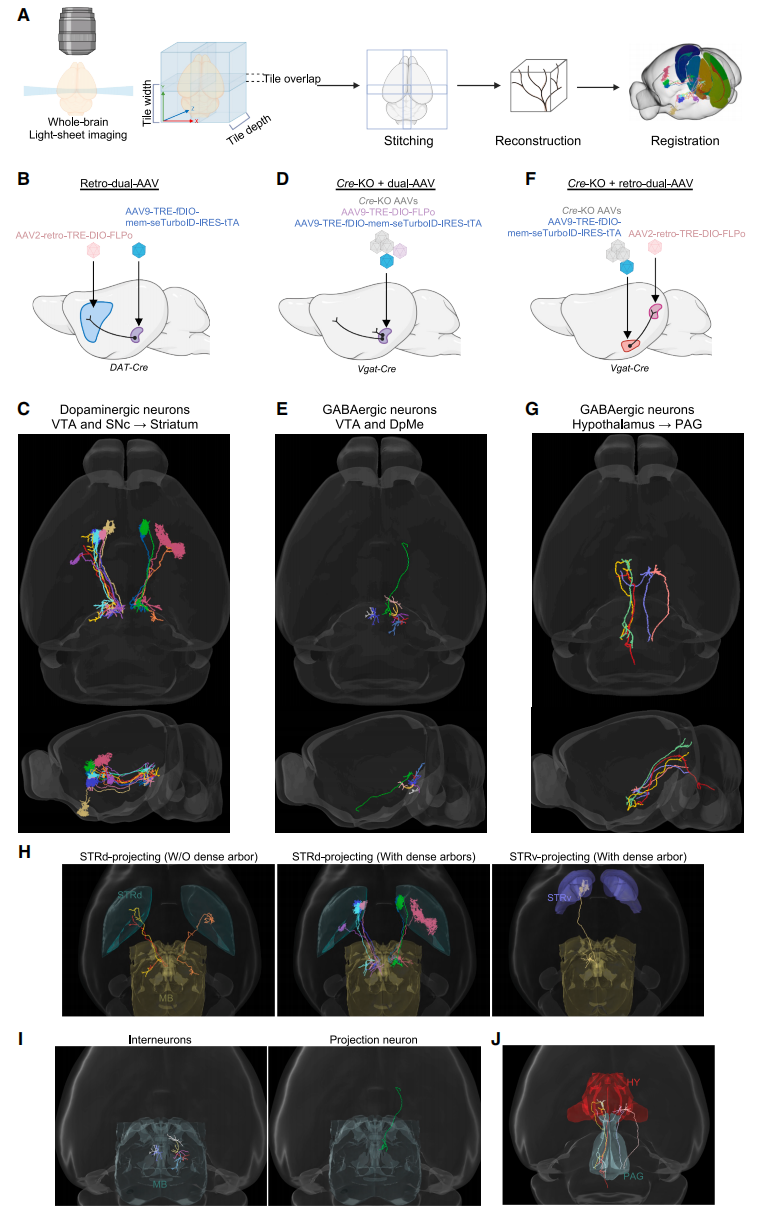
图六 基于LINCS稀疏标记的全脑单神经元重构[9]
综上所述,该研究开发的LINCS化学染料标记技术,通过将工程化可溶性增强型生物素连接酶与单价链霉亲和素配对,构建了高效通用的神经解剖学研究平台,成功突破了神经解剖图谱绘制在标记速度、信号强度、以及可扩展性方面的关键瓶颈。LINCS技术在群体水平绘制神经连接图谱中表现卓越,成功实现脊髓及外周神经系统神经环路的三维可视化。进一步将LINCS与CRISPR-Cas9技术介导Cre基因敲除的稀疏标记策略相结合,可建立稳定易行的全脑单神经元形态分析工作流程,成功实现全脑多类型的单神经元重构。与当前最先进的切片平台相比,LINCS技术显著提升了单神经元重构的效率与可及性,同时降低了成本。配套使用标准商用光片显微镜,可省去样本切片的繁琐步骤,使得单神经元追踪无需依赖专业的大规模成像设备即可实施。该研究基于LINCS技术,构建了可靠且可扩展的神经连接图谱绘制流程,为加速哺乳动物神经回路的解剖学与机制研究提供了有力支持。

GTP研发中心负责实施基因组标签计划(Genome tagging project, GTP),基于自主知识产权的类精子干细胞介导半克隆技术,为全基因组的功能基因一一贴上标签,致力于构建标签细胞和标签小鼠资源库。类精子干细胞是从精子来源单倍体囊胚中建系获得的一种孤雄单倍体胚胎干细胞,将其注入卵母细胞,能够像精子一样支持整个胚胎发育过程,产生健康的半克隆小鼠。GTP研发中心在类精子干细胞的蛋白质编码基因上原位敲入标签序列,建立了液氮保存的标签细胞资源库。研究需要时,利用半克隆技术将标签细胞注射到小鼠卵母细胞中,一步法获得标签小鼠。

已有标签产品可直接订购,详情查阅以下官网链接。如有需要欢迎联系,我们将竭诚为您服务。
标签细胞网址:
标签小鼠网址:
http://www.sibcb.ac.cn/gtp/msearch.jsp
地址:上海市岳阳路320号
责任编辑:甜点
新媒体运营:suway
参考文献
1. Muñoz-Castañeda R, Zingg B, Matho KS, Chen X, Wang Q, Foster NN, Li A, Narasimhan A, Hirokawa KE, Huo B et al: Cellular anatomy of the mouse primary motor cortex. Nature 2021, 598(7879):159-166.
2. Wang X, Xiong H, Liu Y, Yang T, Li A, Huang F, Yin F, Su L, Liu L, Li N et al: Chemical sectioning fluorescence tomography: high-throughput, high-contrast, multicolor, whole-brain imaging at subcellular resolution. Cell Rep 2021, 34(5):108709.
3. Qiu S, Hu Y, Huang Y, Gao T, Wang X, Wang D, Ren B, Shi X, Chen Y, Wang X et al: Whole-brain spatial organization of hippocampal single-neuron projectomes. Science 2024, 383(6682):eadj9198.
4. Dodt HU, Leischner U, Schierloh A, Jährling N, Mauch CP, Deininger K, Deussing JM, Eder M, Zieglgänsberger W, Becker K: Ultramicroscopy: three-dimensional visualization of neuronal networks in the whole mouse brain. Nat Methods 2007, 4(4):331-336.
5. Tian T, Yang Z, Li X: Tissue clearing technique: Recent progress and biomedical applications. J Anat 2021, 238(2):489-507.
6. Weiss KR, Voigt FF, Shepherd DP, Huisken J: Tutorial: practical considerations for tissue clearing and imaging. Nat Protoc 2021, 16(6):2732-2748.
7. Hui Y, Zheng X, Zhang H, Li F, Yu G, Li J, Zhang J, Gong X, Guo G: Strategies for Targeting Neural Circuits: How to Manipulate Neurons Using Virus Vehicles. Front Neural Circuits 2022, 16:882366.
8. Branon TC, Bosch JA, Sanchez AD, Udeshi ND, Svinkina T, Carr SA, Feldman JL, Perrimon N, Ting AY: Efficient proximity labeling in living cells and organisms with TurboID. Nat Biotechnol 2018, 36(9):880-887.
9. Zhong S, Zhang X, Gao X, Li Z, Huang L, Guo Q, Gong R, Ren J, Luo M, Lin R: Ultrabright chemical labeling enables rapid neural connectivity profiling in large tissue samples. Neuron 2025.
10. Jacobs BL, Azmitia EC: Structure and function of the brain serotonin system. Physiol Rev 1992, 72(1):165-229.
11. Gronenborn AM, Filpula DR, Essig NZ, Achari A, Whitlow M, Wingfield PT, Clore GM: A novel, highly stable fold of the immunoglobulin binding domain of streptococcal protein G. Science 1991, 253(5020):657-661.
12. Howarth M, Chinnapen DJ, Gerrow K, Dorrestein PC, Grandy MR, Kelleher NL, El-Husseini A, Ting AY: A monovalent streptavidin with a single femtomolar biotin binding site. Nat Methods 2006, 3(4):267-273.
13. Bäckman CM, Malik N, Zhang Y, Shan L, Grinberg A, Hoffer BJ, Westphal H, Tomac AC: Characterization of a mouse strain expressing Cre recombinase from the 3' untranslated region of the dopamine transporter locus. Genesis 2006, 44(8):383-390.
14. Wang Q, Ding SL, Li Y, Royall J, Feng D, Lesnar P, Graddis N, Naeemi M, Facer B, Ho A et al: The Allen Mouse Brain Common Coordinate Framework: A 3D Reference Atlas. Cell 2020, 181(4):936-953.e920.
15. Lin R, Wang R, Yuan J, Feng Q, Zhou Y, Zeng S, Ren M, Jiang S, Ni H, Zhou C et al: Cell-type-specific and projection-specific brain-wide reconstruction of single neurons. Nature methods 2018, 15(12):1033-1036.



