技术分享:小鼠胚胎活体成像技术IMEE的开发及其应用
哺乳动物大脑皮层是一个复杂且高度有序的结构,由兴奋性谷氨酸能神经元、抑制性GABA能神经元、以及非神经元细胞如大胶质细胞、免疫细胞及内皮细胞共同构成[1, 2]。建立精准的神经元时空分布以及免疫细胞小胶质细胞提供持续性保护,对于大脑皮层的发育至关重要[3, 4]。动态的细胞运动推动了神经元的迁移与小胶质细胞的监视功能[5]。然而,迁移中的中间神经元是如何在局部微环境中与非神经元细胞如内皮细胞和小胶质细胞发生相互作用的,尚未在活体中得到充分研究。此外,胚胎期小胶质细胞在生理环境或应激下的动态运动也少有研究。
受限于现有观测细胞动态运动活体成像技术仍主要依赖于离体方法,传统急性脑切片成像因缺乏血流脱离了血液循环系统[6],以及脑组织切片制备过程会破坏中枢神经系统稳态,导致小胶质细胞在非生理性免疫反应中被激活[7]。另外,现有小鼠胚胎活体成像方法仍存在内部固定方法的观测稳定性差、视野受限及操作复杂的问题,以及外部固定方法因羊水排空破坏子宫内环境,仅有短暂观测窗口的局限性。因此,在体观测小鼠胚胎发育时期大脑中复杂的细胞运动行为面临重大挑战,亟需开发新的小鼠胚胎活体成像技术。
2025年12月,Cell期刊报道了一项研究,通过开发了体外固定胚胎活体成像技术IMEE,实现对小鼠胚胎进行长时程、大视野、深层次的活体成像,以及在视角灵活性、操作简易性和功能适用性方面表现卓越。通过将IMEE技术与血管标记注射及矢量场拓扑分析相结合,系统性表征了神经元迁移的差异化模式,以及在生理与应激条件下的神经元、免疫细胞与血管系统间的互作关系。该研究通过活体展示,揭示了细胞胞体与突触在不同胞外环境中的多样化运动模式,这对理解哺乳动物大脑发育过程中细胞迁移与免疫监视的环境适应性行为具有重要科学意义[8]。
首先,研究者开发了一款操作简易的装置,可在双光子显微镜下稳定固定小鼠胚胎大脑,实现连续性的活体成像,称为体外固定胚胎活体成像技术(IMEE,图一)。IMEE装置能为不同体型的孕鼠提供稳定性支撑、恒温的环境与持续性气体麻醉(图一A),其核心固定组件包含了环形卡盘与载物平台。通过持续泵入卡盘与载物平台的恒温水流,装置内的水循环系统能够维持胚胎周围微环境的适宜温度(图一B)。附着在载物平台底部的PU薄膜为胚胎提供向上支撑力,通过注射器抽取预温生理盐水产生的负压使得胎膜在环形卡孔处轻微隆起,形成密封(图一C)。凭借装置的灵活适配性,IMEE可长时程的兼容从胚胎期E10.5天至E16.5天的产前发育观测窗口,并同时支持侧视和顶视两种观测角度(图一D)。针对不同发育阶段的胚胎适配对应尺寸的卡盘,还能在单次孕鼠手术中便捷实现不同胚胎的快速切换。此外,在卡盘与载物平台间灌注琼脂糖,为胚胎提供周围支撑,通过双光子显微镜筛选具有阳性荧光信号的胚胎进行长时程成像(图一E)。由于羊膜结构保持完整,IMEE装置可在整个长时程成像期间维持恒定的温度与湿度,不会干扰胚胎的正常发育,实时拍摄活体胚胎脑皮质实质内的荧光信号。在此过程中,激发光需依次穿透胎膜、头皮及脑膜等多重光学屏障(图一F),获取的独立图像序列可进行拼接整合,从而获得大视野图像数据集(图一G)。通过将局部影像数据映射至三维重建的全脑模型,可精确定位小范围图像采集区域的空间位置(图一H),以及观测深达约900 μm脑实质的荧光信号(图一I)。
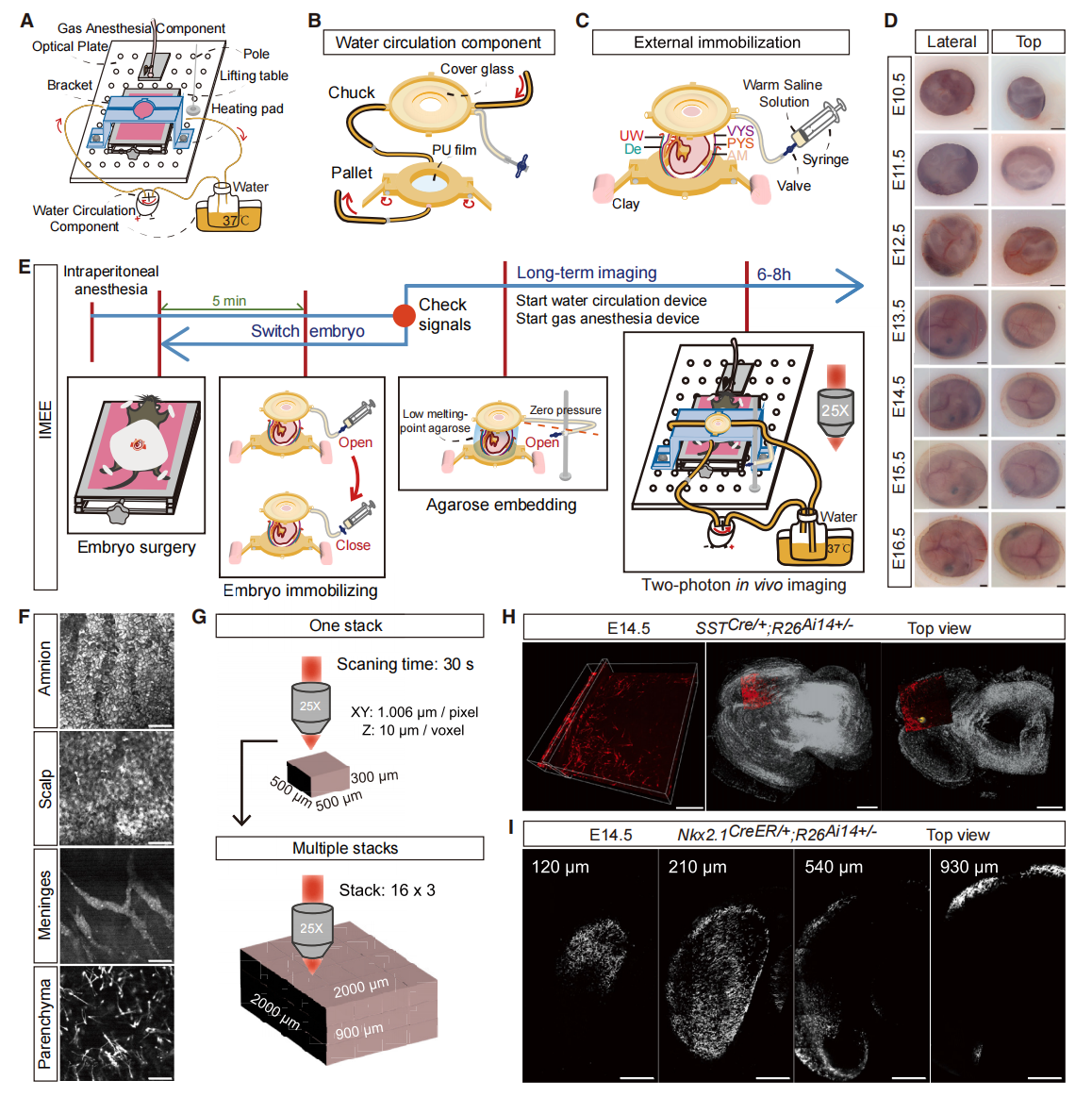
图一 体外固定胚胎活体成像技术IMEE[8]
既往利用急性脑切片延时成像技术的研究表明,新生兴奋性神经元在从皮层生发区向软脑膜表面进行径向迁移的过程中,在进入皮层板前经历多极化迁移阶段,而在进入皮层板后则采用位移运动或胞体转运模式继续迁移(图二A)。然而,兴奋性神经元这种多样化的迁移模式尚未在活体环境中被系统性表征。于是,研究者通过他莫昔芬诱导的Emx1CreERT2/+; R26Ai14+/−小鼠胚胎,对稀疏标记的皮层兴奋性神经元进行IMEE观测(图二B)。通过侧视角观测,在皮层板内同时观察到胞体转运和位移运动型迁移的兴奋性神经元,前者沿径向移动时,其突起的末端分支持续锚定于软脑膜表面(图二C),而后者则具有未达软脑膜表面的无分支突起(图二D)。部分神经元在趋近软脑膜侧时会从位移运动模式切换为胞体转运模式(图二E)。在发育早期与晚期阶段,位移运动型神经元的平均迁移速度均显著慢于胞体转运型神经元,且不同发育阶段间迁移速度未出现显著变化(图二F)。通过顶视角观测,对皮层板下方进行多极迁移的神经元细胞动力学特征进行分析,发现其胞体在5小时观测窗口内保持相对稳定,而神经元突起则持续进行延伸与回缩的动态变化(图二G和H)。IMEE具有广泛适用性,可与胚胎发育研究中常用的其他技术兼容。例如与子宫内电转技术相结合,可在活体环境中成功观测到兴奋性神经元迁移模式的动态转变过程(图二I-K)。以上数据不仅揭示了兴奋性神经元进入皮层板前后不同迁移模式的活体特征,同时展现了IMEE在观测胚胎发育过程中细胞动态运动方面的强大能力。
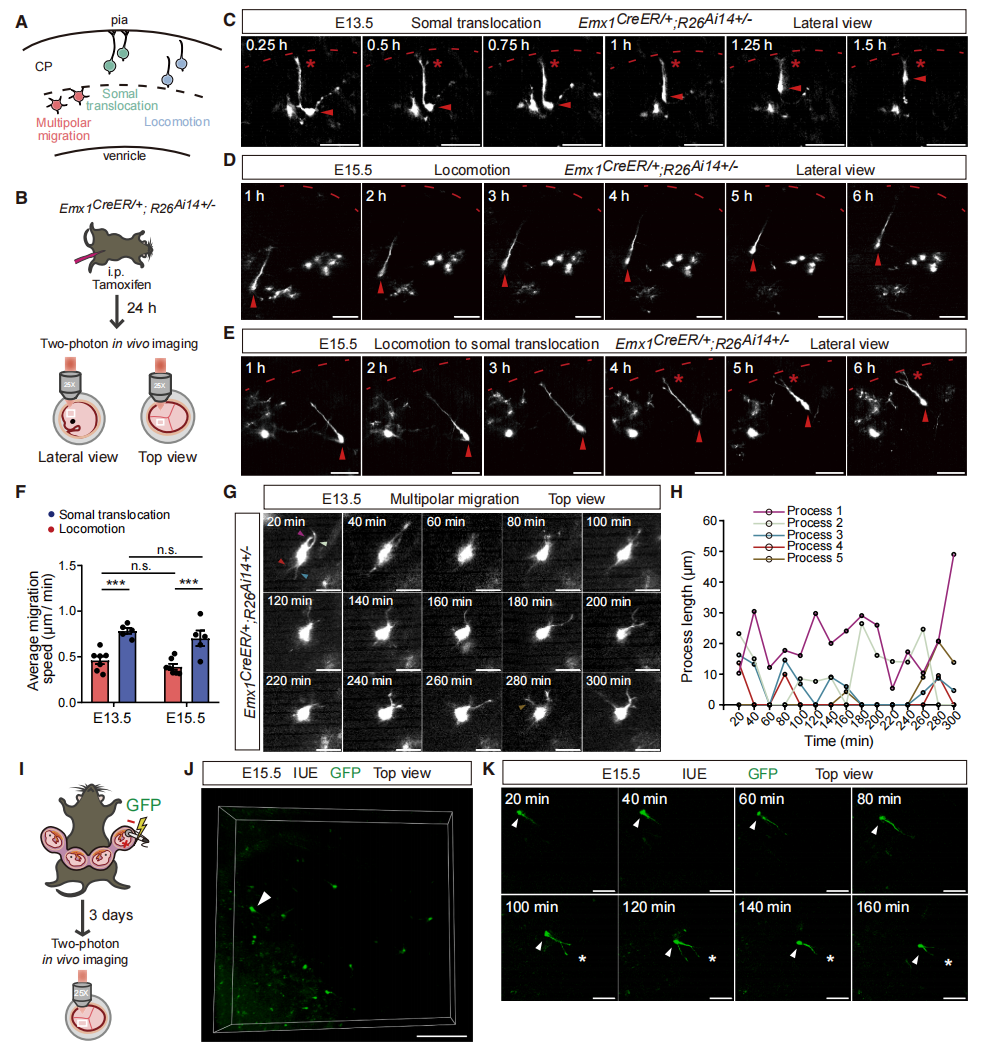
图二 IMEE揭示发育中小鼠大脑皮层内皮质兴奋性神经元的动态迁移模式[8]
与兴奋性神经元不同,皮层中间神经元起源于端脑腹侧区域,主要来自内侧神经节隆起[9]。这些神经元最初通过特定迁移流在皮层内进行切线方向迁移,包括穿行边缘带(MZ)的表层迁移路径,以及穿行脑室下区(SVZ)的深层迁移路径[10]。于是研究者在活体环境中探究皮层中间神经元的切向迁移模式。将纯合致死的Nkx2.1CreER+/−小鼠与R26Ai14+/+小鼠杂交,在IMEE观测中筛选E14.5胚胎,直至获得Nkx2.1CreER+/−; R26Ai14+/−目标基因型胚胎。经他莫昔芬诱导后,可见内侧神经节隆起来源的皮层中间神经元,包括表达生长抑素和表达小清蛋白的中间神经元被密集标记(图三A)。以20分钟为间隔采集完整胚胎大脑皮层半球的延时图像序列,并基于边界结构与非特异性血管信号进行运动校正(图三B)。通过叠加相邻时间点的图像序列,发现大量中间神经元的胞体沿其引导突起方向移动(图三C)。值得注意的是,MZ中间神经元呈现无序的缠结运动模式,而SVZ中间神经元则表现出有序的定向迁移(图三C)。为量化这些差异,以20分钟间隔对中间神经元进行长达1小时的迁移轨迹建模(图三D),并将其投影至平行于成像平面的二维空间以描述其切向迁移特征。结果显示,无论是在三个时间点取平均值(图三E)还是分别检验各时间点,MZ与SVZ中间神经元的迁移方向分布均存在显著差异,前者迁移方向呈现平峰分布,而后者则表现出尖峰分布(图三E)。进一步量化单个中间神经元的角速度与线速度,发现这两种中间神经元在这两项参数上均无显著差异(图三F和G)。
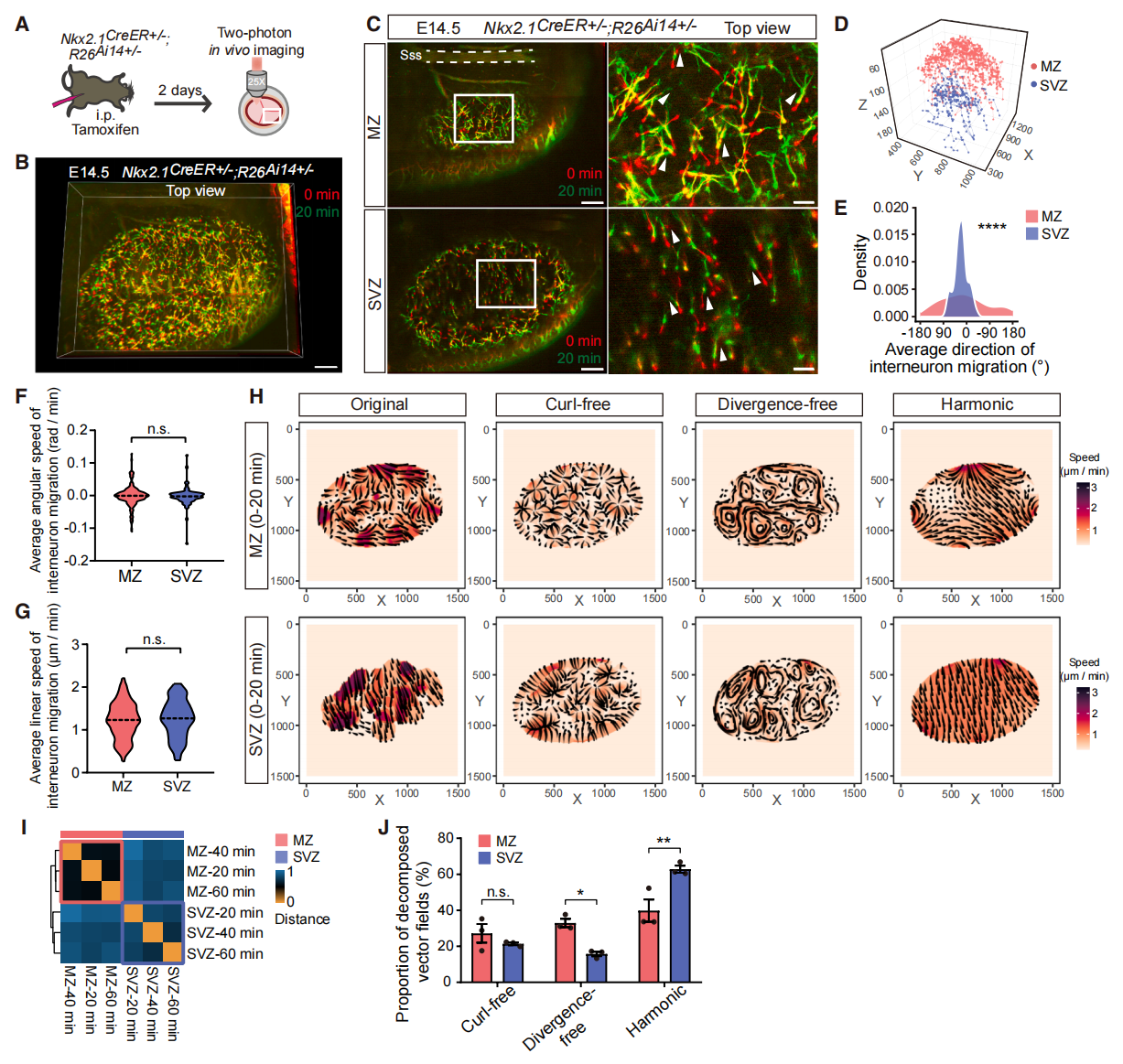
图三 IMEE表征发育中小鼠大脑皮层中间神经元切向迁移[8]
为深入解析中间神经元的迁移模式,研究者基于投射至二维平面的神经元迁移轨迹,以20分钟为间隔构建速度场(图三H)。通过对不同时间点的速度场进行聚类分析,发现各迁移路径内部存在对应规律(图三I)。运用亥姆霍兹-霍奇分解法,将原始速度场分解为三个正交分量:无旋矢量场、螺线矢量场及调和矢量场(图三H)。分析发现,代表均匀群体运动的调和矢量场在SVZ更为显著(图三J)。相比之下,代表螺旋式群体运动的螺线矢量场在MZ贡献更大,而代表辐射状与汇聚式群体运动的无旋矢量场在两条路径间无显著差异(图三J),表明MZ中间神经元异质性的群体运动主要源于直线型群体运动的减弱与螺旋型群体运动的增强。以上数据表明,通过两条路径迁移的皮层中间神经元的迁移模式存在显著差异,MZ路径呈现以螺旋式群体运动为主的异质性迁移,而SVZ路径则表现为以直线型群体运动为主的同质性迁移。
调控中间神经元迁移轨迹的一种潜在机制,涉及在局部微环境中与非神经元细胞的动态相互作用。为活体观察中间神经元与血管系统的相互作用,研究者在Nkx2.1CreER+/−; R26Ai14+/−胚胎中对内侧神经节隆起来源的皮层中间神经元及脑血管系统进行标记(图四A),随后以5-8分钟间隔从顶视角采集大视野图像(图四B)。基于活体观测结果,依据引导突起的动态特征,将神经元-血管相互作用划分为三种模式:1)1型末端接触(TC1),引导突起末端接触血管表面后发生分支回缩;2)2型末端接触(TC2),末端接触血管后单根引导突起发生分叉;以及3)突起接触(PC),引导突起与血管持续相互作用,使神经元沿血管表面单向滑移(图四C和D)。通过荧光强度与空间关联的共定位分析及三维重建技术,验证了这些直接的细胞间接触(图四E-J)。为系统性表征神经-血管相互作用对迁移中神经元的影响,研究者追踪了中间神经元的迁移轨迹(图四L),并量化其在接触期间及接触后的迁移方向与速度。值得注意的是,所有接触模式均显著减缓神经元迁移速度(图四M),其中TC1与TC2模式产生的减速效应强于PC模式(图四N)。TC1与TC2接触后,神经元还表现出显著的迁移方向偏转(图四K)。这种偏转源于两种机制:TC1模式下引导突起分支回缩使神经元能重新定向沿其他已存在的分支迁移,TC2模式下引导突起分叉促使神经元跟随新生成的分支调整方向(图四D)。相比之下,PC模式接触后神经元沿血管表面滑移时轨迹偏转极小,同时伴随胞体形态改变(图四D和K)。以上结果表明,在小鼠皮层发育过程中,迁移中的中间神经元通过特定的接触调控行为来适应局部微环境,实现远离血管的精准导航。
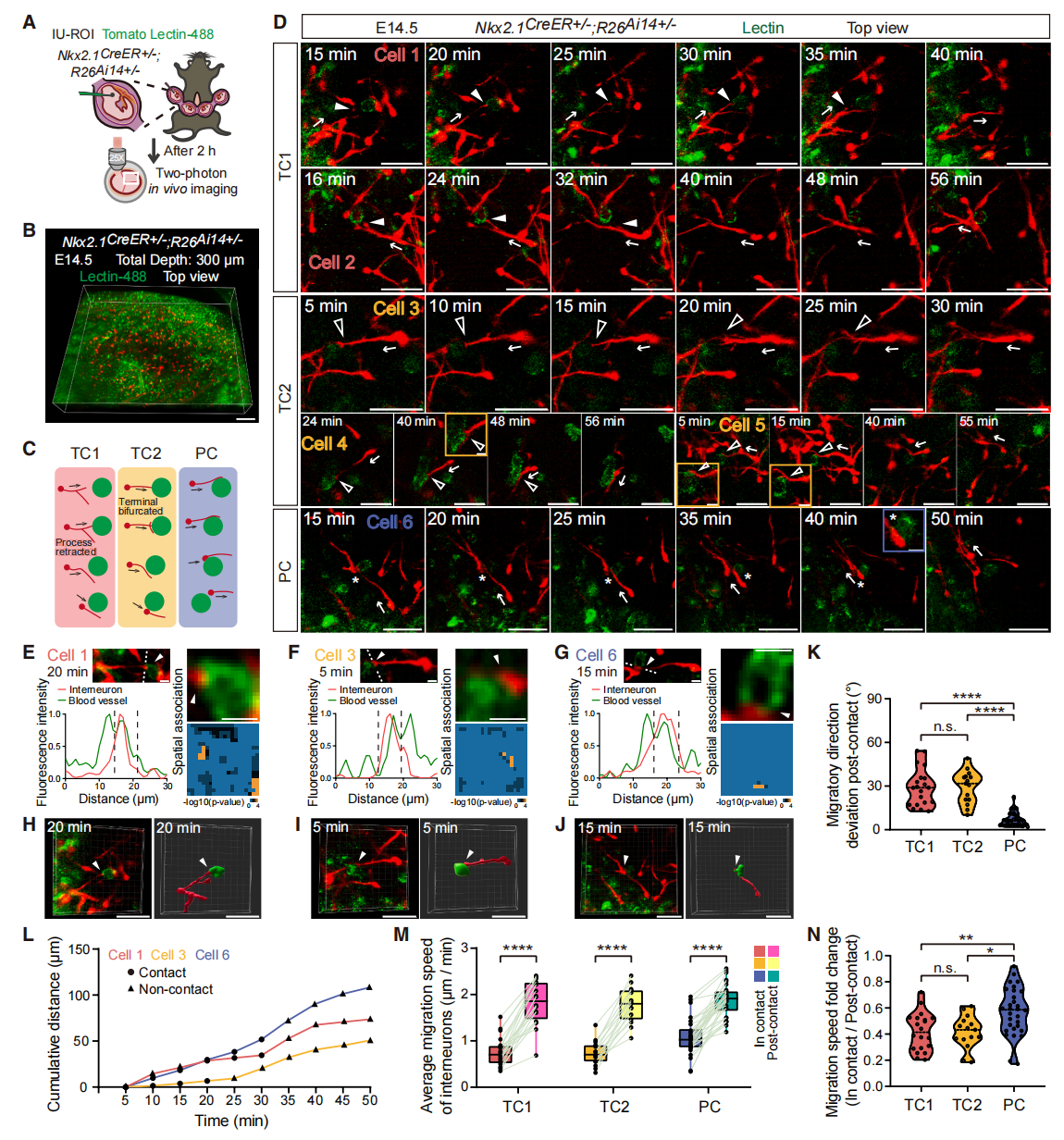
图四 IMEE表征发育中小鼠大脑皮层内迁移中间神经元与血管相互作用[8]
类似地,研究者在体观察中间神经元与小胶质细胞的相互作用,发现两者也存在相似的TC和PC接触模式,小胶质细胞在与迁移的中间神经元接触后也会缩回其突起,表明它们具备动态感知与响应环境的能力。静息态小胶质细胞具有高度活跃的突起,不仅对神经元细胞实施监测功能[11],同时也对血管进行监控[12]。根据其胞体在脑实质中的定位,小胶质细胞可进一步分为实质小胶质细胞(PCM)和毛细血管关联小胶质细胞(CAM),后者的胞体直接位于血管上[13]。为探究两类小胶质细胞的动态运动特征,研究者在标记小胶质细胞的Cx3cr1GFP+/-胚胎期E14.5天进行颅内长时程活体成像,同时成像前2小时通过子宫内眶后注射(IU-ROI)标记脑血管系统(图五A)。随后以10分钟间隔采集大视野图像(图五B)。研究发现,尽管部分小胶质细胞沿其引导突起迁移,但几乎所有被认定为静息状态的分支状小胶质细胞,都通过其精细细胞突起的持续运动主动扫描细胞外环境(图五C)。通过三维重建与表面渲染技术,确认CAM定位于血管系统,其突起在血管周围呈探查性运动(图五D和E)。进一步解析小胶质细胞突起随时间的动态扫描行为,从60分钟观察窗口内每10分钟采集的在体图像中,提取了PCM与CAM的形态学特征。随后基于光流法,根据每个小胶质细胞在相邻时间点的形态学特征构建原始矢量场(图五F和G)。通过对单个小胶质细胞进行矢量场拓扑(TVF)分析,发现与CAM相比,PCM中无旋矢量场的贡献度更高,证实PCM的突起具有更显著的伸缩运动,而代表突起探查性运动的螺线矢量场在两类细胞间则无显著差异(图五H)。根据无旋矢量场对原始矢量场的贡献度分析,在同一类型小胶质细胞内发现了明确的对应关系(图五I)。以上结果揭示了胚胎期静息态小胶质细胞在监测脑实质与血管时会采用不同模式的细胞突起运动方式,表明其能够根据不同的细胞外环境采取适应性的细胞行为。
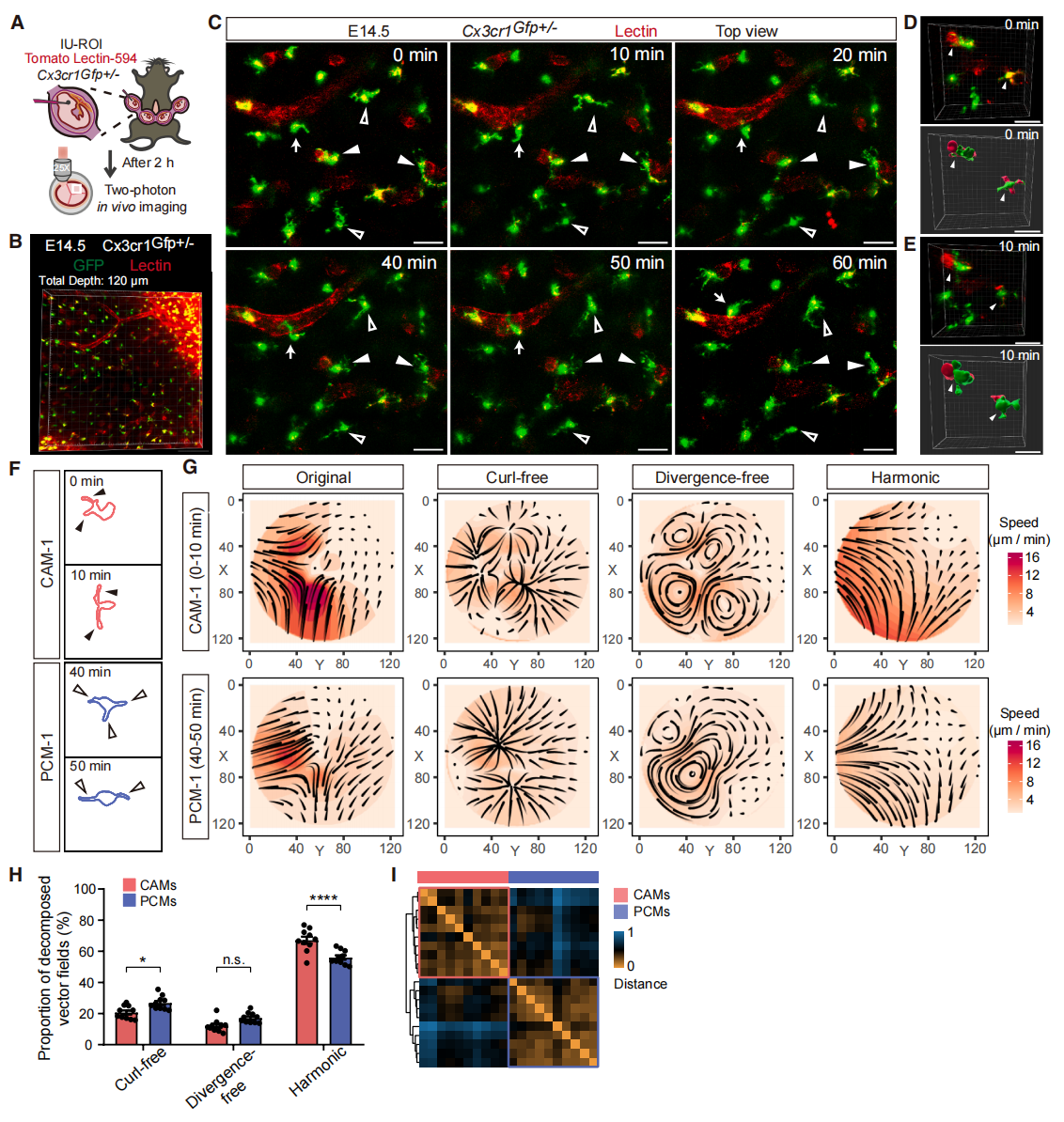
图五 IMEE表征发育中小鼠大脑皮层内PCM与CAM的动态扫描行为[8]
静息态小胶质细胞持续监测大脑,并响应环境应激而迅速激活。为研究它们在胚胎发育期间如何响应环境应激,研究者在Cx3cr1GFP+/-胚胎期E14.5天实施皮层子宫内损伤,30分钟后进行颅内长时程活体成像,并以5分钟间隔采集损伤部位的图像(图六A和B)。距离损伤部位最远350 μm处的小胶质细胞迅速被募集,以平均每分钟2.3 ± 0.7 μm的速度向损伤部位迁移(图六C、D、F和G)。单个小胶质细胞的迁移速度随时间变化,最高速度达每分钟10.8 μm(图六H)。研究发现,小胶质细胞呈现典型的迁移形态,通过特化的引导突起定向迁移至损伤部位(图六E)。有趣的是,小胶质细胞抵达损伤部位后,其突起会发生收缩并趋于静息状态(图六E),表现为长度和运动活性的显著下降(图六I和J),表明小胶质细胞在损伤部位向激活状态转变。此外,在损伤部位小胶质细胞内观察到密集的纤维连接蛋白,提示这些被募集的小胶质细胞在环境应激下具有吞噬和组织修复功能。通过对活体成像后的脑组织进行三维重建和免疫染色,获得了小胶质细胞在整个胚胎脑内的聚集定位,并进一步证实损伤部位的募集细胞主要为P2Y12阳性小胶质细胞(图六K和L)。以上结果表明,胚胎期小胶质细胞能快速从静息状态转变为定向迁移以响应环境应激,并在损伤部位呈现激活状态,从而促进组织保护和稳态恢复。
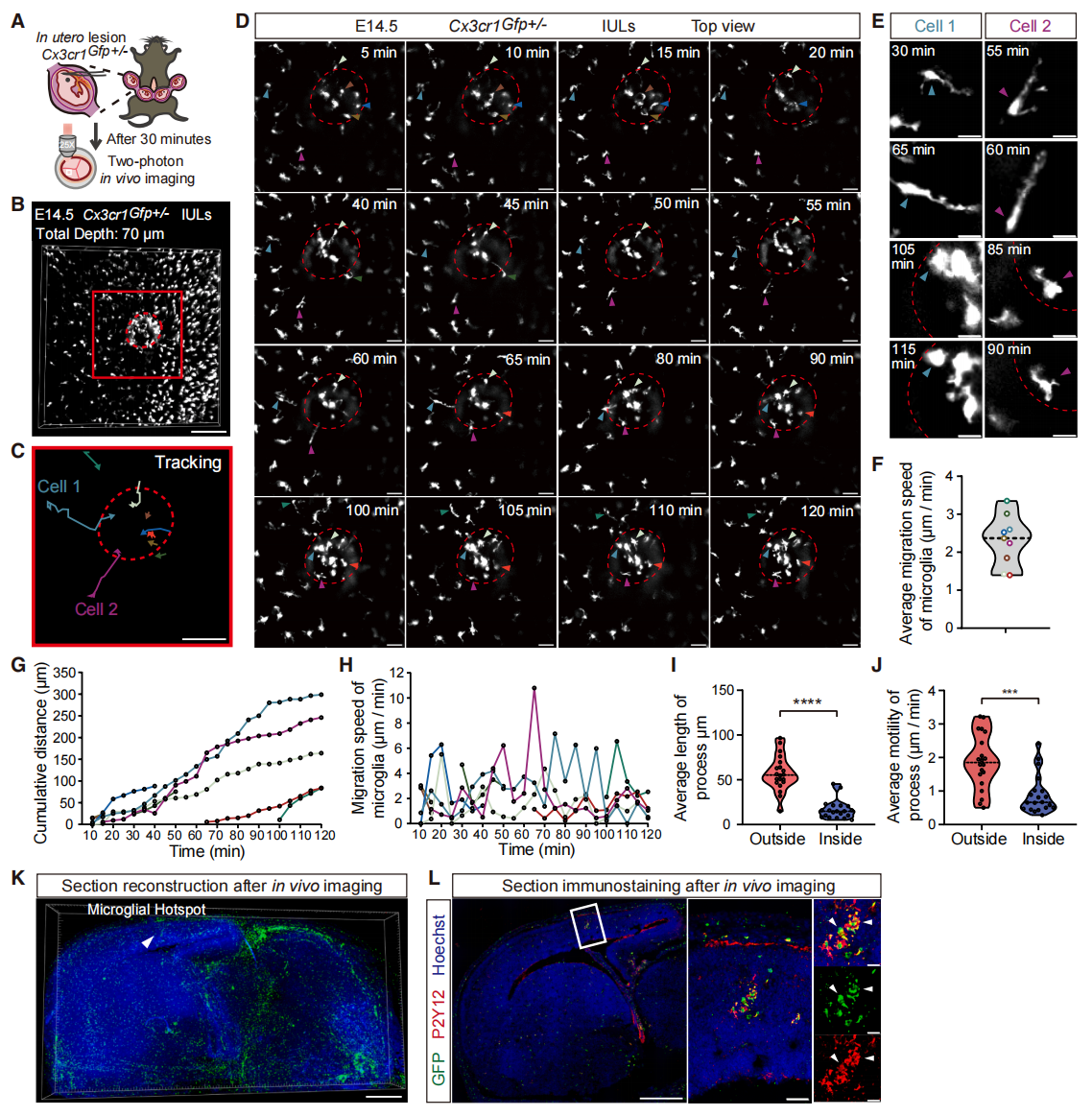
图六 IMEE揭示发育中小鼠大脑皮层内小胶质细胞募集与活化[8]
综上所述,该研究建立了具有高稳定性、灵活视角、操作简易和广泛应用特点的小鼠胚胎长时程活体成像方法IMEE,能实现胚胎颅内的长时程、大视野、深层次活体成像。利用IMEE,研究者探究了小鼠大脑发育过程中的细胞动态行为,包括神经元迁移模式、神经元与血管系统及小胶质细胞的动态相互作用,以及在生理条件和环境应激下小胶质细胞的监视行为,揭示了神经元的迁移导向与免疫监视功能均依赖于细胞通过胞体或突触的特定运动模式对局部环境产生适应性调整。该研究革新了小鼠胚胎活体成像技术,将发育生物学研究从静态切片模式推向三维动态观测模式,为理解哺乳动物胚胎发育中的神经-血管-免疫系统互作与协同发育机制开辟了全新的观测范式。

GTP研发中心负责实施基因组标签计划(Genome tagging project, GTP),基于自主知识产权的类精子干细胞介导半克隆技术,为全基因组的功能基因一一贴上标签,致力于构建标签细胞和标签小鼠资源库。类精子干细胞是从精子来源单倍体囊胚中建系获得的一种孤雄单倍体胚胎干细胞,将其注入卵母细胞,能够像精子一样支持整个胚胎发育过程,产生健康的半克隆小鼠。GTP研发中心在类精子干细胞的蛋白质编码基因上原位敲入标签序列,建立了液氮保存的标签细胞资源库。研究需要时,利用半克隆技术将标签细胞注射到小鼠卵母细胞中,一步法获得标签小鼠。

已有标签产品可直接订购,详情查阅以下官网链接。如有需要欢迎联系,我们将竭诚为您服务。
标签细胞网址:
标签小鼠网址:
http://www.sibcb.ac.cn/gtp/msearch.jsp
地址:上海市岳阳路320号
责任编辑:多一百
新媒体运营:suway
参考文献
1. Rakic P: Evolution of the neocortex: a perspective from developmental biology. Nature reviews Neuroscience 2009, 10(10):724-735.
2. Molnár Z, Clowry GJ, Šestan N, Alzu'bi A, Bakken T, Hevner RF, Hüppi PS, Kostović I, Rakic P, Anton ES et al: New insights into the development of the human cerebral cortex. Journal of anatomy 2019, 235(3):432-451.
3. Silva CG, Peyre E, Nguyen L: Cell migration promotes dynamic cellular interactions to control cerebral cortex morphogenesis. Nature reviews Neuroscience 2019, 20(6):318-329.
4. Hattori Y: The multifaceted roles of embryonic microglia in the developing brain. Frontiers in cellular neuroscience 2023, 17:988952.
5. Nadarajah B, Alifragis P, Wong RO, Parnavelas JG: Neuronal migration in the developing cerebral cortex: observations based on real-time imaging. Cerebral cortex (New York, NY : 1991) 2003, 13(6):607-611.
6. Humpel C: Organotypic brain slice cultures: A review. Neuroscience 2015, 305:86-98.
7. Stence N, Waite M, Dailey ME: Dynamics of microglial activation: a confocal time-lapse analysis in hippocampal slices. Glia 2001, 33(3):256-266.
8. Long Z, Yu Y, He C, Xu L, Yan Y, Li Z, Guo ZV, Mi D: Intravital observation of neuronal and immune cell dynamics in the developing mammalian brain. Cell 2025.
9. Wonders CP, Anderson SA: The origin and specification of cortical interneurons. Nature reviews Neuroscience 2006, 7(9):687-696.
10. Lim L, Mi D, Llorca A, Marín O: Development and Functional Diversification of Cortical Interneurons. Neuron 2018, 100(2):294-313.
11. Nimmerjahn A, Kirchhoff F, Helmchen F: Resting microglial cells are highly dynamic surveillants of brain parenchyma in vivo. Science 2005, 308(5726):1314-1318.
12. Mondo E, Becker SC, Kautzman AG, Schifferer M, Baer CE, Chen J, Huang EJ, Simons M, Schafer DP: A Developmental Analysis of Juxtavascular Microglia Dynamics and Interactions with the Vasculature. J Neurosci 2020, 40(34):6503-6521.
13. Bisht K, Okojie KA, Sharma K, Lentferink DH, Sun YY, Chen HR, Uweru JO, Amancherla S, Calcuttawala Z, Campos-Salazar AB et al: Capillary-associated microglia regulate vascular structure and function through PANX1-P2RY12 coupling in mice. Nature communications 2021, 12(1):5289.



