技术分享:突触小泡“吻-缩-逃”实现胞吐与超快速回收
大脑功能的发挥有赖于神经元之间的信息传递。这一过程通过突触小泡(SV)的胞吐作用完成,当突触前动作电位(AP)产生时,小泡会释放神经递质[1, 2]。过去数十年的电生理学研究已揭示突触小泡胞吐过程中包含的一系列快速事件,包括停靠、融合孔形成等步骤,这些过程均在毫秒级时间内完成[3]。关于突触小泡的胞吐与回收机制,学界主要提出两种模型:“吻-逃”与“全融合”模型。在“吻-逃”模型中,融合孔短暂开启释放神经递质后立即关闭,囊泡可被回收再利用[4]。而在“全融合”模型中,囊泡则完全塌陷融入质膜[5]。相较而言,“吻-逃”模型被认为具有更高能量效率,更能支持高频率的突触传递。然而,囊泡释放过程发生在毫秒时间尺度,且结构变化处于纳米空间尺度,因技术手段的限制,使得关于这两种模型的争议长期悬而未决。
2025年10月,Science期刊报道了一项研究,通过自主研发的光遗传学耦合毫秒级时间分辨冷冻电子断层扫描技术,破解了神经信息传递过程中,突触小泡释放与快速回收的生物物理过程——“吻-缩-逃/全融合”。具体来说,在突触激活后4 ms内,突触小泡与质膜发生瞬时“亲吻”,形成直径约4 nm的脂质融合孔,其两侧可见SNARE蛋白复合体;随后迅速“收缩”至原表面积的一半;至70 ms时,多数收缩小泡通过“逃离”途径完成循环,其余小泡则塌陷全融合入突触前膜;100 ms后,超速内吞作用开始回收扩张的突触前膜。该研究发现“吻-缩-逃”是海马体突触中突触小泡胞吐与快速循环的主导生物物理机制。该机制成功调和了“吻-逃”与“全融合”这两种神经传递模型之间的矛盾,为突触传递的高效性与精确性提供了统一解释[6]。
近年来,具有纳米级空间分辨率的冷冻电子断层扫描技术(cryo-ET)已被应用于研究突触超微结构,揭示了囊泡与质膜相互作用的精细特征[7]。于是,研究者首先采用细胞冷冻电镜断层扫描技术(cryo-ET),对培养在多孔碳包被金载网上的大鼠海马体神经元完整突触进行成像,并按照既定流程获得了分子分辨率级别的三维重构结构(图一A和B)。在扫描图像中,突触的识别依据以下特征结构:包括两个紧密相邻的区室,一个是富含囊泡的区域,另一个区室与宽度相对均匀的突触间隙相邻,该间隙内可见跨间隙蛋白质密度分布(图一A-D)。根据既往关联成像研究确立的标准,进一步将突触分类为兴奋性与抑制性,主要关注兴奋性突触。在突触间隙与突触后致密区(PSD)相对的位置,被称为活性区(AZ)的突触前膜区域是突触小泡(SV)停靠与融合的位点。传统电镜成像中显著的AZ致密突起在图像中不明显(图一A)。因此研究者根据宽度均匀的突触间隙下方区域来划定AZ边界,并将紧邻AZ下方约20 nm的胞质层定义为膜下AZ带,该区域容纳了大多数膜相互作用的SV,可能对应即刻可释放池(图一A-F)。通过量化SV尺寸,发现AZ带内多数SV明显小于突触前末梢内远离该区域的小泡(图一C-I)。整体而言,AZ带内SV尺寸分布呈现两个独立的高斯峰:一个峰值对应平均直径29 nm,另一个峰值位于41 nm,后者正是AZ带外大部分囊泡的典型尺寸(图一E和G)。以两个高斯曲线交点34 nm为界,将SV划分为两个尺寸组别(图一G)。在AZ带内,识别出四种主要SV类型:i)锚定囊泡,通过蛋白纤丝与突触前膜连接;ii)半融合囊泡,与突触前膜发生部分融合;iii)开孔囊泡,与质膜形成狭窄融合孔,颈部宽度小于22 nm;iv)Ω形囊泡,与质膜形成宽大融合孔,颈部宽度大于22 nm(图一H)。这些囊泡的尺寸与其类型高度相关,大多数锚定囊泡直径较大,而半融合、开孔及Ω形囊泡多数直径较小(图一I),表明其与质膜的直接相互作用可能与囊泡膜的损耗相关。
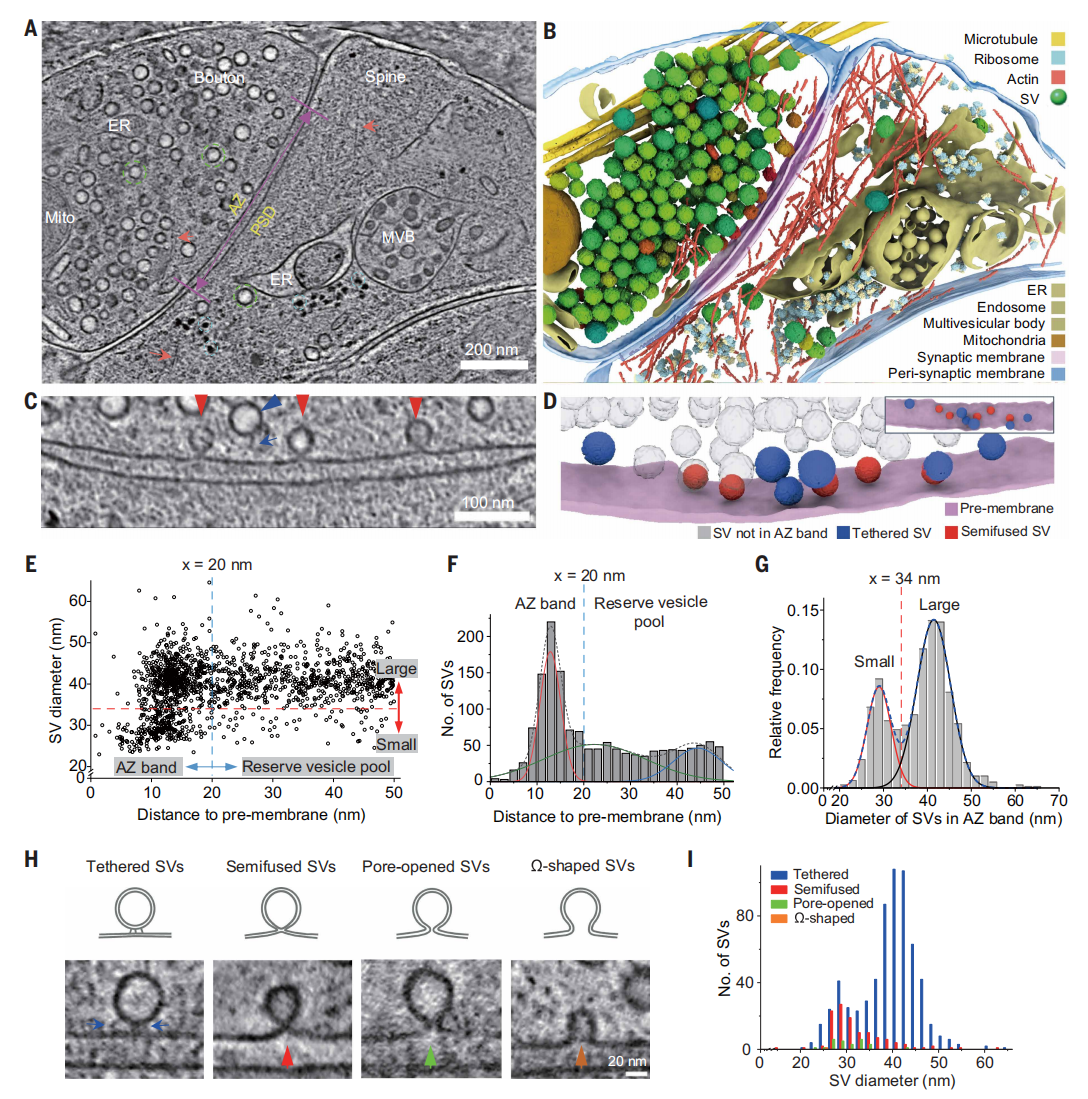
图一 原位cryo-ET显示基础状态下活性区附近存在的多种类型突触小泡[6]
为探究AZ带内不同类型的SV是否反映胞吐过程的不同阶段,以及确定该过程的时间顺序,研究者开发了时间分辨冷冻电镜技术(图二)。该方法通过光遗传学刺激触发动作电位(AP),随后进行毫秒级精度的骤冻处理(图二A)。使用通道视紫红质变体ChIEF转染神经元,并验证光刺激能有效诱发动作电位(图二B和C)。为抑制样本处理过程中神经元的自发性重复激活,应用CNQX阻断兴奋性传递[8]。采集了动作电位触发后约4、8、30及70 ms时间点冻结的突触冷冻断层图像(图二D-I)。观察到在动作电位后4 ms时半融合与开孔囊泡数量显著增加(图二K和L),表明这些囊泡的产生由动作电位触发。为探究半融合与开孔突触小泡的形成是否涉及膜融合机制,使用破伤风神经毒素(TeNT)处理神经元,该毒素通过切割SNARE复合体的关键组分突触短蛋白,从而阻断囊泡胞吐过程。TeNT完全阻断了半融合与开孔囊泡的形成(图二I、K和L),并在静息与光刺激突触中引起锚定囊泡的累积(图二J)。由此可见,动作电位触发的半融合与开孔囊泡形成需要功能性SNARE复合体参与。
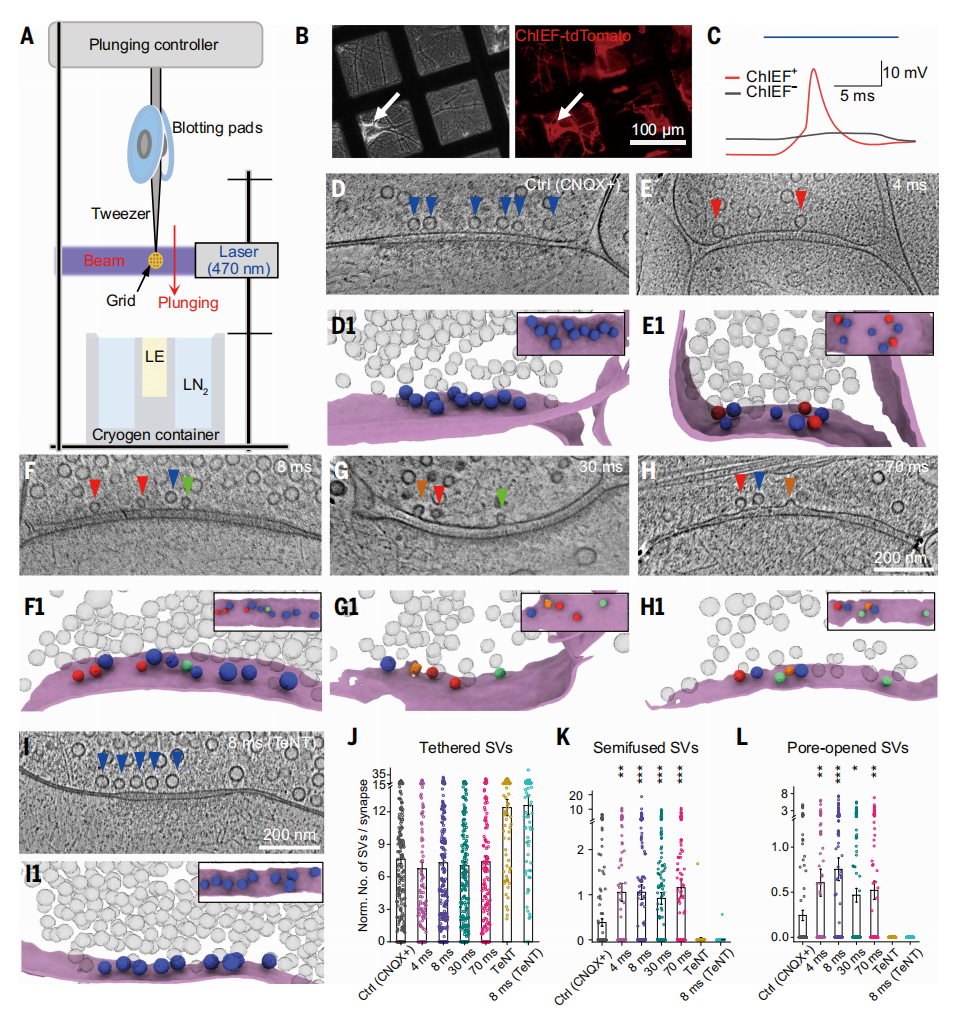
图二 毫秒级时间分辨率cryo-ET解析动作电位诱发的囊泡胞吐过程[6]
将半融合与开孔突触小泡划分为大、小两个亚群(图三A),观察到大型半融合小泡的数量在动作电位后4 ms达到峰值,随后逐渐减少,而大型开孔与小型开孔囊泡的数量在8 ms达到峰值,小型半融合小泡的数量则持续增加至70 ms(图三B)。这些趋势揭示了SV的状态转变:从大型半融合态(4 ms达顶峰)→大型开孔态(8 ms达顶峰)→快速转化为小型开孔态(8 ms达顶峰)→经融合孔闭合后缓慢转化为小型半融合态(持续增加至70 ms)。在大型半融合小泡中,囊泡膜与质膜凸起末端直接接触,形成称为“亲吻”的亚稳态中间体。继“亲吻”步骤后,融合孔打开,体现为大型开孔囊泡数量的增加。随后这些囊泡迅速收缩为小型开孔态,表面积缩减约一半,对应直径从41 nm减小至29 nm。进一步分析介导膜融合的分子机器。通过对大、小型半融合及开孔囊泡进行亚断层图平均化处理(图三C-F),清晰揭示了具有明确双层膜结构的融合孔,以及连接囊泡腔与胞外空间的直接通道(图三D和E)。该融合孔直径约4 nm,足以释放神经递质。在所有半融合与开孔囊泡的亚断层图结构中,发现在接触位点两侧存在微弱但持续存在的线性密度信号(图三C-F),这些密度特征很可能对应三联SNARE复合体的卷曲螺旋结构。总体而言,各SV亚群显著的时间动态特征,共同支持了SNARE依赖的“吻-缩”胞吐事件假说。在初始“亲吻”过程中,大型半融合囊泡可能由锚定囊泡转化而形成,随后的“收缩”过程中,大型开孔囊泡迅速转化为小型开孔囊泡,继而这些囊泡会在小型半融合状态“暂留”(图三G)。
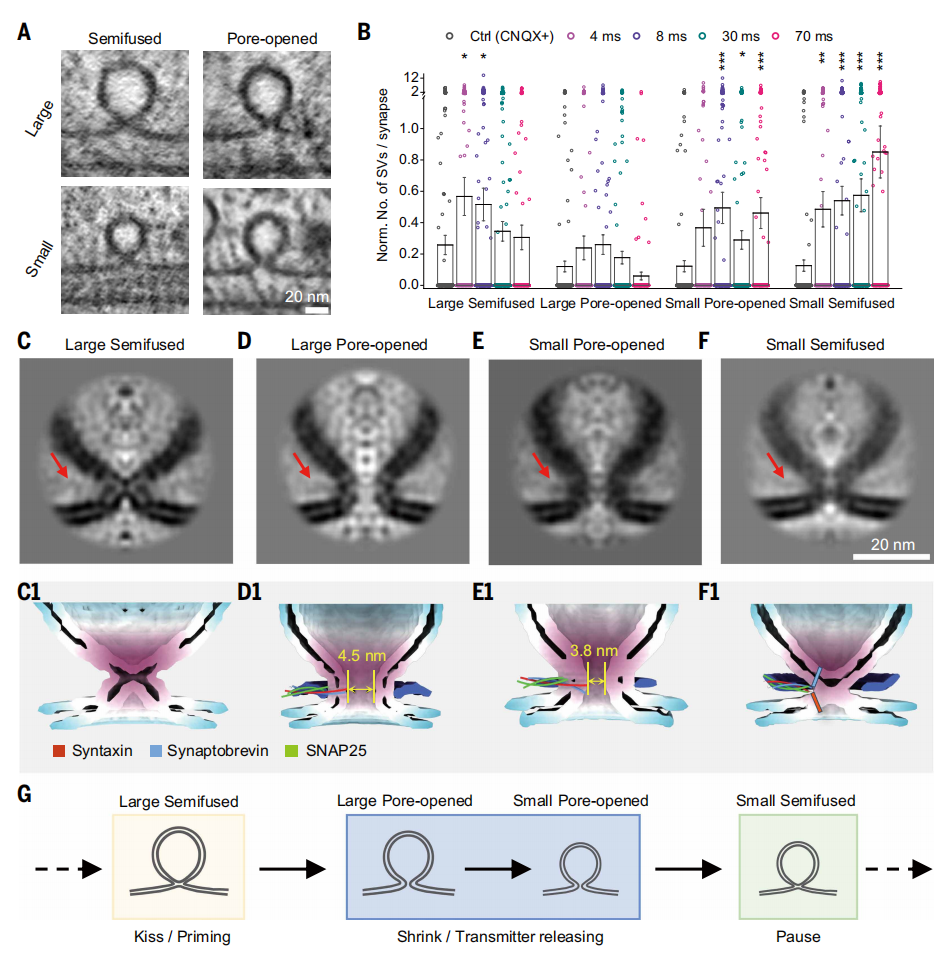
图三 突触小泡胞吐的“吻-缩”过程[6]
动作电位刺激后小型半融合小泡的累积现象引发研究者对它们后续命运的思考。AZ带内小型锚定囊泡的数量与动作电位后时间呈紧密正相关(图四A-C)。这些囊泡的数量在动作电位后约30 ms开始增加,并持续上升至70 ms之后,说明它们出现在小型半融合小泡之后(图四C),提示“吻-缩”后存在“逃离”途径,由此构成完整的“吻-缩-逃”胞吐-内吞循环路径。此外,在动作电位触发胞吐的后期阶段观察到囊泡塌陷全融合入突触前膜的现象,呈现Ω形或凹坑状形态(图四D和E)。这些塌陷囊泡多数为小型,其尺寸与小型半融合或开孔囊泡相当(图四F)。从时间维度看,大多数塌陷囊泡出现在动作电位后约70 ms,即在小型开孔囊泡数量增加之后,提示存在“吻-缩-全融合”路径。在动作电位后的所有时间点,与遵循逃离路径的囊泡相比,塌陷囊泡的数量始终只占总量的很小部分(图四G)。由此可见,“吻-缩-逃”似乎是海马体突触中突触小泡胞吐与回收的主导机制。通过捕捉“吻-缩-逃”与“吻-缩-全融合”全过程,将形态学定义的大/小锚定态、半融合态及开孔态囊泡,与既往定义的停靠及预激活囊泡状态相关联(图四H)。
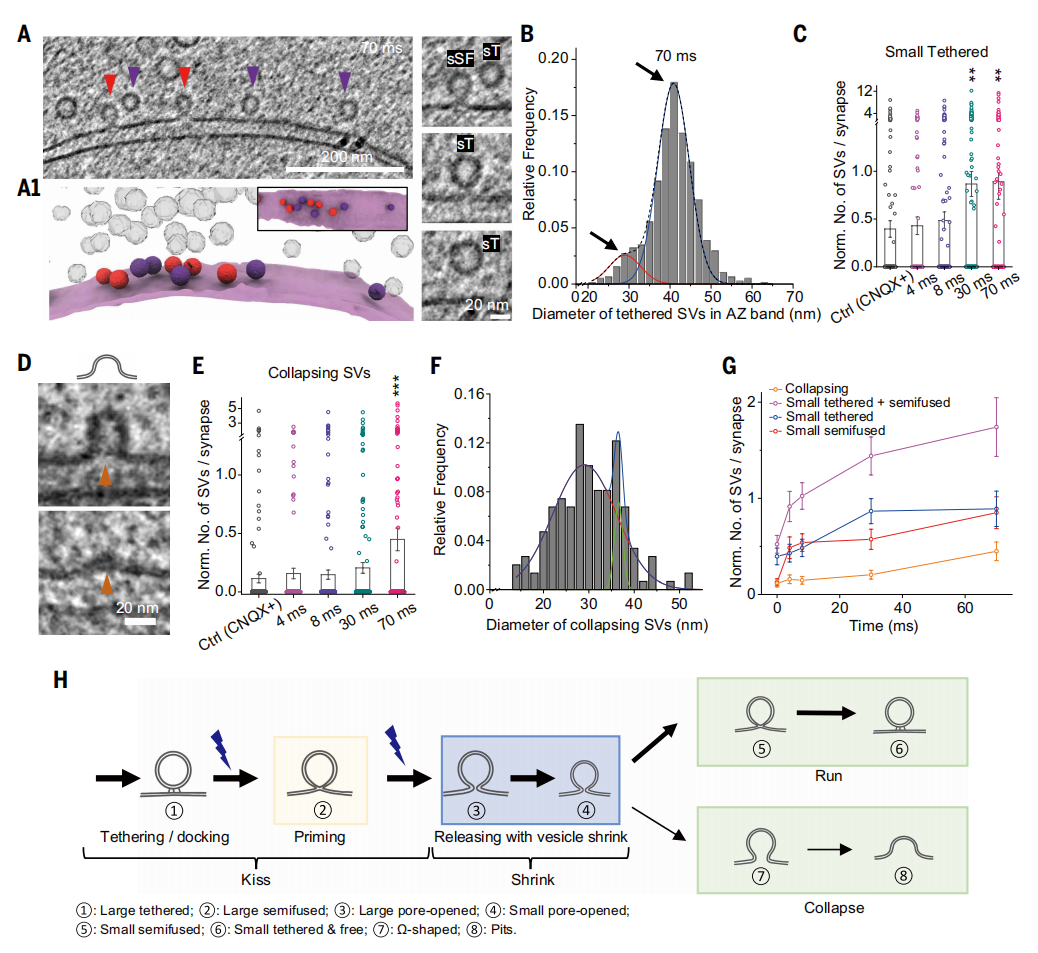
图四 在完成“吻-缩”后,突触小泡主要通过“逃离”方式实现回收[6]
最后,研究者深入探究AZ带内逃离囊泡,即小型锚定与游离态囊泡的最终去向。对动作电位后>100 ms时间点冻结的突触进行时间分辨冷冻电镜研究。在此时间点,观察到位于AZ带外侧的小型囊泡(图五A和B),推测这些囊泡是经“吻-缩-逃”路径后从AZ带迁移而来。这些再循环囊泡主要分布于突触前末梢内囊泡集群的外周区域(图五C),表明逃离囊泡不会直接融入常规尺寸囊泡的储备池。在动作电位后100-300 ms期间,AZ周边区域出现直径约80 nm的大型内吞结构增多现象(图五A、D和E),这些结构很可能对应既往报道的超速内吞[9]。相比之下,网格蛋白介导的内吞在0-300 ms时间窗内保持稳定(图五E)。这些观察结果提示,超速内吞可补偿由“吻-缩-逃”和“吻-缩-全融合”两种囊泡胞吐模式造成的膜损失(图五F)。
综上所述,该研究利用时间分辨细胞冷冻电子断层扫描技术,毫秒级精度捕捉大鼠海马神经元突触小泡胞吐的瞬时中间状态,证实动作电位触发后小泡会经历快速的“吻-缩-逃”过程。突触小泡首先与突触前膜直接接触,随后形成狭窄融合孔后迅速收缩,通过扩散与压力驱动双重机制释放神经递质,继而通常在数十毫秒内脱离突触前膜,实现超快速回收。该“吻-缩-逃”过程占释放事件的80%以上,少数囊泡则经历“吻-缩-全融合”过程实现胞吐。该研究调和了长期争议的“吻-逃”与“全融合”模型,为囊泡胞吐与循环过程提供了统一的机制框架。

GTP研发中心负责实施基因组标签计划(Genome tagging project, GTP),基于自主知识产权的类精子干细胞介导半克隆技术,为全基因组的功能基因一一贴上标签,致力于构建标签细胞和标签小鼠资源库。类精子干细胞是从精子来源单倍体囊胚中建系获得的一种孤雄单倍体胚胎干细胞,将其注入卵母细胞,能够像精子一样支持整个胚胎发育过程,产生健康的半克隆小鼠。GTP研发中心在类精子干细胞的蛋白质编码基因上原位敲入标签序列,建立了液氮保存的标签细胞资源库。研究需要时,利用半克隆技术将标签细胞注射到小鼠卵母细胞中,一步法获得标签小鼠。

已有标签产品可直接订购,详情查阅以下官网链接。如有需要欢迎联系,我们将竭诚为您服务。
标签细胞网址:
标签小鼠网址:
http://www.sibcb.ac.cn/gtp/msearch.jsp
地址:上海市岳阳路320号
责任编辑:多一百
新媒体运营:suway
参考文献
1. Del Castillo J, Katz B: Quantal components of the end-plate potential. The Journal of physiology 1954, 124(3):560-573.
2. Südhof TC: Neurotransmitter release: the last millisecond in the life of a synaptic vesicle. Neuron 2013, 80(3):675-690.
3. Taschenberger H, Woehler A, Neher E: Superpriming of synaptic vesicles as a common basis for intersynapse variability and modulation of synaptic strength. Proceedings of the National Academy of Sciences of the United States of America 2016, 113(31):E4548-4557.
4. Wu LG, Hamid E, Shin W, Chiang HC: Exocytosis and endocytosis: modes, functions, and coupling mechanisms. Annual review of physiology 2014, 76:301-331.
5. Harata NC, Aravanis AM, Tsien RW: Kiss-and-run and full-collapse fusion as modes of exo-endocytosis in neurosecretion. Journal of neurochemistry 2006, 97(6):1546-1570.
6. Tao CL, Tian CL, Liu YT, Lu ZH, Qi L, Li XW, Li C, Shen X, Gu ML, Huang WL et al: "Kiss-shrink-run" unifies mechanisms for synaptic vesicle exocytosis and hyperfast recycling. Science 2025, 390(6770):eads7954.
7. Held RG, Liang J, Brunger AT: Nanoscale architecture of synaptic vesicles and scaffolding complexes revealed by cryo-electron tomography. Proceedings of the National Academy of Sciences of the United States of America 2024, 121(27):e2403136121.
8. Volman V, Gerkin RC, Lau PM, Ben-Jacob E, Bi GQ: Calcium and synaptic dynamics underlying reverberatory activity in neuronal networks. Physical biology 2007, 4(2):91-103.
9. Watanabe S, Rost BR, Camacho-Pérez M, Davis MW, Söhl-Kielczynski B, Rosenmund C, Jorgensen EM: Ultrafast endocytosis at mouse hippocampal synapses. Nature 2013, 504(7479):242-247.
转载请注明来源于【GTP研发中心】
声明:本文仅用于分享,不代表GTP研发中心立场,若有侵权,请及时联系我们第一时间更正!



